
(18分)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能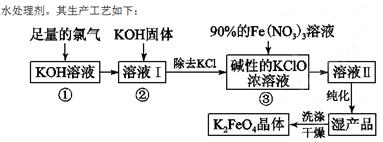
(1)反应①应在温度较低的情况下进行。因在温度较高时KOH与Cl2反应生成的是KClO3。写出在温度较高时KOH与Cl2反应的化学方程式 ,该反应的氧化产物是 。
(2)在溶液Ⅰ中加入KOH固体的目的是 (填编号)。
| A.与溶液Ⅰ中过量的Cl2继续反应,生成更多的KClO |
| B.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |
| C.为下一步反应提供碱性的环境 |
| D.使KClO3转化为KClO |
 +____H2O — ____Fe(OH)3(胶体)+____O2↑+____OH-。
+____H2O — ____Fe(OH)3(胶体)+____O2↑+____OH-。 (1)6KOH+3Cl2 KClO3+5KCl+3H2O KClO3 (2)AC(3分)
KClO3+5KCl+3H2O KClO3 (2)AC(3分)
(3)2Fe3++3ClO-+10OH-===2FeO +3Cl-+5H2O(2分)
+3Cl-+5H2O(2分)
(4)用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净
(5)4 10 4 3 8(2分)
解析试题分析:(1)据题目信息、氧化还原反应中化合价发生变化确定产物有:KClO3、KCl、H2O,根据电子得失守恒和质量守恒来配平,可得6KOH+3Cl2 KClO3+5KCl+3H2O;Cl2既是氧化剂又是还原剂,氯化合价升高,得到 KClO3,KClO3是还原产物。
KClO3+5KCl+3H2O;Cl2既是氧化剂又是还原剂,氯化合价升高,得到 KClO3,KClO3是还原产物。
(2)A、根据生产工艺流程图,第①步氯气过量,加入KOH固体后会继续反应生成KClO,正确;B、因温度较高时KOH 与Cl2 反应生成的是KClO3,而不是KClO,错误; C、第③步需要碱性条件,所以碱要过量,正确;D、KClO3转化为 KClO,化合价只降不升,错误。
(3)据题目信息和氧化还原反应中化合价发生变化确定找出反应物:Fe3+、ClO-,生成物:FeO42-、Cl-,根据电子得失守恒和质量守恒来配平,可得2Fe3++3ClO-+10OH-=2FeO42-+
3Cl-+5H2O
(4)因只要检验最后一次的洗涤中无Cl-,即可证明K2FeO4晶体已经洗涤干净,所以检验方法为:用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净。
(5)根据电子得失守恒和质量守恒来配平,可得4FeO42-+10H2O═4Fe(OH)3(胶体)+3O2↑+8OH-。
考点:本题考查化学流程的分析、氧化还原反应原理、晶体洗涤干净的方法。


科目:高中化学 来源: 题型:单选题
能在水溶液中大量共存的一组离子是
| A.Na+、Mg2+、I-、ClO- | B.Al3+、NH4+、SO42-、Cl- |
| C.K+、Ag+、NO3-、Cl- | D.NH4+、Na+、OH-、SiO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子方程式中,正确的
| A.在AlCl3溶液中加入过量氨水:Al3+ + 3NH3·H2O =Al(OH)3↓ + 3NH4+ |
| B.大理石加入过量盐酸中:CO32-+2H+= CO2↑+H2O |
| C.稀硫酸和Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D.在CuSO4溶液中加入Ba(OH)2溶液:Ba2+ + SO42- =BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子方程式的书写正确的是( )
| A.铁和稀硫酸反应:2Fe + 6H+ =2Fe 3+ +3H 2↑ |
| B.NaHCO3溶液与NaOH溶液反应: OH― + HCO3―= CO32― + H2O |
| C.钠和冷水反应 Na+2H2O=Na++2OH-+H2↑ |
| D.氯化铝溶液中加入过量的氨水 Al3+ + 4NH3·H2O =AlO2- + 4NH4++ 2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液中会发生如下反应:Mn2++ S2O82-+H2O→MnO4-+SO42一十H+该反应常用于检验Mn2+的存在。其特征现象是 。若反应中有0.1 mol还原剂参加反应,则消耗氧化剂的物质的量为 mol。
(2)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有 。
(3)将NaBiO3固体(黄色微溶)加入到MnSO3和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应: NaBiO3+ MnSO4+ H2S04→ Na2S04+ Bi2(SO4)3+ NaMnO4+ H2O。
①配平上述反应的化学方程式;
②上述反应中还原产物是 。
③用单线桥表示该氧化还原反应 。
(4)S2O82-在一定条件下,可转变为S2O32-,写出往K2S2O3中滴加稀硫酸的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(8分)写出下列反应的离子方程式
(1)含少量NaHCO3的溶液与含过量Ba(OH)2的溶液混合: ;
(2)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式 ;
(3)硫酸铜溶液和氢氧化钡溶液混合
(4)用醋酸除去水壶中的水垢
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分) A、B、C、D、E是位于短周期的主族元素。已知:①热稳定性:HmD>HmC;②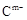 、
、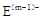 具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
HmDm的电子式___________________。(1分)
能证明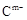 、
、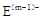 的还原性强弱的离子方程式为__________________________________。
的还原性强弱的离子方程式为__________________________________。
(3)将E的单质通入A与D形成的化合物的水溶液中,其离子方程式为:__________________________。
(4)常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液等体积混合,写出该反应的离子方程式 。
在该溶液中溶质中含有的化学键类型是 (1分)
(5)在A、B、C、E单质中,符合下列转化关系的是_____________(填元素符号)。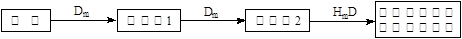
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(14分)氧化锌是橡胶、油漆、搪瓷、电缆、医药、电子、化学等工业的重要原料。以氧
化锌粗品为原料制备活性氧化锌的生产工艺流程如下: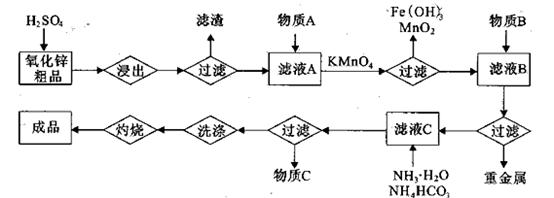
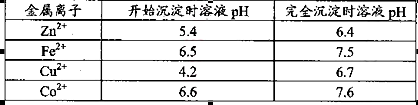
(1).浸出”后得到的酸性溶液中含有Zn2+、SO42-,另含有Fe2+、Cu2+、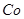 +、Mn2+等
+、Mn2+等
杂质。物质A的作用是调节溶液的pH至5 4,物质A最好选择________。
| A.NH3.H2O | B.Na2CO3 | C.H2SO4 | D.ZnO |
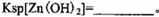 。
。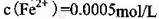 ,则处理1
,则处理1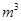 该溶液,Fe2+所消耗的KMnO4的质量为________g(保留两位有效数字)。
该溶液,Fe2+所消耗的KMnO4的质量为________g(保留两位有效数字)。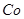 2+可利用置换反应除去,则物质B是_________。
2+可利用置换反应除去,则物质B是_________。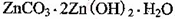 ,生成该沉淀的化学方程式为________。
,生成该沉淀的化学方程式为________。查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有一无色透明的溶液,要确定是否含有以下离子:H+、K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如下:
| 实验步骤 | 实验现象 |
| (1)取少量该溶液,加几滴紫色石蕊溶液 | 溶液变红色 |
| (2)取少量该溶液加热浓缩,加Cu片和浓H2SO4,加热 | 有无色气体产生,气体遇空气可以变成红棕色 |
| (3)取少量该溶液,加BaCl2溶液 | 有白色沉淀生成 |
| (4)取(3)中上层清液,加AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于HNO3 |
| (5)取少量该溶液,加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com