
| ||


科目:高中化学 来源: 题型:
| A、WZ2分子中所有原子最外层都为8电子结构 |
| B、WX2、ZX2的化学键类型相同 |
| C、WX2是以极性键结合成的直线型分子 |
| D、原子半径大小顺序 W<X<Y<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 4 |
| 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
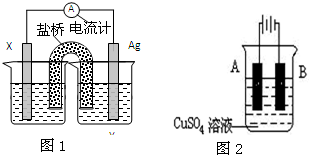 (Ⅰ)依据氧化还原反应:2Ag+(aq)+Fe(s)=Fe2+(aq)+2Ag(s)设计的原电池如图1所示.
(Ⅰ)依据氧化还原反应:2Ag+(aq)+Fe(s)=Fe2+(aq)+2Ag(s)设计的原电池如图1所示.查看答案和解析>>
科目:高中化学 来源: 题型:
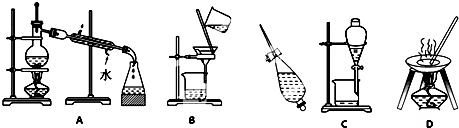
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| a | |||||||
| b | c | ||||||
| d | e | f | |||||
| 名称 | 常温时的状态 | 结构简式 | 熔点/.C | 沸点/.C | 相对密度 |
| 甲烷 | 气 | CH4 | -l82.5 | -161.5 | |
| 乙烷 | 气 | CH3CH3 | -l82.8 | -88.6 | |
| 丙烷 | 气 | CH3CH2CH3 | -188.0 | -42.1 | 0.5005 |
| 戊烷 | 液 | CH3(CH2)3CH3 | -129.7 | 36.0 | 0.5572 |
| 癸烷 | 液 | CH3(CH2)3CH3 | -29.7 | 172.1 | 0.7298 |
| 十七烷 | 固 | CH3(CH2)15CH3 | 22 | 302.2 | 0.7767 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | |
| Z | W |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com