
 Cu2++2NO2↑+2H2O或3Cu+8H++2NO3-
Cu2++2NO2↑+2H2O或3Cu+8H++2NO3- 3Cu2++2NO↑+4H2O Au Pt
3Cu2++2NO↑+4H2O Au Pt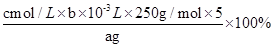 c
c Cu2++2NO2↑+2H2O或3Cu+8H++2NO3-
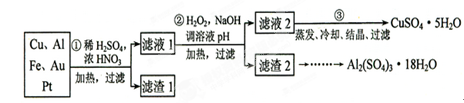
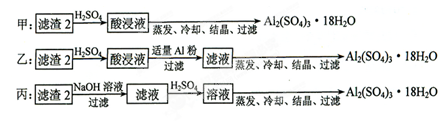
Cu2++2NO2↑+2H2O或3Cu+8H++2NO3- 3Cu2++2NO↑+4H2O;由于浓硝酸也不能溶解金和Pt,所以滤渣1的主要成分为Au和Pt。
3Cu2++2NO↑+4H2O;由于浓硝酸也不能溶解金和Pt,所以滤渣1的主要成分为Au和Pt。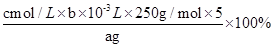 ;锥形瓶不需要干燥,a不影响;滴定终点时滴定管尖嘴中产生气泡,说明消耗的标准液体积偏小,则测定结果偏低;未除净可与EDTA反应的干扰离子,则消耗的标准液体积偏大,测定结果偏高,答案选c。
;锥形瓶不需要干燥,a不影响;滴定终点时滴定管尖嘴中产生气泡,说明消耗的标准液体积偏小,则测定结果偏低;未除净可与EDTA反应的干扰离子,则消耗的标准液体积偏大,测定结果偏高,答案选c。

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源:不详 题型:实验题
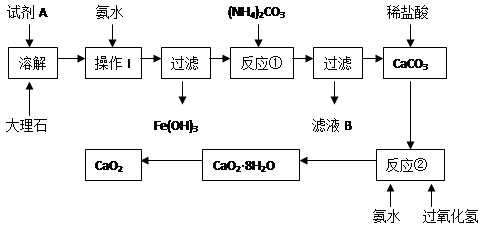
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
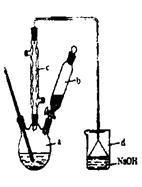
| | 苯 | 溴 | 溴苯 |
| 密度/gcm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中的溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
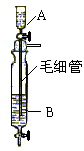
| A.A中装浓硫酸,B中装浓盐酸 |
| B.A中装浓盐酸,B中装浓硫酸 |
| C.A中装氢氧化钠浓溶液,B中装浓氨水 |
| D.A中装浓氨水,B中装氢氧化钠浓溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.液体分两层,石蕊层仍为紫色,有机层呈无色 |
| B.石蕊层为三层环,由上而下是蓝、紫、红色 |
| C.石蕊层有两层,上层为紫色,下层为蓝色 |
| D.石蕊层为三层环,由上而下是红、紫、蓝色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com