
【题目】研究发现,在![]() 低压合成甲醇反应(
低压合成甲醇反应(![]() )中,
)中,![]() 氧化物负载的
氧化物负载的![]() 氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)![]() 和
和![]() 分子中
分子中![]() 原子的杂化形式分别为__________和__________。
原子的杂化形式分别为__________和__________。
(2)在![]() 低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为____,原因是_____。
低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为____,原因是_____。
(3)硝酸锰是制备上述反应催化剂的原料,![]() 中的化学键除了
中的化学键除了![]() 键外,还存在__________。
键外,还存在__________。
【答案】![]()
![]()
![]()
![]() 与
与![]() 均为极性分子,
均为极性分子,![]() 中氢键比甲醇多;
中氢键比甲醇多;![]() 与
与![]() 均为非极性分子,
均为非极性分子,![]() 分子量较大、范德华力较大 离子键和
分子量较大、范德华力较大 离子键和![]() 键(
键(![]() 键)
键)
【解析】
(1)![]() 中
中![]() 的价层电子对数为2,所以为
的价层电子对数为2,所以为![]() 杂化,
杂化, ![]() 分子中C的价层电子对数为4,故为
分子中C的价层电子对数为4,故为![]() 杂化,故答案为:
杂化,故答案为:![]() ;
;![]() ;
;
(2)水和甲醇均为极性分子,常温常压下两种物质均呈液态;二氧化碳和氢气均为非极性分子,常温常压下两种物质均呈气态,根据四种物质在相同条件下的状态可以判断出水甲醇的沸点均高于二氧化碳、氢气的沸点。由于水分子中的2个氢原子都能参与氢键的形成,而甲醇分子中只有羟基上的氢原子能够形成氢键,所以水中的氢键比甲醇多,则水的沸点高于甲醇的沸点。二氧化碳和氢气都属于分子晶体,但由于二氧化碳的相对分子质量大于氢气,所以二氧化碳的沸点高于氢气的沸点,故答案为:![]() ;
;![]() 与
与![]() 均为极性分子,
均为极性分子,![]() 中氢键比甲醇多;
中氢键比甲醇多;![]() 与
与![]() 均为非极性分子,
均为非极性分子,![]() 分子量较大、范德华力较大;
分子量较大、范德华力较大;
(3)![]() 是离子化合物,存在离子键;此外在
是离子化合物,存在离子键;此外在![]() 中,3个O原子和中心原子
中,3个O原子和中心原子![]() 之间还形成一个4中心6电子的大
之间还形成一个4中心6电子的大![]() 键(
键(![]() 键),所以
键),所以![]() 中的化学键有
中的化学键有![]() 键、
键、![]() 键和离子键,故答案为:离子键和
键和离子键,故答案为:离子键和![]() 键(
键(![]() 键)。
键)。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.ns电子的能量可能低于(n-1)p电子的能量
B.6C的电子排布式1s22s22p![]() ,违反了洪特规则
,违反了洪特规则
C.电子排布式(21Sc)1s22s22p63s23p63d3违反了能量最低原理
D.电子排布式(22Ti)1s22s22p63s23p10违反了泡利不相容原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A、B是两种单烯烃,A分子中含有6个碳原子,B分子中含有4个碳原子,其中A的核磁共振氢谱中只有一个吸收峰而B有两个;②烯烃复分解反应可表示为R1CH=CHR2+R1’CH=CHR2’![]() R1CH=CHR1’+R2CH=CHR2’。
R1CH=CHR1’+R2CH=CHR2’。
请根据如图转化关系,回答相关问题:
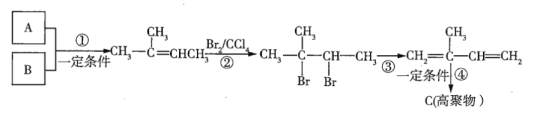
(1)反应②的反应类型为___,反应③的反应条件为___。
(2)当![]() 与Br2,按物质的量之比为1:1反应时,所得产物的结构简式为___、___、__。
与Br2,按物质的量之比为1:1反应时,所得产物的结构简式为___、___、__。
(3)聚异戊二烯是天然橡胶的主要成分,其中天然橡胶为顺式聚异戊二烯,杜仲胶为反式聚异戊二烯,则反式聚异戊二烯的结构简式为__。
(4)反应①的化学方程式为__。
(5)C的结构简式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】数十亿年来,地球上的物质不断变化,大气的成分也发生了很大的变化。下表是目前空气和原始大气的主要成分:
目前空气的主要成分 |
|
原始大气的主要成分 |
|
用上表所涉及的分子填写下列空白:
(1)含有10个电子的分子有__________(填化学式,下同)。
(2)由极性键构成的非极性分子有________。
(3)与![]() 可直接形成配位键的分子有________
可直接形成配位键的分子有________
(4)不含孤电子对的分子(稀有气体除外)是______,它的立体构型为_______。
(5)极易溶于水且水溶液呈碱性的分子是__________,它之所以极易溶于水是因为它的分子和水分子之间形成了______。
(6)![]() 的结构可表示为
的结构可表示为![]() ,与
,与![]() 结构最相似的分子是______,这两种结构相似的分子的极性__________(填“相同”或“不相同”),
结构最相似的分子是______,这两种结构相似的分子的极性__________(填“相同”或“不相同”),![]() 分子中有一个键的形成与另外两个键不同,它叫_______。
分子中有一个键的形成与另外两个键不同,它叫_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产中常用MnS作为沉淀剂除去工业废水中Cu2+:Cu2++MnS=CuS+Mn2+,下列说法错误的是( )
A.该反应达平衡时c(Mn2+)=c(Cu2+)
B.MnS的Ksp比CuS的Ksp大
C.往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大
D.该反应的平衡常数K=
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想合成具有以下结构的四种烃分子,下列有关说法不正确的是( )

A. 1 mol甲分子内含有10 mol共价键
B. 由乙分子构成的物质不能发生氧化反应
C. 丙分子的二氯取代产物只有三种
D. 分子丁是不可能合成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.2000molL-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3mL酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数请回答:
(1)以上步骤有错误的是___(填编号)。
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入___(从图中选填“甲”或“乙”)中。
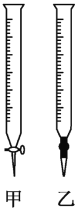
(3)下列操作会引起实验结果偏大的是___(填编号)。
A.在锥形瓶装液前,留有少量蒸馏水
B.滴定前,滴定管尖嘴有气泡,滴定后无气泡
C.用酸式滴定管量取液体时,释放液体前滴定管前端有气泡,之后消失
(4)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视___。判断到达滴定终点的现象是:锥形瓶中溶液___。
(5)以下是实验数据记录表:
滴定次数 | 盐酸体积(mL) | NaOH溶液体积读数(mL) | |
滴定前 | 滴定后 | ||
1 | 20.00 | 0.00 | 21.30 |
2 | 20.00 | 0.00 | 16.30 |
3 | 20.00 | 0.00 | 16.32 |
通过计算可得,该盐酸浓度为___ molL-1(计算结果保留4位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国成功研制出了具有自主知识产权的治疗缺血性脑梗死新药——丁苯酞。有机物G是合成丁苯酞的中间产物,G的一种合成路线如图:

已知:R-Br![]() R-MgBr
R-MgBr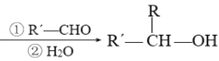
回答下列问题:
(1)A的结构简式是___,E的化学名称是___。
(2)由B生成C的化学方程式为___。
(3)G的结构简式为___。合成丁苯酞的最后一步转化为: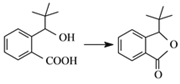 ,则该转化的反应类型是___。
,则该转化的反应类型是___。
(4)参照题中信息和所学知识,写出用![]() 和CH3MgBr为原料(其他无机试剂任选)制备
和CH3MgBr为原料(其他无机试剂任选)制备![]() 的合成路线:___。
的合成路线:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国第二化工设计院提出,用间接电化学法对大气污染物 NO 进行无害化处理,其原理示意如图(质子膜允许H+和 H2O 通过),下列相关判断正确的是
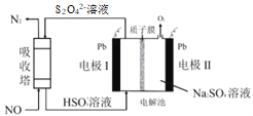
A.电极Ⅰ为阴极,电极反应式为 2H2O+2e- =2OH- +H2↑
B.电解池中质子从电极Ⅰ向电极Ⅱ作定向移动
C.吸收塔中的反应为 2NO+ 2S2O42-+H2O=N2+4HSO3-
D.每处理1molNO电解池质量减少16g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com