
【题目】我国成功研制出了具有自主知识产权的治疗缺血性脑梗死新药——丁苯酞。有机物G是合成丁苯酞的中间产物,G的一种合成路线如图:

已知:R-Br![]() R-MgBr
R-MgBr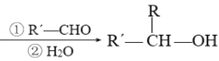
回答下列问题:
(1)A的结构简式是___,E的化学名称是___。
(2)由B生成C的化学方程式为___。
(3)G的结构简式为___。合成丁苯酞的最后一步转化为: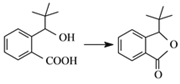 ,则该转化的反应类型是___。
,则该转化的反应类型是___。
(4)参照题中信息和所学知识,写出用![]() 和CH3MgBr为原料(其他无机试剂任选)制备
和CH3MgBr为原料(其他无机试剂任选)制备![]() 的合成路线:___。
的合成路线:___。
【答案】![]() 2-甲基-1-丙烯(或异丁烯)
2-甲基-1-丙烯(或异丁烯) 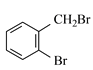 +NaOH
+NaOH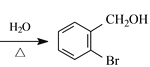 +NaBr
+NaBr 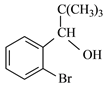 酯化反应(或取代反应)
酯化反应(或取代反应) ![]()
【解析】
A与溴在催化条件下发生取代反应生成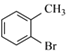 ,可知A为
,可知A为![]() ,
, 与溴在光照时发生侧链的取代反应,由D可知C为
与溴在光照时发生侧链的取代反应,由D可知C为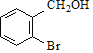 ,则B为
,则B为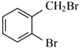 ;由F与Mg/乙醚的反应产物可知F为(CH3)3CBr,则E为
;由F与Mg/乙醚的反应产物可知F为(CH3)3CBr,则E为![]() ,根据信息,生成的G为
,根据信息,生成的G为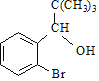 ,据此分析解答。
,据此分析解答。
(1)由以上分析可知A为![]() ,E为
,E为![]() ,E的名称为2-甲基-1-丙烯,故答案为:
,E的名称为2-甲基-1-丙烯,故答案为:![]() ;2-甲基-1-丙烯;
;2-甲基-1-丙烯;
(2)根据流程图,由B生成C,是卤代烃的水解反应,反应的化学方程式为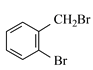 +NaOH
+NaOH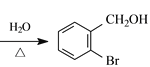 +NaBr,故答案为:
+NaBr,故答案为: +NaOH
+NaOH +NaBr;
+NaBr;
(3)G的结构简式为 ,
,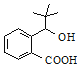 →
→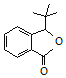 发生的是分子内羟基和羧基的酯化反应,也是取代反应,故答案为:
发生的是分子内羟基和羧基的酯化反应,也是取代反应,故答案为: ;酯化反应(或取代反应);
;酯化反应(或取代反应);
(4)用![]() 和CH3MgBr为原料(其他无机试剂任选)制备
和CH3MgBr为原料(其他无机试剂任选)制备![]() ,可先由
,可先由![]() 发生取代反应生成醇,然后氧化生成酮,与CH3MgBr/水作用可生成
发生取代反应生成醇,然后氧化生成酮,与CH3MgBr/水作用可生成![]() ,合成路线为
,合成路线为![]() ,故答案为:
,故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.碳原子间都以碳碳单键结合,其余的价键均与氢原子结合即为烷烃分子,这一系列化合物的分子通式为![]()
B.分子式相同,各元素质量分数也相同的物质是同种物质
C.烷烃分子中,相邻的三个碳原子有可能在同一条直线上
D.![]() 、
、![]() 互为同系物
互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,在![]() 低压合成甲醇反应(
低压合成甲醇反应(![]() )中,
)中,![]() 氧化物负载的
氧化物负载的![]() 氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)![]() 和
和![]() 分子中
分子中![]() 原子的杂化形式分别为__________和__________。
原子的杂化形式分别为__________和__________。
(2)在![]() 低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为____,原因是_____。
低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为____,原因是_____。
(3)硝酸锰是制备上述反应催化剂的原料,![]() 中的化学键除了
中的化学键除了![]() 键外,还存在__________。
键外,还存在__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能,乙图是一种用惰性电极电解饱和食盐水的消毒液发生器。关于甲、乙的说法正确的是
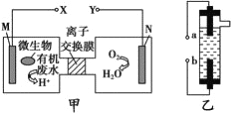
A. 装置乙中的b极要与装置甲的X极连接
B. 装置乙中a极的电极反应式为:2Cl- -2e-=Cl2↑
C. 当N极消耗5.6L(标准状况下)气体时,则有2NA个H+通过离子交换膜
D. 若有机废水中主要含有葡萄糖,则装置甲中M极发生的电极反应为: C6H12O6+6H2O-24e-=6CO2↑+24H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是H3AsO4水溶液中含砷的各物种分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系。下列说法错误的是
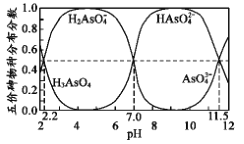
A.NaH2AsO4溶液呈酸性
B.向NaH2AsO4溶液滴加 NaOH 溶液过程中,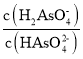 先增加后减少
先增加后减少
C.H3AsO4和HAsO42-在溶液中不能大量共存
D.Ka3( H3AsO 4) 的数量级为10-12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是一种大气污染物,但它在化工和食品工业上却有广泛应用。某兴趣小组同学对SO2的实验室制备和性质实验进行研究。
(1)甲同学按照教材实验要求设计如图所示装置制取SO2
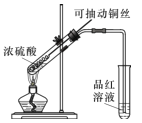
①本实验中铜与浓硫酸反应的化学方程式是 ______,铜丝可抽动的优点是_______。
②实验结束后,甲同学观察到试管底部出现黑色和灰白色固体,且溶液颜色发黑。甲同学认为灰白色沉淀应是生成的白色CuSO4夹杂少许黑色固体的混合物,其中CuSO4以白色固体形式存在体现了浓硫酸的________性。
③乙同学认为该实验设计存在问题,请从实验安全和环保角度分析,该实验中可能存在的问题是________。
(2)兴趣小组查阅相关资料,经过综合分析讨论,重新设计实验如下(加热装置略):
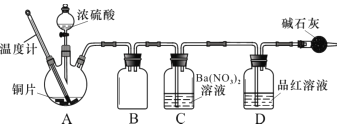
实验记录 A 中现象如下:
序号 | 反应温度/℃ | 实验现象 |
1 | 134 | 开始出现黑色絮状物,产生后下沉,无气体产生 |
2 | 158 | 黑色固体产生的同时,有气体生成 |
3 | 180 | 气体放出的速度更快,试管内溶液为黑色浑浊 |
4 | 260 | 有大量气体产生,溶液变为蓝色,试管底部产生灰白色固体,品红溶液褪色 |
5 | 300 | 同上 |
查阅资料得知: 产物中的黑色和灰白色固体物质主要成分为 CuS、Cu2S 和 CuSO4,其中CuS 和 Cu2S为黑色固体,常温下都不溶于稀盐酸,在空气中灼烧均转化为CuO和SO2。
①实验中盛装浓硫酸的仪器名称为 ____________。
②实验记录表明__________对实验结果有影响,为了得到预期实验现象,在操作上应该____________。
③装置C 中发生反应的离子方程式是 ___________________。
④将水洗处理后的黑色固体烘干后,测定灼烧前后的质量变化,可以进一步确定黑色固体中是否一定含有 CuS其原理为__________(结合化学方程式解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,国家电投集团正在建设国内首座百千瓦级铁-铬液流电池储能示范电站。铁-铬液流电池总反应为Fe2+ + Cr3+![]() Fe3 + + Cr2+,工作示意图如图。下列说法错误的是
Fe3 + + Cr2+,工作示意图如图。下列说法错误的是

A.放电时a电极反应为 Fe 3++e- =Fe2+
B.充电时b电极反应为 Cr3++e- =Cr2+
C.放电过程中H+通过隔膜从正极区移向负极区
D.该电池无爆炸可能,安全性高,毒性和腐蚀性相对较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在人们的日常生活、生产和环保事业中属于“明星物质”。回答下列问题:
(1)氨气是农业肥料和化工生产的重要原料,其电子式为____。
(2)叠氮化钠(NaN3)在药物制备、合成影像、化学分析、汽车制造等行业有着广泛的用途,但该物质极易爆炸,且有副毒。可用NaClO溶液对含有叠氮化钠的溶液进行处理,生成一种无污染的气体单质,反应的化学方程式为______________。
(3)“固氮”是农业科学家研究的永恒主题。在某特殊催化剂和光照条件下,N2与水反应可生成NH3。
已知:
(i)4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H1=-1266 kJ/mol;
2N2(g) +6H2O(g) △H1=-1266 kJ/mol;
(ii)H2O(g)=H2O(l) △H2= -44.0kJ/mol。
则2N2(g) +6H2O(l)![]() 4NH3(g)+3O2(g) △H3=______kJ/mol。
4NH3(g)+3O2(g) △H3=______kJ/mol。
(4)目前“人工固氮”最成功的应用就是工业合成氨:
N2(g) +3H2(g)![]() 2NH3(g) △H=-92.4kJ/mol。将1.00molN2和3.00molH2充入到容积为3L的恒容密闭容器中,发生上述反应。
2NH3(g) △H=-92.4kJ/mol。将1.00molN2和3.00molH2充入到容积为3L的恒容密闭容器中,发生上述反应。

①图甲是测得X、Y 的浓度随时间变化的曲线.其中Y 为_____(写化学式),反应达到平衡时的平均反应速率v(N2) =_________。
②在不同温度和压强下,平衡体系中NH3的体积分数与温度、压强关系如图乙,则压强p1_____p2(填“>”“<”“=”或“不确定”,下同),B、D 两点的平衡常数KB____KD,B 点N2 的转化率=_________(保留3位有效数字)。
(5)“绿水青山就是金山银山”,利用原电池原理(6NO2 +8NH3=7N2+12H2O)可以处理氮的氧化物和NH3 尾气,装置原理图如图丙:

负极反应式为__________,当有标准状况下4.48 L NO2被处理时,转移电子的物质的量为_____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法正确的是( )
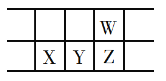
A.原子半径:W>Z
B.常温下,X的单质与Y的单质均能溶于浓硫酸
C.X的最高价氧化物的水化物是强碱
D.最简单气态氢化物热稳定性:Z<W
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com