
【题目】向0.1molL﹣1 . 醋酸溶液中逐滴加入氨水至过量时,溶液的导电能力将发生相应的变化,其电流强度I随加入氨水的体积(V)变化的曲线关系是图中的( )
A.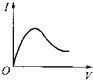
B.
C.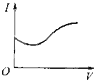
D.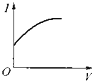
科目:高中化学 来源: 题型:
【题目】把0.3mol铜完全溶解于某浓度的硝酸中收集到0.3mol 气体,则反应消耗硝酸的物质的量为( )
A.1.2molB.0.8molC.0.9molD.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境中氮氧化物的合理控制和治理是减少雾霾天气、优化生存环境的有效途径之一.请运用化学反应原理知识,回答下列问题:.
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知: ①CH4 (g)+4NO2 (g)═4NO(g)+CO2 (g)+2H2O(1)△H1=﹣662kJmol﹣1
②CH4 (g)+4NO(g)═2N2 (g)+CO2 (g)+2H2O(1)△H2=﹣1251kJmol﹣1
据此,写出CH4将NO2还原为N2的热化学方程式:
(2)用活性炭还原法也可处理氮氧化物.有关反应为:C(s)+2NO(g)N2 (g)+CO2 (g)某研究小组向一个容积(3L)恒定的真空密闭容器中加人0.3mol NO和足量的活性炭与催化剂(固体试样的体积忽略不计),在恒温(T1℃)条件下发生反应,经10min反应达到平衡,测得N2的物质的量为0.09mol. ①0min~10min内以v(NO)表示的平均化学反应速率为 .
②下列各项能判断该反应达到平衡状态的是 .
A.容器内压强保持不变
B.速率关系:2v(NO)(正)=v (N2)(逆)
C.容器内CO2的体积分数不变
D.混合气体的密度保持不变
③在相同条件下,若在容器中放人生石灰,则NO的平衡转化率(填“增大”、“不变”或“减小”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制取纯净的CuCl22H2O的主要过程是:①将粗氧化铜(含少量Fe及不溶于酸的杂质)溶解于稀盐酸中,过滤;②对①所得滤液按下列步骤进行操作: 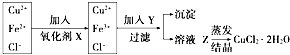 已知Fe3+、Fe2+、Cu2+开始沉淀时的pH分别为1.9、7.0、4.7,沉淀完全时pH分别为3.2、9.0、6.7.请回答以下问题:
已知Fe3+、Fe2+、Cu2+开始沉淀时的pH分别为1.9、7.0、4.7,沉淀完全时pH分别为3.2、9.0、6.7.请回答以下问题:
(1)已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性,其中最适合的X是 , 其反应的离子方程式是 .
(2)Y物质的作用是调节溶液酸性,使pH为3~4.现有下列试剂,可选用的有(填代号).
A.氨水
B.Cu(OH)2
C.Cu2(OH)2 CO3
D.Na2CO3
(3)若Y用CuO,则除去Fe3+的离子方程式是
(4)溶液Z在蒸发结晶时应注意 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素X 的最高价含氧酸的化学式为 HnXO2n﹣2,则在其气态氢化物中 X 的化合价为( )
A.﹣(12﹣5n)B.﹣(12﹣3n)C.﹣(6﹣3n)D.﹣(10﹣n)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的说法中正确的是( )
A. 苯与H2在一定条件下的加成产物环己烷![]() 中,所有碳原子在同一平面上
中,所有碳原子在同一平面上
B. ![]() 可以用于表示苯的分子结构,但是其中并不含有碳碳双键,因此苯的性质跟烯烃不相同
可以用于表示苯的分子结构,但是其中并不含有碳碳双键,因此苯的性质跟烯烃不相同
C. 苯的分子式是C6H6,苯分子中的碳原子远没有饱和,因此能与溴水发生加成反应而使之褪色
D. 苯环上的碳碳键是一种介于单键和双键之间的独特的键,因此苯可以发生取代反应不能发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3-CH=CH-COOH,该有机物能发生的反应是( )
①取代反应 ②加成反应 ③使溴水褪色 ④使酸性KMnO4溶液褪色 ⑤酯化反应 ⑥聚合反应
A.以上反应均可发生B.只有⑤不能发生C.只有⑥不能发生D.只有②不能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是

A. 正极反应为AgCl +e-=Ag +Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性, r溶液是一种常见的强酸,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是

A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态
D. X的最高价氧化物的水化物为强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com