
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ʱ�������������������̨����Ȧ��ֱ���þƾ���������� |
| B������ʱ���¶ȼ�ˮ�������Բ����ƿ��Һ��֮�£�����ˮ���������¿ڽ� |
| C����ȡʱ���ֱ��������ձ����¿ڽ����л����ˮ�� |
| D������100ml 0.100 mol/L������ͭ��Һʱ���ɽ�2.50�˵�������100mL����ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������Ư�۳���������ˮ�ľ�����ɱ�����������ߵ�����ԭ����ͬ |
| B����PH��ֽ�����ˮ��PHԼΪ3 |
| C��������H2��Cl2�а�����ȼ�գ�������ɫ�Ļ��棬����ƿ���а������� |
| D����������ˮ��Ӧ���ɴ���������ᣬ������ˮ���ձ�Ϊϡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ڢ� | B���ڢ� | C���٢� | D���٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CuSO4��Һ��Ba��OH��2��Һ��ϣ�Ba2++SO42-=BaSO4�� |
| B������ʯ��ˮ��ϡ���ᷴӦ��OH-+H+=H2O |
| C��NaHSO3��Һ��NaHSO4��Һ��ϣ�SO32-+2H+=H2O+SO2�� |
| D��������������ͭ��Һ�У�Fe+3Cu2+=2Fe3++3Cu |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��BF3 |
| B��CCl4 |
| C��NH3 |
| D��H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| ||
| A��+335.7 |
| B��-335.7 |
| C��+16.3 |
| D��-16.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��C2H5OH��1��+3O2��g��=2CO2��g��+3H2O��1����H=-Q | ||||||
B��C2H5OH��1��+3O2��g��=2CO2��g��+3H2O��1����H=-
| ||||||
C��
| ||||||
| D��C2H5OH��1��+3O2��g��=2CO2��g��+3H2O��1����H=-2Q |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| 1 |
| 2 |
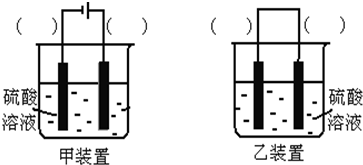
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com