

| 1 |
| 2 |
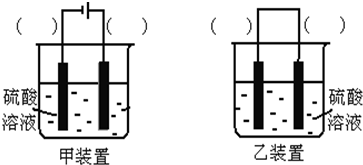
| 1 |
| 2 |
| 1 |
| 2 |
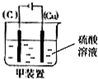 ,
, .
.


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Fe2+、SO42-、Mg2+ |
| B、Na+、Cl-、NH4+、S2- |
| C、Al3+、Na+、Cl-、S2- |
| D、Na+、K+、Br-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| A | 单质为密度最小的气体 |
| B | 元素最高正价与最低负价之和为0 |
| D | 可形成D2、D3两种气态单质,其中一单质是保护地球地表环境的重要屏障 |
| E | 存在质量数为23,中子数为12的核素 |
| F | 单质F为淡黄色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电子层结构相同的微粒,其化学性质一定相似 |
| B、第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| C、非金属元素的原子两两结合形成的化合物不一定是共价化合物 |
| D、元素周期律是元素原子核外电子排布周期性变化的结果 |
查看答案和解析>>
科目:高中化学 来源: 题型:
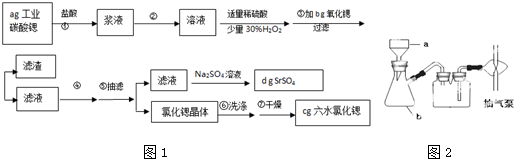
查看答案和解析>>
科目:高中化学 来源: 题型:
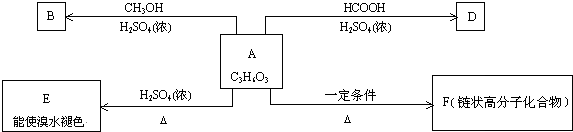
查看答案和解析>>
科目:高中化学 来源: 题型:
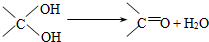

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com