

| 106 |
| 12 |
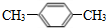 .A与氯气在光照条件下发生甲基上的取代反应生成B与C,B只有一个吸收峰,则A中甲基上H原子被全部取代生成B,则B为
.A与氯气在光照条件下发生甲基上的取代反应生成B与C,B只有一个吸收峰,则A中甲基上H原子被全部取代生成B,则B为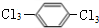 ,B发生水解反应、酸化得到D,结合一个碳原子上连有两个羟基时不稳定,易转化为C=O,则D为
,B发生水解反应、酸化得到D,结合一个碳原子上连有两个羟基时不稳定,易转化为C=O,则D为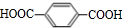 ,D与1-丙醇发生酯化反应生成E,由E的分子式可知,应是1分子D与2分子1-丙醇发生酯化反应,则E为
,D与1-丙醇发生酯化反应生成E,由E的分子式可知,应是1分子D与2分子1-丙醇发生酯化反应,则E为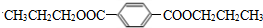 .C发生水解反应生成F,F连续发生氧化反应生成D,则C为
.C发生水解反应生成F,F连续发生氧化反应生成D,则C为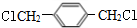 ,F为
,F为 ,H为
,H为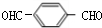 .F与D发生缩聚反应生成G为
.F与D发生缩聚反应生成G为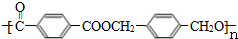 ,据此解答.
,据此解答.| 106 |
| 12 |
 .A与氯气在光照条件下发生甲基上的取代反应生成B与C,B只有一个吸收峰,则A中甲基上H原子被全部取代生成B,则B为
.A与氯气在光照条件下发生甲基上的取代反应生成B与C,B只有一个吸收峰,则A中甲基上H原子被全部取代生成B,则B为 ,B发生水解反应、酸化得到D,结合一个碳原子上连有两个羟基时不稳定,易转化为C=O,则D为
,B发生水解反应、酸化得到D,结合一个碳原子上连有两个羟基时不稳定,易转化为C=O,则D为 ,D与1-丙醇发生酯化反应生成E,由E的分子式可知,应是1分子D与2分子1-丙醇发生酯化反应,则E为
,D与1-丙醇发生酯化反应生成E,由E的分子式可知,应是1分子D与2分子1-丙醇发生酯化反应,则E为 .C发生水解反应生成F,F连续发生氧化反应生成D,则C为
.C发生水解反应生成F,F连续发生氧化反应生成D,则C为 ,F为
,F为 ,H为
,H为 .F与D发生缩聚反应生成G为
.F与D发生缩聚反应生成G为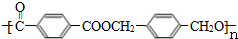 ,
, ,G的结构简式为
,G的结构简式为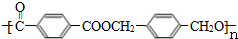 ,
, ;
;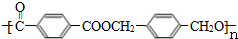 ;
; ,其含氧官能团为:醛基,D为
,其含氧官能团为:醛基,D为 ,含氧官能团为:羧基,故答案为:醛基;羧基;
,含氧官能团为:羧基,故答案为:醛基;羧基; ,侧链中碳原子均处于苯环的平面内,分子中有8个碳原子肯定共平面,故答案为:8;
,侧链中碳原子均处于苯环的平面内,分子中有8个碳原子肯定共平面,故答案为:8; ,
, ;
; ,含有醇羟基,可以发生取代反应,羟基连接碳原子上有氢原子,可以发生氧化反应,羟基连接碳原子相邻的碳原子上,没有氢原子,不能发生消去反应,含有苯环,可以与氢气发生加成反应,
,含有醇羟基,可以发生取代反应,羟基连接碳原子上有氢原子,可以发生氧化反应,羟基连接碳原子相邻的碳原子上,没有氢原子,不能发生消去反应,含有苯环,可以与氢气发生加成反应,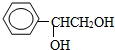 ,
, .
.


科目:高中化学 来源: 题型:

| 1 |
| 2 |
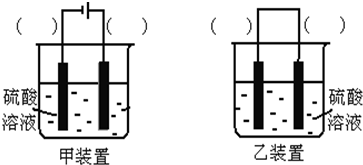
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该温度和压强可能是标准状况 |
| B、标准状况下该纯净物若为气态,其体积是22.4L |
| C、该气体分子为双原子分子 |
| D、若在该条件下O2为气态,则此时1mol O2的体积为30L |
查看答案和解析>>
科目:高中化学 来源: 题型:
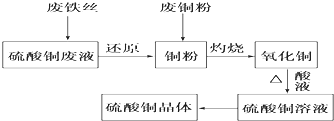
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
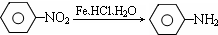 (苯胺、弱碱性、易氧化)
(苯胺、弱碱性、易氧化)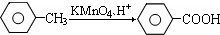
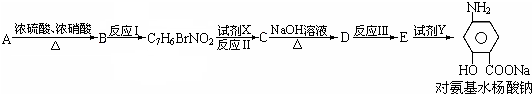
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com