
����Ŀ�����Ƶı�����ˮ�к��ж���������ijУ��ѧ�о���ѧϰС���ͬѧΪ̽�������ʣ���������ʵ�飬���������ɡ�
��1��������ʹʪ��ĺ�ɫ������ɫ��ʹ����ɫ�����Ļ�ѧʽ��__________��
��2������ˮ����һ��ʱ�����Һ��ɫ��dz���йط�Ӧ�Ļ�ѧ����ʽΪ__________��__________��
��3�����Ƶı�����ˮ��̼��Ƶķ�Ӧ����ȡ��ŨHClO ��Һ �� �� �� ֮һ��
ʵ��һ �����о���

������ͼ��ʾ�����Թ��м�������Ŀ�״̼��ƣ��ټ���Լ20 mL���Ƶı�����ˮ����ַ�Ӧ�����������ݲ�������Һdz����ɫ��ȥ��
�������ˣ�����Һ������ɫ�����ϣ����������ˮ��Ư���Ը�ǿ��
����Ϊ��ȷ����Ӧ�������Һ��Ϊ���ݣ��ֱ��������ʵ����
��һ����ʯ��ˮ��ϣ���������������ɫ����;
�ڶ�����ϡ�����ϣ���������������ɫ���壬
�������ݼ��ȣ��۲쵽��Һ��������д�����ɫ���������
����⣬����ʵ���в�������ɫ�����ΪCO2��
����Ӧ�����õ���ҺƯ������ǿ��ԭ����__________________________________________________��
����������ʵ�����֪������������Һ�е����ʳ�CaCl2��HClO�⣬����__________��
ʵ��� �����о���
������A�ڣ�������������ס�Ŀ�״̼���(����)��150 mL���Ƶı�����ˮ������ͼ��ʾװ��ʵ��(ʵ��ǰ����B�г����˱���NaHCO3��Һ)�������ٲ������ݺ�������������ʣ���̼������Һ�棬�ܷ���ټ�����ƿ�е�Һ����ֱ������B�е����岻������(������HClO�ķֽ�)��

������A������Ϊ__________��
��ȷ��������B�����������ʵ�����������������a���ȴ�����A��ȴ������;b��____________��c�� ƽ����̶������е�Һ�������
��ʵ������������B���ռ�������������ڱ�״����Ϊ168mL����150mL ���Ƶı�����ˮ�����̼�����ȫ��Ӧ��������Һ��HClO�����ʵ���Ũ��Ϊ__________��(��Ӧǰ����Һ����仯���Բ���)
���𰸡� HClO Cl2+ H2O![]() HCl+ HClO 2HClO
HCl+ HClO 2HClO![]() 2HCl+O2 �� CaCO3 ������ˮ�е�HCl��ʹ��ӦCl2+H2O
2HCl+O2 �� CaCO3 ������ˮ�е�HCl��ʹ��ӦCl2+H2O![]() HCl+HClO�Ļ�ѧƽ�������ƶ���HClOŨ������ Ca(HCO3)2 Բ����ƿ �����ƶ�����B������B��Һ����ˮ���е�Һ����ƽ 0.05 mol��L-1
HCl+HClO�Ļ�ѧƽ�������ƶ���HClOŨ������ Ca(HCO3)2 Բ����ƿ �����ƶ�����B������B��Һ����ˮ���е�Һ����ƽ 0.05 mol��L-1
����������1����������ˮ����ˮ��ӦCl2+H2O![]() HCl+HClO������HClO����Ư���ԣ���ʹʪ��ĺ�ɫ������ɫ����ʹ����ɫ�����Ļ�ѧʽ��HClO����2������ˮ����һ��ʱ�����Һ��ɫ��dz������ΪHClO���ȶ�������ֽ�����HCl��O2��HClOŨ�Ƚ��ͣ�ƽ��Cl2+H2O
HCl+HClO������HClO����Ư���ԣ���ʹʪ��ĺ�ɫ������ɫ����ʹ����ɫ�����Ļ�ѧʽ��HClO����2������ˮ����һ��ʱ�����Һ��ɫ��dz������ΪHClO���ȶ�������ֽ�����HCl��O2��HClOŨ�Ƚ��ͣ�ƽ��Cl2+H2O![]() HCl+HClO�����ƶ����������ģ���Һ��ɫ��dz���йط�Ӧ�Ļ�ѧ����ʽΪ��Cl2+H2O
HCl+HClO�����ƶ����������ģ���Һ��ɫ��dz���йط�Ӧ�Ļ�ѧ����ʽΪ��Cl2+H2O![]() HCl+HClO��2HClO
HCl+HClO��2HClO![]() 2HCl+O2������3����CaCO3������ˮ�е�HCl��ʹ��ӦCl2+H2O
2HCl+O2������3����CaCO3������ˮ�е�HCl��ʹ��ӦCl2+H2O![]() HCl+HClO�Ļ�ѧƽ�������ƶ���HClOŨ������Ӧ����������Ϊ������̼��������̼��Ʒ�Ӧ���ã�����������̼����ˮ�����ԣ������˴�����ĵ��룬ʹ��Һ�д�����Ũ�ȸ��ߵĴ����ᣬ�����Һ������ɫ�����ϣ����������ˮ��Ư���Ը�ǿ����������ˮ��ӦCl2+H2O
HCl+HClO�Ļ�ѧƽ�������ƶ���HClOŨ������Ӧ����������Ϊ������̼��������̼��Ʒ�Ӧ���ã�����������̼����ˮ�����ԣ������˴�����ĵ��룬ʹ��Һ�д�����Ũ�ȸ��ߵĴ����ᣬ�����Һ������ɫ�����ϣ����������ˮ��Ư���Ը�ǿ����������ˮ��ӦCl2+H2O![]() HCl+HClO�����ɣ���Ϊ̼����ǹ����ģ����ҷ�Ӧ���ж�����̼���ɣ����̼��ƺͶ�����̼��ˮ��Ӧ�����˿�����ˮ��̼�����CaCO3+CO2+H2O=Ca(HCO3)2����˵ڶ�����ϡ������Ca(HCO3)2+2HCl=CaCl2+2CO2��+2H2O�����Բ���������Һ�е����ʳ�CaCl2��HClO�⣬����Ca(HCO3)2��������A������ΪԲ����ƿ����ȷ��������B�����������ʵ�����������������a���ȴ�����A��ȴ��������b�������ƶ�����B������B��Һ����ˮ���е�Һ����ƽ��c��ƽ����̶������е�Һ���������ʵ������и��ݷ�ӦCl2+H2O
HCl+HClO�����ɣ���Ϊ̼����ǹ����ģ����ҷ�Ӧ���ж�����̼���ɣ����̼��ƺͶ�����̼��ˮ��Ӧ�����˿�����ˮ��̼�����CaCO3+CO2+H2O=Ca(HCO3)2����˵ڶ�����ϡ������Ca(HCO3)2+2HCl=CaCl2+2CO2��+2H2O�����Բ���������Һ�е����ʳ�CaCl2��HClO�⣬����Ca(HCO3)2��������A������ΪԲ����ƿ����ȷ��������B�����������ʵ�����������������a���ȴ�����A��ȴ��������b�������ƶ�����B������B��Һ����ˮ���е�Һ����ƽ��c��ƽ����̶������е�Һ���������ʵ������и��ݷ�ӦCl2+H2O![]() HCl+HClO��2HCl+2CaCO3=Ca(HCO3)2+ CaCl2��Ca(HCO3)2+2HCl=CaCl2+2CO2��+2H2O��֪��n(HClO)=n(HCl)=2n(CO2)=
HCl+HClO��2HCl+2CaCO3=Ca(HCO3)2+ CaCl2��Ca(HCO3)2+2HCl=CaCl2+2CO2��+2H2O��֪��n(HClO)=n(HCl)=2n(CO2)= ![]() =0.015mol��c(HClO)=
=0.015mol��c(HClO)= ![]() =0.1mol/L��
=0.1mol/L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͨ��ʯ�����Ƶ�Ư�ۣ�����Ҫ�ɷ���Ca(OH)2��3CaCl( ClO)��H2O����֪�������ο������ᷴӦ������������������õ�Ư����Ũ�����Ƶõ�Cl2�У������������������ˮ�����⣬��������
A. HC1��O2 B. CO2��HCl C. HC1 ��H2 D. CO2��H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʹ�õ���ͭ������ͭ������ԭ����ã����ҶԻ�������û����Ⱦ���ǣ�������
A.Cu�� ![]() Cu��NO3��2
Cu��NO3��2
B.Cu ![]() CuO
CuO ![]() Cu��NO3��2
Cu��NO3��2
C.Cu ![]() Cu��NO3��2
Cu��NO3��2
D.Cu ![]() CuCl2
CuCl2 ![]() Cu��NO3��2
Cu��NO3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����к�������NaCl�� Na2SO4��Na2CO3�����ʵ�NaNO3��Һ��ѡ���ʵ����Լ���ȥ���ʣ��õ�������NaNO3���壬ʵ����������ͼ��ʾ��
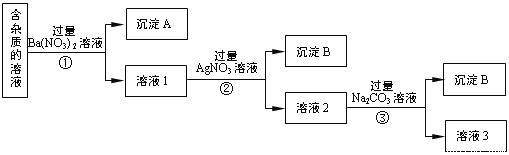
��1������A����Ҫ�ɷ���_____________��______________���ѧʽ����
��2���٢ڢ��о����еķ��������_______________��
��3����Һ3�����������Եõ�NaNO3���壬��Һ3�п϶����е�������__________��Ϊ�˳�ȥ���ʣ�������Һ3�м���������______________��
��4��ʵ��̽��С����ʵ������Ҫ�õ�456 mL1 molL-1��HNO3��Һ��������ʵ������ֻ����һƿ8 molL-1��HNO3��Һ����С����8molL-1��HNO3��Һ����������Һ��
��ʵ��������IJ�����������_________��________mL��Ͳ���ձ���__________����ͷ�ιܵȡ�
����ʵ������Ҫ��ȡ8molL-1��HNO3��Һ________mL��
������ʵ������е������Ƶ���ҺŨ��ƫ�ߵ���_____________��
A.ȡ8molL-1��HNO3��Һ��Һʱ���ӿ̶���
B.��ȡ�õ���Ͳˮϴ��δ�����κβ���
C. 8molL-1��HNO3��Һ����Ͳת�����ձ�����ˮϴ����Ͳ��ȫ��ת�����ձ�
D.����ʱ���ӿ̶���
E.���ݺ�����ƿ��ҡ�Ⱥ���Һ����ڿ̶��ߣ�δ�����κβ���
��5��ijͬѧת����Һ�IJ�����ͼ��ʾ����ͬѧ�����еĴ�����______________________________________������ƿ�Ŀ̶��߱��ڱȽ�ϸ��ƿ��֮�ϵ�ԭ����___________��
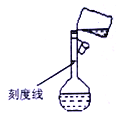
A.Ϊ������ B.Ϊ��ͳһ�� C.Ϊ�����ȷ�� D.����̻�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���2L���ܱ������У�X,Y,Z������������ʵ�����ʱ��仯��������ͼ��ʾ������������ȷ���ǣ� �� 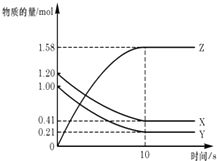
A.��Ӧ��ʼ��10s����Z��ʾ�ķ�Ӧ����Ϊ0.158mol/��Ls��
B.��Ӧ��ʼ��10s��X�����ʵ���Ũ�ȼ�����0.79mol/L
C.��Ӧ��ʼ��10sʱ��Y��ת����Ϊ79.0%
D.��Ӧ�Ļ�ѧ����ʽΪ��X��g��+Y��g��Z��g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�ֳ����ķ�ɢϵ���ش��������⣮
������е�����ˮ����μ�����Һ����������� ��
ֹͣ���ȣ����Ƶ�Fe��OH��3���壬��ȡFe��OH��3���廯ѧ��Ӧ����ʽΪ ��
����Fe��OH��3�����м���Na2SO4������Һ���������ӣ������ӷ��ţ������ã�ʹ�����γ��˳�����������̽��� ��
�����ֽ������Һ���õķ������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������[��NH4��2Fe��SO4��2]��һ����Ҫ�Ļ���ԭ�ϣ������й�˵����ȷ���ǣ�������
A.Na+��Fe3+��NO3����Cl2�����ڸ����ʵ���Һ�д�������
B.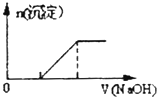
��O.1mo1��L��1�����ʵ���Һ�����0��Lmol��1NaOH��Һ�����ɳ��������ʵ�������μ���NaOH��Һ�����ϵ��ͼ��ʾ
C.�����������Fe2+�Ƿ���ʵķ�����������ʵ���Һ�е��뼸��KSCN��Һ���۲���Һ�Ƿ���ɫ
D.������ʵ���Һ��ժ��Ba��OH��2��Һ��ǡ��ʹSO42����ȫ���������ӷ���ʽΪ��Fe2++2SO42��+3Ba2++2OH���T2BaSO4��+Fe��OH��2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25��ʱ���ܱ�������X��Y��Z��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����±���
���� | X | Y | Z |
��ʼŨ��/molL��1 | 0.1 | 0.2 | 0 |
ƽ��Ũ��/molL��1 | 0.05 | 0.05 | 0.1 |
����˵��������ǣ�������
A.��Ӧ�ﵽƽ��ʱ��X��ת����Ϊ50%
B.��Ӧ�ɱ�ʾΪX+3Y2Z����ƽ�ⳣ��Ϊ1600
C.����ѹǿʹƽ��������Z�ķ����ƶ���ƽ�ⳣ������
D.�ı��¶ȿ��Ըı�˷�Ӧ��ƽ�ⳣ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӧ����㷺�Ľ����������Ȼ���������Լ������ĺ������ξ�Ϊ��Ҫ�����
(1)��д��Fe��ˮ������Ӧ�Ļ�ѧ����ʽ:_____________��
(2)��ʵ�����У�FeCl2�������ۺ�______(������)��Ӧ�Ʊ���
(3)Fe3O4���ö��ַ����Ƶã�������һ�ֵ��ʺ�һ�ֻ�����ͨ�����Ϸ�Ӧ�Ʊ��Ļ�ѧ����ʽΪ______��
(4)��ש������������ս���ɵģ����京��Fe2O3�ʺ�ɫ���غ�ɫ���������������������ϡ������һ����ʵ��֤����ש�к���Fe3+:_________________��
(5)����һ����FeCl2 ��FeCl3�Ļ������Ʒ��ʵ����n(Fe)��n(C1)=1��2.1�������Ʒ��FeCl3�����ʵ�������Ϊ_________��
(6)�������(K2FeO4)��һ��ǿ������������Ϊˮ��������������ز��ϡ�FeCl3��KClO��ǿ���������·�Ӧ����ȡK2FeO4���䷴Ӧ�����ӷ���ʽΪ:____________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com