
【题目】铁是应用最广泛的金属,铁的氯化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)请写出Fe与水蒸气反应的化学方程式:_____________。
(2)在实验室中,FeCl2可用铁粉和______(填名称)反应制备。
(3)Fe3O4可用多种方法制得,其中由一种单质和一种化合物通过化合反应制备的化学方程式为______。
(4)红砖是用黏土高温烧结而成的,因其含有Fe2O3呈红色或棕红色而得名,常用作建筑材料。请设计一个简单实验证明红砖中含有Fe3+:_________________。
(5)现有一含有FeCl2 和FeCl3的混合物样品,实验测得n(Fe):n(C1)=1:2.1,则该样品中FeCl3的物质的量分数为_________。
(6)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:____________。
【答案】 3Fe+4H2O(g) ![]() Fe3O4+4H2 稀盐酸或氯化铁溶液 6FeO + O2
Fe3O4+4H2 稀盐酸或氯化铁溶液 6FeO + O2![]() 2Fe3O4(或 4Fe2O3 + Fe
2Fe3O4(或 4Fe2O3 + Fe![]() 3Fe3O4) 将样品粉碎,用盐酸浸泡后取上层清液,滴加 KSCN 溶液后显红色 10% 2Fe3+ + 3ClO- + 10OH- = FeO42- + 3Cl- + 5H2O
3Fe3O4) 将样品粉碎,用盐酸浸泡后取上层清液,滴加 KSCN 溶液后显红色 10% 2Fe3+ + 3ClO- + 10OH- = FeO42- + 3Cl- + 5H2O
【解析】(1)Fe与水蒸气在加热条件下反应生成氢气和四氧化三铁,反应的化学方程式为3Fe+4H2O(g)![]() Fe3O4+4H2。(2)在实验室中,FeCl2可用铁粉和稀盐酸或氯化铁溶液反应制备。(3)由一种单质和一种化合物通过化合反应制备,根据原子守恒以及铁元素化合价可知应该是氧化亚铁与氧气或氧化铁与铁单质,反应的化学方程式为6FeO+O2
Fe3O4+4H2。(2)在实验室中,FeCl2可用铁粉和稀盐酸或氯化铁溶液反应制备。(3)由一种单质和一种化合物通过化合反应制备,根据原子守恒以及铁元素化合价可知应该是氧化亚铁与氧气或氧化铁与铁单质,反应的化学方程式为6FeO+O2![]() 2Fe3O4或4Fe2O3+ e
2Fe3O4或4Fe2O3+ e![]() 3Fe3O4。(4)在溶液中可以用KSCN溶液检验铁离子,所以首先要溶解红砖,则实验证明红砖中含有Fe3+的实验方案是将样品粉碎,用盐酸浸泡后取上层清液,滴加KSCN溶液后显红色。(5)设FeCl2和FeCl3的物质的量分别是xmol、ymol,则根据原子守恒可知
3Fe3O4。(4)在溶液中可以用KSCN溶液检验铁离子,所以首先要溶解红砖,则实验证明红砖中含有Fe3+的实验方案是将样品粉碎,用盐酸浸泡后取上层清液,滴加KSCN溶液后显红色。(5)设FeCl2和FeCl3的物质的量分别是xmol、ymol,则根据原子守恒可知![]() ,解得x=9y,所以该样品中FeCl3的物质的量分数为
,解得x=9y,所以该样品中FeCl3的物质的量分数为![]() 。(6)次氯酸钾中氯+1价具有强氧化性,可将+3价的铁氧化成+6价,用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为2Fe3++3ClO-+10OH-=FeO42-+3Cl-+5H2O。
。(6)次氯酸钾中氯+1价具有强氧化性,可将+3价的铁氧化成+6价,用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为2Fe3++3ClO-+10OH-=FeO42-+3Cl-+5H2O。


 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源: 题型:
【题目】新制的饱和氯水中含有多种做粒,某校化学研究性学习小组的同学为探究其性质,做了如下实验,请你帮助完成。
(1)氯气能使湿润的红色布条褪色,使其褪色的微粒的化学式是__________。
(2)将氯水光照一段时间后,溶液颜色逐渐变浅,有关反应的化学方程式为__________、__________。
(3)新制的饱和氯水与碳酸钙的反应是制取较浓HClO 溶液 的 方 法 之一。
实验一 定性研究:

Ⅰ.如图所示,在试管中加入过量的块状碳酸钙,再加入约20 mL新制的饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去。
Ⅱ.过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强。
Ⅲ.为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体,
将第三份加热,观察到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
①反应后所得的溶液漂白性增强的原因是__________________________________________________。
②依据上述实验可推知:步骤Ⅱ的滤液中的溶质除CaCl2、HClO外,还有__________。
实验二 定量研究:
在仪器A内,放有塑料网包住的块状碳酸钙(过量)和150 mL新制的饱和氯水,按如图所示装置实验(实验前仪器B中充满了饱和NaHCO3溶液),待不再产生气泡后,将塑料网中剩余的碳酸钙提出液面,密封后再加热烧瓶中的液体,直到仪器B中的气体不再增加(不考虑HClO的分解)。

③仪器A的名称为__________。
④准确读出仪器B中气体体积的实验操作步骤依次是:a.等待仪器A冷却到室温;b.____________;c. 平视与刻度线相切的液面读数。
⑤实验结束后,测得仪器B中收集到的气体体积在标准状况下为168mL,则150mL 新制的饱和氯水与过量碳酸钙完全反应后,所得溶液中HClO的物质的量浓度为__________。(反应前后,溶液体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A. 0.1mol氯气通入水中,转移电子的数目为0.1NA
B. 常温常压下,7.8g过氧化钠含有阴离子的数目为0.2NA
C. 标准状况下,22.4LCl2与足量的铁充分反应,转移电子数为3NA
D. 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】混合动力汽车(HEV)中使用了镍氢电池,其工作原理如图所示: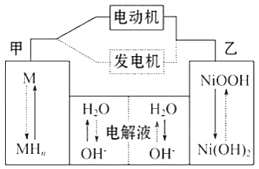
其中M为储氢合金,MH为吸附了氢原子的储氢合金,KOH溶液作电解液.关于镍氢电池,下列说法不正确的是( )
A.充电时,阴极附近pH降低
B.电动机工作时溶液中OH﹣向甲移动
C.放电时正极反应式为:NiOOH+H2O+e﹣═Ni(OH)2+OH﹣
D.电极总反应式为:M+Ni(OH)2 ![]() MH+NiOOH
MH+NiOOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】饮用水中含有砷会导致砷中毒,水体中溶解的砷主要以As(Ⅲ)亚砷酸盐和As(Ⅴ)砷酸盐形式存在.
(1)砷与磷为同一主族元素,磷的原子结构示意图为 .
(2)根据元素周期律,下列说法正确的是 .
a.酸性:H2SO4>H3PO4>H3AsO4
b.原子半径:S>P>As
c.非金属性:S>P>As
(3)关于地下水中砷的来源有多种假设,其中一种认为是富含砷的黄铁矿(FeS2)被氧化为Fe(OH)3 , 同时生成SO42﹣ , 导致砷脱离矿体进入地下水.FeS2被O2氧化的离子方程式为 .
(4)去除水体中的砷,可先将As(Ⅲ)转化为As(Ⅴ),选用NaClO可实现该转化.研究NaClO投加量对As(Ⅲ)氧化率的影响得到如下结果: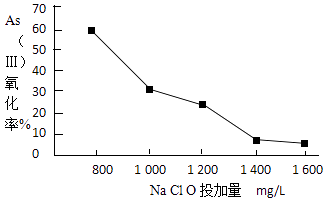
已知:投料前水样pH=5.81,0.1mol/LNaClO溶液pH=10.5,溶液中起氧化作用的物质是次氯酸.产生此结果的原因是 .
(5)强阴离子交换柱可以吸附以阴离子形态存在的As(Ⅴ)达到去除As的目的.
已知:一定条件下,As(Ⅴ)的存在形式如表所示:
pH | <2 | 2~7 | 7~11 | 11~14 |
存在形式 | H3AsO4 | H2AsO3﹣ | HAsO42﹣ | HAsO42﹣、AsO43﹣ |
pH=6时,NaClO氧化亚砷酸(H3AsO3)的离子方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PCl5(g)一定条件下可以转化成PCl3(g)或红磷P(s).
(1)已知: PCl5(g)═PCl3(g)+Cl2(g)△H1K1
PCl3(g)═P(s)+ ![]() Cl2(g)△H2K2
Cl2(g)△H2K2
K1、K2表示该反应的平衡常数.
则PCl5(g)═P(s)+ ![]() Cl2(g)该反应的△H=(用△H1、△H2表示),反应的平衡常数K=(用K1、K2表示).
Cl2(g)该反应的△H=(用△H1、△H2表示),反应的平衡常数K=(用K1、K2表示).
(2)在210℃时,将4mol PCl3气体充入1L真空恒容密闭容器中发生反应:2PCl3(g)═2P(s)+3Cl2(g) 测得数据如下表:
时间/min | 0 | 10 | 20 | 30 | 40 |
n(PCl3)/mol | 4 | 2.8 | 2 | 1 | 1 |
并测得反应达到平衡时热量变化数值为Q,反应平衡常数为K,PCl3转化率为α.
①0~30min时,用Cl2表示该反应的反应速率为;平衡时,PCl3转化率α=;该温度下反应的平衡常数K= .
②其它条件保持不变,若上述反应在恒压条件下进行反应,达平衡时测得热量变化数值、平衡常数、PCl3转化率分别为Q′、K′、α′,则Q′(填“>”“<”或“=”,下同)Q,K′K,α′α.
③保持其它条件不变,若向上述平衡体系中再充入1molCl2(g)、1molP(s)和1molPCl3(g),则上述平衡反应(填“正向”、“逆向”或“不”)移动.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁烷催化裂化,其碳链按两种方式断裂,生成两种烷烃和两种烯烃。若丁烷的裂化率为90%,且裂化后两种烯烃的质量相等,则裂化后得到的相对分子质量最小的气态烃在混合烃中的体积分数为 ( )
A. 11% B. 19% C. 40% D. 50%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com