
【题目】下列说法正确的是( )
A.凡是放热反应都是自发的,凡是吸热反应都是非自发的
B.自发反应一定是放热反应,非自发反应一定是吸热反应
C.自发反应在恰当条件下才能实现
D.自发反应在任何条件下都能实现
科目:高中化学 来源: 题型:
【题目】为了得到比较纯净的物质,使用的方法恰当的是
A.向Na2CO3饱和溶液中,通入过量的CO2后,在加热的条件下,蒸发得NaHCO3晶体
B.向FeCl3溶液里加入足量NaOH溶液,经过滤、洗涤沉淀,再充分灼烧沉淀得Fe2O3
C.向FeBr2溶液中加入过量的氯水,加热蒸发得FeCl3晶体
D.加热蒸发AlCl3饱和溶液得纯净的AlCl3晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定实验是化学学科中重要的定量实验。请回答下列问题:
Ⅰ.酸碱中和滴定——已知某NaOH试样中含有NaCl杂质,为测定试样中NaOH的质量分数,进行如下实验:
①称量1.00 g样品溶于水,配成250 mL溶液;
②准确量取25.00 mL所配溶液于锥形瓶中;
③滴加几滴酚酞溶液;
④用0.10 mol/L的盐酸标准液滴定三次,每次消耗盐酸的体积记录如下:
滴定序号 | 待测液体积mL | 所消耗盐酸标准液的体积/mL | |
滴定前读数 | 滴定后读数 | ||
1 | 25.00 | 0.50 | 20.60 |
2 | 25.00 | 6.00 | 26.00 |
3 | 25.00 | 1.10 | 21.00 |
(1)用__________滴定管(填“酸式”或“碱式”)盛装0.10 mol/L的盐酸标准液
(2)试样中NaOH的质量分数为__________
(3)若出现下列情况,测定结果偏高的是________
A.滴定前用蒸馏水冲洗锥形瓶
B.在振荡锥形瓶时不慎将瓶内溶液溅出
C.若在滴定过程中不慎将数滴酸液滴在锥形瓶外
D.酸式滴定管滴至终点时,俯视读数
E.酸式滴定管用蒸馏水洗后,未用标准液润洗
Ⅱ.氧化还原滴定
(4)取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1 mol·L-1的高锰酸钾溶液滴定,发生的反应为2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O滴定时,KMnO4溶液应装在酸式滴定管中,滴定终点时现象是__________
(5)用0.01 mol/L的I2标准溶液滴定未知浓度的Na2S2O3溶液,选用的指示剂是__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的表述正确的是
A.离子结构示意图:![]() 可以表示16O2-,也可以表示18O2-
可以表示16O2-,也可以表示18O2-
B.比例模型:![]() 可以表示甲烷分子,也可以表示四氯化碳分子
可以表示甲烷分子,也可以表示四氯化碳分子
C.氯化铵的电子式为:![]()
D.二氧化碳分子的比例模型是: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组,为研究金属的腐蚀和防护的原理,做了以下实验:将剪下的一块镀锌铁片,放入锥形瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞试液,按如图所示的装置进行实验,过一段时间后观察。下列现象不可能出现的是
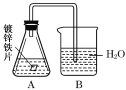
A.锌被腐蚀B.金属片剪口变红
C.B中导气管里形成一段水柱D.B中导气管产生气泡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N—N键的键能为160kJ·mol-1(N2的键能为942kJ·mol-1),晶体片段结构如右图所示。又发现利用N2可制取出N5、N3。含N5+离子的化合物及N60、N5极不稳定。则下列说法错误的是( )
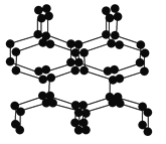
A. 按键型分类,该晶体中含有非极性共价键
B. 含N5+离子的化合物中既有离子键又有共价键
C. 高聚氮与N2、N3、N5、N5+、N60互为同素异形体
D. 这种固体的可能潜在应用是烈性炸药或高能材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机材料PMMA、新型可降解高分子材料PET、常见解热镇痛药Aspirin的合成路线如下:
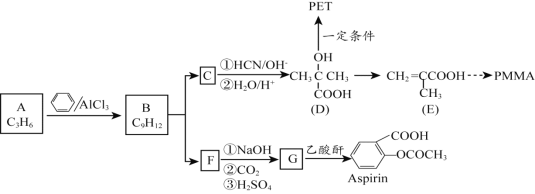
已知:![]()
![]()
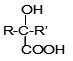
(1)A属于烯烃,其结构简式是_______。
(2)A与苯在AlCl3催化作用下反应生成B的反应类型是_______。
(3)写出B的一溴代物只有2种的芳香烃的名称__________写出生成这两种一溴代物所需要的反应试剂和反应条件____________
(4)B在硫酸催化条件下被氧气氧化可得有机物C与F。
①C由碳、氢、氧三种元素组成, C的结构简式是_________。
②向少量F溶液中滴加几滴FeCl3溶液,溶液呈紫色,且F在其同系物中相对分子质量最小。G物质中含氧官能团名称为_______。
(5)D在一定条件下制取PET的化学方程式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟氨(NH2OH)是一种还原剂,和联氨一样是一种弱碱,不稳定,室温下吸收水汽迅速分解。回答下列问题:
(1)请写出羟氨的电子式___。
(2)利用KMnO4标准溶液定量间接测定羟氨的纯度。测定步骤如下:
①溶液配制:称取5.0g某羟氨样品,溶解在______酸中后加适量蒸馏水,将其全部转移至100mL的______中,加蒸馏水至_______。
②取20.00mL的羟氨酸性溶液与足量硫酸铁在煮沸条件下反应:2NH2OH2++4Fe3+=N2O↑+4Fe2++H2O+6H+,生成的Fe2+用0.4000 mol·L-1的酸性KMnO4溶液滴定,滴定达到终点的现象是____________。请写出Fe2+与酸性KMnO4溶液反应的离子方程式_____________。重复滴定3次,每次消耗酸性高锰酸钾标准溶液的体积如表所示:
![]()
计算试样的纯度____%。
(3)下列操作导致误差偏高的有______(填编号)。
a 滴定前滴定管尖嘴处有气泡,滴定后消失
b 滴定管未经润洗盛装KMnO4溶液
c 羟氨称量时,时间过长和溶解时没有及时用酸酸化
d KMnO4溶液起始读数仰视,终点正常读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾(KMnO4)和双氧水(H2O2)都是常见物质。
(1)写出二者共同元素的原子最外层轨道表示式:___________K在周期表的位置是 ___________ ;25Mn属于_____________族元素。
(2)双氧水(H2O2)和水都是极弱电解质,但H2O2比H2O更显酸性。若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:_____________
(3)2g高锰酸钾溶于10ml水时溶液没有明显的温度变化,请解释理由__________________________________,氧化剂一般来说,酸性越强其氧化性也越强,因此常用酸化的高锰酸钾作氧化剂。用高锰酸钾法测定H2O2时,不能用HCl来酸化原因是_________________;
(4)往H2O2水溶液中滴入一滴酸性KMnO4溶液,从溶液内部析出大量无色气泡。写出可能的化学反应方程式。_____________________________________
(5)往H2O2水溶液中滴入酸性KMnO4溶液,下列方程式错误的是__________
A 3H2O2+2KMnO4+3H2SO4→K2SO4+2MnSO4+6H2O+4O2↑
B 5H2O2+2KMnO4+3H2SO4→K2SO4+2MnSO4+8H2O+5O2↑
C 7H2O2+2KMnO4+3H2SO4→K2SO4+2MnSO4+10H2O+6O2↑
D 9H2O2+2KMnO4+3H2SO4→K2SO4+2MnSO4+12H2O+7O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com