
����Ŀ��������أ�KMnO4����˫��ˮ��H2O2�����dz������ʡ�
(1)д�����߹�ͬԪ�ص�ԭ�����������ʾʽ��___________K�����ڱ���λ���� ___________ ;25Mn����_____________��Ԫ�ء�
(2)˫��ˮ��H2O2����ˮ���Ǽ�������ʣ���H2O2��H2O�������ԡ�����H2O2�����Ƕ�Ԫ���ᣬ��д������ˮ�еĵ��뷽��ʽ��_____________
(3)2g�����������10mlˮʱ��Һû�����Ե��¶ȱ仯�����������__________________________________,������һ����˵������Խǿ��������ҲԽǿ����˳����ữ�ĸ�����������������ø�����ط��ⶨH2O2ʱ��������HCl���ữԭ����_________________;
(4)��H2O2ˮ��Һ�е���һ������KMnO4��Һ������Һ�ڲ�����������ɫ���ݡ�д�����ܵĻ�ѧ��Ӧ����ʽ��_____________________________________
(5)��H2O2ˮ��Һ�е�������KMnO4��Һ�����з���ʽ�������__________
A 3H2O2��2KMnO4��3H2SO4��K2SO4��2MnSO4��6H2O��4O2��
B 5H2O2��2KMnO4��3H2SO4��K2SO4��2MnSO4��8H2O��5O2��
C 7H2O2��2KMnO4��3H2SO4��K2SO4��2MnSO4��10H2O��6O2��
D 9H2O2��2KMnO4��3H2SO4��K2SO4��2MnSO4��12H2O��7O2��
���𰸡�![]() �������ڢ�A ��B���� H2O2
�������ڢ�A ��B���� H2O2 ![]() H+ + HO2-�� HO2-
H+ + HO2-�� HO2- ![]() H+ + O22- �����������ˮʱ��ɢ�������յ�������ˮ�Ϲ��̷ų���������� ��HCl���л�ԭ�� 5H2O2��2KMnO4��3H2SO4 �� K2SO4��2MnSO4��8H2O��5O2����2 H2O2
H+ + O22- �����������ˮʱ��ɢ�������յ�������ˮ�Ϲ��̷ų���������� ��HCl���л�ԭ�� 5H2O2��2KMnO4��3H2SO4 �� K2SO4��2MnSO4��8H2O��5O2����2 H2O2 ![]() 2H2O + O2�� A
2H2O + O2�� A
��������
(1)���߹�ͬԪ��Ϊ��Ԫ�أ�Oԭ�����������ʾʽΪ��![]() ��K�ڵ��ĸ����ڣ������һ�����ӣ����������ڱ��е�λ���ǵ�������IA�壻25Mn����VIIB��Ԫ�أ��ʴ�Ϊ��
��K�ڵ��ĸ����ڣ������һ�����ӣ����������ڱ��е�λ���ǵ�������IA�壻25Mn����VIIB��Ԫ�أ��ʴ�Ϊ��![]() ����������IA�壻VIIB���壻
����������IA�壻VIIB���壻
(2)��Ԫ����ֲ����룬�Ե�һ��Ϊ�������Ե��뷽��ʽΪ��H2O2![]() H+ + HO2-��HO2-
H+ + HO2-��HO2-![]() H++O22-������H2O2
H++O22-������H2O2![]() H+ + HO2-��HO2-
H+ + HO2-��HO2-![]() H++O22-��
H++O22-��
(3)û�����Ե��¶ȱ仯��˵�������������ˮ��ɢ�������յ�������ˮ�Ϲ��̷ų��������������ȣ��������ǿ�����ԣ�HCl���л�ԭ�ԣ��ᷢ��������ԭ����Ϊ�������������ˮʱ��ɢ�������յ�������ˮ�Ϲ��̷ų��������������HCl���л�ԭ�ԣ�
(4)��H2O2ˮ��Һ�е���һ������KMnO4��Һ������Һ�ڲ�����������ɫ���ݣ�˵���������������������߷�Ӧ���������߹������������ֽ��������������ʽΪ��5H2O2��2KMnO4��3H2SO4=K2SO4��2MnSO4��8H2O��5O2����2 H2O2 ![]() 2H2O + O2����
2H2O + O2����
(5)���ݵ�ʧ�����غ��ԭ���غ��жϣ�A����


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д� �������ϵ�д�
�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.���Ƿ��ȷ�Ӧ�����Է��ģ��������ȷ�Ӧ���Ƿ��Է���
B.�Է���Ӧһ���Ƿ��ȷ�Ӧ�����Է���Ӧһ�������ȷ�Ӧ
C.�Է���Ӧ��ǡ�������²���ʵ��
D.�Է���Ӧ���κ������¶���ʵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���¼��t��ʱ��4����ͬ������ͭ��Һ�м�����ˮ����ͭ�������Լ����������� ͭ����(CuSO4��5H2O)������(�¶ȱ��ֲ���)��ʵ����駣�
����ͭ��Һ | �� | �� | �� | �� |
�������ˮ����ͭ(g) | 3.00 | 5.50 | 8.50 | 10.00 |
����������ͭ����(g) | 1.00 | 5.50 | 10.90 | 13.60 |
������6.20g��ˮ����ͭʱ����������ͭ���������(g)Ϊ
A.7.70B.6.76C.5.85D.9.00
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ȳ����ż����Ӧ�ڿ������ͷ�����ϡ������ӵ���������Ҫ�о���ֵ����Ȳ������ż����ӦΪ 2CH��CH ![]() CH��CC��CH+H2����Ȳż����Ӧ�����������仯��ͼ�������ߢ���ʾ�����ߢ�Ϊ�ı�ijһ�����������仯������˵������ȷ���ǣ� ��
CH��CC��CH+H2����Ȳż����Ӧ�����������仯��ͼ�������ߢ���ʾ�����ߢ�Ϊ�ı�ijһ�����������仯������˵������ȷ���ǣ� ��
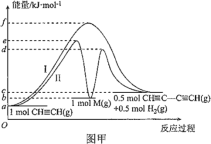
A.���ߢ�Ӧ����ܼ��ܴ�����������ܼ���
B.���ߢ�ı�������Ǽ����˴���
C.���ߢ��Ӧ�����£���һ����Ӧ�� ��H=+(b-a)kJ��mol-1
D.���ߢ��Ӧ�����£������ܷ�Ӧ���ʵĴ�С�ǵڶ�����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ũ����ͬ��NaOH��Һ��100mL����A��B��C�����ձ��У��ֱ���������Һ��ͨ�벻������CO2����ַ�Ӧ����������������Һ����μ���0.2mol/L�����ᣬ����CO2������������������֮���ϵ��ͼ��ʾ�������ж���ȷ���ǣ� ��
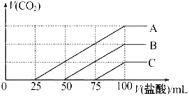
A.ԭNaOH��Һ��Ũ��Ϊ0.2mol/L
B.B�ձ���ͨ���CO2���Ϊ448mL
C.ͨ��CO2����ȷ��A�ձ��е�����
D.ͨ��CO2��C�ձ������ʳɷֵ����ʵ���֮��Ϊn(NaOH)��n(Na2CO3)��2��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȡ10g�����ʵ�Na2CO3��Ʒ�����ʲ����뷴Ӧ��������100 mL(���ܶ�Ϊ1.0g��mL-1)ϡ���ᣬ��ַ�Ӧ���ձ���ʣ�����ʵ�������Ϊ106.48g�����ɵ�����ȫ���ݳ�����̼������Ʒ�Ĵ���Ϊ _______________________��������Ӧ�����Һ��ˮϡ�͵�400mL�������Һ��pHΪ1����ԭϡ��������ʵ���Ũ��Ϊ _________________ mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ������з�����ӦN2+3H2![]() 2NH3����H��0���ﵽƽ���ֻ�ı�ijһ������ʱ����Ӧ�����뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ,�ش��������⣺
2NH3����H��0���ﵽƽ���ֻ�ı�ijһ������ʱ����Ӧ�����뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ,�ش��������⣺
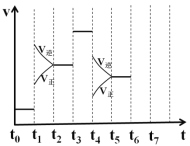
(1)����ƽ��״̬��ʱ�����______����ѡ���
A��t0��t1������B��t1��t2������C��t2��t3
D��t3��t4 E��t4��t5���� F��t5��t6
(2)t1��t3��t4ʱ�̷ֱ�ı��һ�������ǣ���ѡ���
A������ѹǿ B����Сѹǿ C�������¶�
D�������¶� E���Ӵ��� F���뵪��
t1ʱ��__________��t4ʱ��__________��
(3)����(2)�еĽ��ۣ�����ʱ����У����İٷֺ�����ߵ���________����ѡ���
A��t0��t1 B��t2��t3 C��t3��t4 D��t5��t6
(4)�����t6ʱ�̣��ӷ�Ӧ��ϵ�з�������ְ���t7ʱ�̷�Ӧ�ﵽƽ��״̬������ͼ�л�����Ӧ���ʵı仯����_________��
(5)һ�������£��ϳɰ���Ӧ�ﵽƽ��ʱ����û�������а������������Ϊ20%����Ӧ���뷴Ӧǰ�Ļ���������֮��Ϊ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1mol��L-1HCl��Һ�ζ�0.1mol��L-1 NH3��H2O��Һ���ζ�������ͼa��ʾ�������Һ��pH������Ũ�ȱ仯�Ĺ�ϵ��ͼb��ʾ������˵������ȷ����
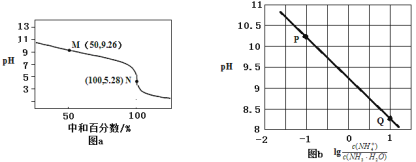
A.Kb(NH3��H2O)��������Ϊ10-5
B.P��Q�����У�ˮ�ĵ���̶�������
C.���ζ�����Һ������ʱ��c(NH4+)��c(NH3��H2O)
D.N�㣬c(Cl- ) - c(NH4+)=![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й��о���Ա���Ƴ�һ�������Ϲ����������̫�����ڴ�������ʵ�ָ�Ч�ֽ�ˮ������Ҫ��������ͼ��ʾ��

��֪�����������л�ѧ���ļ������±���ʾ��
��ѧ�� | H2O��H��O�� | O2��O��O �� | H2��H��H�� | H2O2��O��O�� | H2O2��O��H�� |
����kJ/mol | 463 | 496 | 436 | 138 | 463 |
����Ӧ�����зֽ���2 molˮ��������˵������ȷ����
A. �ܷ�ӦΪ2H2O![]() 2H2��+O2��
2H2��+O2��
B. ����I������926 kJ����
C. ����II�ų���574 kJ����
D. ���̢����ڷ��ȷ�Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com