
| c(H+)?c(CH3COO-) |
| c(CH3COOH) |
| c(H+)?c(CH3COO-) |
| c(CH3COOH) |
| (0.1mol/L×1.3%)2 |
| 0.1molL×(1-1.3%) |
| c(CH3COOH) |
| c(CH3COONa) |
| 0.1 |
| c(CH3COONa) |


科目:高中化学 来源: 题型:
 洋蓟在国际市场上属高档蔬菜,以良好的保健功能和药用价值被冠以“蔬之皇”的美称,从洋蓟提取的洋蓟素结构如图,请回答下列问题
洋蓟在国际市场上属高档蔬菜,以良好的保健功能和药用价值被冠以“蔬之皇”的美称,从洋蓟提取的洋蓟素结构如图,请回答下列问题 +A
+A| 催化剂 |
| 一定条件 |

查看答案和解析>>
科目:高中化学 来源: 题型:
 元素周期表揭示了化学元素间的内在联系,使其构成了一个完整的体系.
元素周期表揭示了化学元素间的内在联系,使其构成了一个完整的体系.查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D、E、F均为周期表中前四周期的元素.请按要求回答下列问题.
A、B、C、D、E、F均为周期表中前四周期的元素.请按要求回答下列问题.| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
| 1 |
| 4 |
| 3 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

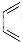 +
+ →G(抗病毒药阿昔洛韦中间体),G的结构简式为:
→G(抗病毒药阿昔洛韦中间体),G的结构简式为:查看答案和解析>>
科目:高中化学 来源: 题型:
 )是一种重要的工业原料,某研究性学习小组的同学拟用下列装置制取高纯度的苯甲酸甲酯.
)是一种重要的工业原料,某研究性学习小组的同学拟用下列装置制取高纯度的苯甲酸甲酯.
| 熔点/℃ | 沸点/℃ | 密度/g?cm-3 | 水溶性 | |
| 苯甲酸 | 122.4 | 249 | 1.27 | 微溶 |
| 甲醇 | -97 | 64.3 | 0.79 | 互溶 |
| 苯甲酸甲酯 | -12.3 | 199.6 | 1.09 | 不溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com