
【题目】Ⅰ氢、碳、氮都是重要的非金属元素,它们的单质及其化合物在科学研究和工业生产中有重要的应用。
(1)下列微粒基态的电子排布中未成对电子数最多的是__(填序号)
a.N3- b.Fe3+ c.Cu d.Cr e.C
(2)第一电离能介于B、N之间的第二周期元素有_____种。
(3)已知HCO3-在水溶液中可通过氢键成为二聚体(八元环结构),试画出该二聚体的结构式:____________________________。
(4)[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2-+4H++4H2O![]() [Zn(H2O)4]2++4HOCH2CN
[Zn(H2O)4]2++4HOCH2CN
①Zn2+基态核外电子排布式为____。1 mol HCHO分子中含有σ键的物质的量为____mol。
②HOCH2CN分子中碳原子轨道的杂化类型是__。与H2O分子互为等电子体的阴离子为__。
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为______。
Ⅱ.由原子序数由小到大的A、B、C、D、E五种元素构成某配位化合物X,其原子个数比为14∶4∶5∶1∶1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6ns1,回答下列问题。
(1)该配位化合物X的化学式为________。
(2)元素B、C、D的第一电离能由小到大排列顺序为________。(用元素符号表示)
(3)D元素原子的最外层电子轨道表示式为________。
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1∶1和1∶2,两种化合物可任意比互溶,解释其主要原因为_______________________。
(5)A元素与E元素可形成一种红色离子化合物Y,其原子个数比为1∶1,该化合物Y可与稀硝酸反应,生成一种蓝色溶液和两种无色气体(其中一种为A元素的单质),写出该反应的化学方程式_____________________________。
【答案】 d 3 ![]() 或
或![]() 1s22s22p63s23p63d10 3 sp3、sp NH2-
1s22s22p63s23p63d10 3 sp3、sp NH2- ![]() [Cu(NH3)4]SO4·H2O S<O<N
[Cu(NH3)4]SO4·H2O S<O<N ![]() H2O与H2O2之间形成氢键 6CuH+16HNO3===6Cu(NO3)2+3H2↑+4NO↑+8H2O
H2O与H2O2之间形成氢键 6CuH+16HNO3===6Cu(NO3)2+3H2↑+4NO↑+8H2O
【解析】I.(1)考查能级,a、N的最外层有5个电子,得到3个电子达到稳定结构,即N3-没有未成对电子;b、Fe价电子排布式是3d64s2,Fe3+价电子排布式为3d5,有5个未成对电子;c、Cu的价电子排布式为3d104s1,只有1个未成对电子;d、Cr的价电子排布式为3d54s1,有5个未成对电子;e、C价电子排布式为2s22p2,2个未成对电子;综上所述,未成对电子最多的是Cr,故d正确;(2)考查第一电离能的规律,同周期从左向右第一电离能增大,但IIA>IIIA,VA>VIA,符合信息的元素是Be、C、O有三种;(3)考查氢键,根据氢键的形成,八元环是![]() 或
或![]() ;(4)本题考查电子排布式、化学键类型、杂化类型、等电子体、配合物等知识,①Zn位于第四周期第IIB族,其核外电子排布式为[Ar]3d10;甲醛的结构式为
;(4)本题考查电子排布式、化学键类型、杂化类型、等电子体、配合物等知识,①Zn位于第四周期第IIB族,其核外电子排布式为[Ar]3d10;甲醛的结构式为![]() ,成键原子只能形成一个σ键,因此1mol甲醛中含有的σ键的物质的量为3mol;②有两种碳原子,以单键形成的碳原子,是sp3杂化类型,C和N之间形成叁键,此碳原子是sp杂化;等电子体是价电子总数相等,原子总数相同的微粒,因此与H2O互为等电子体的阴离子是NH2-;③根据信息,Zn2+提供空轨道,CN-中C提供孤电子对,应是
,成键原子只能形成一个σ键,因此1mol甲醛中含有的σ键的物质的量为3mol;②有两种碳原子,以单键形成的碳原子,是sp3杂化类型,C和N之间形成叁键,此碳原子是sp杂化;等电子体是价电子总数相等,原子总数相同的微粒,因此与H2O互为等电子体的阴离子是NH2-;③根据信息,Zn2+提供空轨道,CN-中C提供孤电子对,应是![]() ;II.C和D属于主族,且原子序数D为C的二倍,即D为S,C为O,根据E的外围电子排布式,推出E为Cu,根据问题(4)可以与氧形成1:1和1:2的化合物,且两种化合物任意比例互溶,因此推出A为H,B为N,(1)考查化学式的书写,根据原子个数比,推出化学式为[Cu(NH3)4]SO4·H2O ;(2)考查第一电离能的规律,非金属性越强第一电离能越大,同周期从左向右第一电离能增大,但IIA>IIIA,VA>VIA,第一电离能的大小顺序是N>O>H;(3)考查轨道式的书写,D为S,最外层有6个电子,电子排布式为3s23p4,轨道式为
;II.C和D属于主族,且原子序数D为C的二倍,即D为S,C为O,根据E的外围电子排布式,推出E为Cu,根据问题(4)可以与氧形成1:1和1:2的化合物,且两种化合物任意比例互溶,因此推出A为H,B为N,(1)考查化学式的书写,根据原子个数比,推出化学式为[Cu(NH3)4]SO4·H2O ;(2)考查第一电离能的规律,非金属性越强第一电离能越大,同周期从左向右第一电离能增大,但IIA>IIIA,VA>VIA,第一电离能的大小顺序是N>O>H;(3)考查轨道式的书写,D为S,最外层有6个电子,电子排布式为3s23p4,轨道式为![]() ;(4)考查影响溶解度的因素,形成的化合物是H2O和H2O2,H2O与H2O2之间形成分子间氢键,两者互溶;(5)考查化学方程式的书写,化合物是CuH,与硝酸反应生成蓝色溶液,即为Cu(NO3)2,两种气体为H2和NO,因此反应方程式为6CuH+16HNO3=6Cu(NO3)2+3H2↑+4NO↑+8H2O。
;(4)考查影响溶解度的因素,形成的化合物是H2O和H2O2,H2O与H2O2之间形成分子间氢键,两者互溶;(5)考查化学方程式的书写,化合物是CuH,与硝酸反应生成蓝色溶液,即为Cu(NO3)2,两种气体为H2和NO,因此反应方程式为6CuH+16HNO3=6Cu(NO3)2+3H2↑+4NO↑+8H2O。


科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为CH2=CH— CH2OH。下列关于该有机物的叙述不正确的是
A.能与金属钠发生反应并放出氢气
B.能在催化剂作用下与H2发生加成反应
C.在浓H2SO4催化下能与乙酸发生酯化反应
D.能发生银境反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进入秋冬季节后,雾霾这种环境污染问题逐渐凸显。从物质分类来看雾霾属于胶体,它区别于溶液等其它分散系的本质特征是( )
A. 胶粒可以导电 B. 胶体具有丁达尔效应
C. 胶体粒子大小在1~100nm之间 D. 胶体的分散剂为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,向容积为2L的密闭容器中充入一定量的X气体和Y气体,发生如下反应:
X(g)+2Y(g)![]() Z(g)
Z(g)
反应过程中测定的部分数据见下表:
反应时间/min | n(X)/mol | n(Y)/ mol |
0 | 2.00 | 2.40 |
10 | 1.00 | |
30 | 0.40 |
下列说法正确的是
A.前10 min内反应的平均速率为v(Z)=0.10 mol·L-1·min-1
B.温度为200℃时,上述反应平衡常数为20,则正反应为吸热反应
C.若密闭容器体积可变,其他条件不变,在达到平衡后缩小容器体积为原来一半,则c(X)<1mol/L
D.保持其他条件不变,向容器中再充入1.00 mol X气体和1.20 mol Y气体,到达平衡后,X转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列转化关系中,烃A为石油的裂解气里含是较高的气体(碳元素的质量分数为0.857),B分子中含有三元环,分子式为C2H4O;1molD与足量Zn反应生成22.4LH2(标准状况);E为六元环化合物。请回答下列问题:

(1)写出A 的结构简式____________。
(2)①的反应类型为___________。
(3)D物质中含氧原子团的名称为___________;写出HOCH2CH2OH与金属钠反应的化学方程式___________。
(4)写出反应②的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁是一种常见的水处理剂,无水氯化铁遇潮湿空气,极易吸水生成FeCl3nH2O。在实验室中,可以采用下列仪器和药品制取较纯的无水氯化铁固体。

(1)实验开始时,先点燃____处的酒精灯(填A或D)。A中发生反应的化学方程式为____________________________________________。
(2)B装置中盛放的是饱和食盐水,其作用为__________________________________
(3)F装置中的试剂为浓硫酸,其作用是防止G中的水蒸气进入E中。用一件仪器装填适当试剂后,也可起到F和G的作用,所装填的试剂为_______________。
(4)G装置中反应的离子方程式为_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜基及硼系高温超导材料都具有良好的应用前景。回答下列问题:
(1)写出Cu原子价电子的轨道表达式:____________。BF3的立体构型是____________。
(2)NaBH4被认为是有机化学上的“万能还原剂”, NaBH4电子式为____________,其中三种元素的第一电离能由大到小的顺序是_________________。
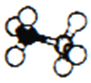
(3)BH3·NH3是一种有效、安全的固体储氢材料,结构如右图所示。 B原子的轨道杂化类型是____________。该物质中含有配位键,其中提供空轨道接受孤对电子的是____________。该物质易溶于水,其原因是____________。
(4)硼与氦形成类似苯的化合物B3N3H6(硼氮苯),俗称无机苯。硼氮苯属于分子____________(填“极性”或“非极性”),一个硼氮苯分子中有____________个σ键,形成π键的电子由____________提供。
(5)硼与镁形成的高温超导材料晶体结构如图所示。该六方晶胞中镁原子与硼原子的数量比为____________,晶体密度d=____________g·cm-3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】称取两份铝粉,第一份加足量NaOH溶液,第二份加足量硫酸,如果要得到相同体积(同温同压)的氢气,两份铝粉的质量比是( )
A. 1∶1 B. 1∶3 C. 3∶2 D. 1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于丙烯(CH3—CH = CH2)的说法不正确的
A. 丙烯分子有8个σ键,1个π键 B. 丙烯分子中碳原子有两种杂化方式
C. 丙烯分子至少有六个原子在同一平面上 D. 丙烯分子中3个碳原子在同一直线上
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com