
【题目】(1)分子式为C5H10、核磁共振氢谱中只有一个峰的烃的结构简式_______;
(2)①分子式为C7H8的芳香烃与浓硝酸反应的化学方程式____________________________,②环己烯与溴的四氯化碳溶液反应的化学方程式_________________________________;
(3)用系统命名法命名
①![]() 名称:_________________。
名称:_________________。
② 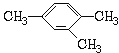 名称:_________________。
名称:_________________。
【答案】![]()
![]() +3HNO3(浓)
+3HNO3(浓)![]()
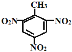 +3H2O
+3H2O ![]() +Br2
+Br2![]()
![]() 2,2,7-三甲基-4-乙基辛烷 1,2,4-三甲(基)苯
2,2,7-三甲基-4-乙基辛烷 1,2,4-三甲(基)苯
【解析】
(1)因该分子核磁共振氢谱中只有一个峰,说明分子中10个氢原子属于同一种等效氢原子,可推知该分子只能是环戊烷,其结构简式为![]() 。
。
(2) ①分子式为C7H8的芳香烃为甲苯,甲苯与浓硝酸发生硝化反应,生成2,4,6-三硝基甲苯,化学方程式为:![]() +3HNO3(浓)
+3HNO3(浓)![]()
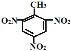 +3H2O。②环己烯与溴发生加成反应生成1,2-二溴环己烷,化学方程式为:
+3H2O。②环己烯与溴发生加成反应生成1,2-二溴环己烷,化学方程式为:![]() +Br2
+Br2![]()
![]() 。
。
(3) ①选择最长的碳链为主链,主链有8个碳原子称为辛烷,为使支链的位次之和最小,应该从右端开始给主链编号,该有机物名称为2,2,7-三甲基-4-乙基辛烷。②该分子为苯的同系物,给苯环上碳原子编号时要使侧链位次之和最小,其名称是1,2,4-三甲(基)苯。


科目:高中化学 来源: 题型:
【题目】在图所示的装置中,a的活动性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )
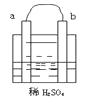
A.碳棒上有气体放出,溶液的pH增大
B.a是正极,b是负极
C.导线中有电子流动,电子从a极流到b极
D.a极上发生了氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人类较早使用的金属之一。运用铁及其化合物的有关知识,回答下列问题:
(1)铁和铁合金是生活中的常用材料,下列叙述中,正确的是________。
A.纯铁硬度比生铁高 B.纯铁耐腐蚀性强,不易生锈
C.不锈钢是铁合金,只含金属元素 D.铁在一定条件下,可与水蒸气反应
E.铁在冷的浓硫酸中钝化
(2)向沸水中逐滴滴加1 mol·L-1 FeCl3溶液,至液体呈透明的红褐色,该反应的离子方程式为______________________________________________________
形成该分散系的微粒直径范围是_________________________________。
(3)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出 FeCl3溶液与铜反应的离子方程式________________________________________________。
欲从腐蚀后的废液中回收铜并重新获得FeCl3溶液,现有下列试剂:①氯气,②铁粉,③浓硝酸,④浓盐酸,⑤烧碱,⑥浓氨水,需要用到的一组试剂是________。
A.①②④ B.①③④⑥ C.②④⑤ D.①④⑥
(4)高铁酸钠Na2FeO4 是一种新型净水剂。
①高铁酸钠主要通过如下反应制取:2Fe(OH)3+3NaClO+4NaOH===2Na2FeO4+3X+5H2O,则X的化学式为____________。
②下列物质能作水处理剂的有________。
A.KAl(SO4)2·12H2O B.[Fe(OH)(SO4)]n C.ClO2 D.“84”消毒液
③请写出向酸化的FeCl2溶液中滴加双氧水的离子方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将标准状况下2.24L CO2缓慢通入1L0.15molL-1的NaOH溶液中,气体被充分吸收,下列关系不正确的是
A. c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
B. c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
C. 2c(Na+)=3[c(H2CO3)+c(HCO3-)+c(CO32-)]
D. 2c(OH-)+c(CO32-)=c(HCO3-)+3c(H2CO3)+2c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~J均为有机化合物,它们之间的转化如下图所示:

实验表明:
①D既能发生银镜反应,又能与金属钠反应放出氢气 ;
②核磁共振氢谱表明:G、I分子中有两种氢,F分子中有三种氢,且其峰面积之比为1 :1 :1 ;
③G能使溴的四氯化碳溶液褪色 ;
④1mol J与足量金属钠反应可放出22.4L氢气(标准状况)。
请根据以上信息回答下列问题:
(1)A的结构简式为___________________________。
(2)D的结构简式为___________________________________。
(3)由E生成F的化学方程式为____________________________。与E具有相同官能团的E的同分异构体还有 ___________种。
(4)G的结构简式为__________________________。
(5)由I生成J的化学方程式_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,反应X(g)![]() 4Y(g)+Z(g) ΔH=-Q kJ·mol-1在2 L恒容密闭容器中进行,X和Z的浓度随时间变化如图所示,下列说法不正确的是
4Y(g)+Z(g) ΔH=-Q kJ·mol-1在2 L恒容密闭容器中进行,X和Z的浓度随时间变化如图所示,下列说法不正确的是

A. 2 min内,X的平均反应速率为0.25 mol·L-1·min-1
B. 第t min时,该反应达到平衡状态
C. 第5 min后,X的生成速率与Z的生成速率相等且保持不变
D. 5 min内,反应放出的热量为1.6Q kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.金刚石和石英晶体都是原子晶体,都属于共价化合物
B.NaOH和MgCl2晶体中都含有共价键,但都属于离子晶体
C.氮化镁中每个离子的最外电子层都形成了具有8个电子的稳定结构
D.NaCl溶液蒸发结晶过程中,有离子键的形成,但没有分子间作用力的破坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨化学方程式 N2(g)+3H2(g)![]() 2NH3(g) △H=92.4 kJ/mol。将l mol N2(g)、3 mol H2(g)充入2 L的密闭容器中,在500℃下反应,10 min 时达到平衡,NH3的体积分数为
2NH3(g) △H=92.4 kJ/mol。将l mol N2(g)、3 mol H2(g)充入2 L的密闭容器中,在500℃下反应,10 min 时达到平衡,NH3的体积分数为![]() ,下列说法中正确的是
,下列说法中正确的是

A. 若达到平衡时,测得体系放出9.24 kJ热量,则H2反应速率变化曲线如图甲所示
B. 反应过程中,混合气体平均相对分子质最M,混合气体密度d,混合气体压强p,三者关系如图乙所示
C. 图丙容器I和II达到平衡时,NH3的体积分数![]() ,则容器I放出热量与容器II吸收热量之和为92.4 kJ
,则容器I放出热量与容器II吸收热量之和为92.4 kJ
D. 若起始加入物料为1 mol N2,3 mol H2,在不同条件下达到平衡时,NH3的体积分数变化如图丁所示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、 F、G是周期表中短周期的七种元素,有关性质或结构信息如下表:
元素 | 有关性质或结构信息 |
A | 地壳中含量最多的元素 |
B | B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的 |
C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
D | D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味 |
E | E与D同周期,且在该周期中原子半径最小 |
F | F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
G | G是形成化合物种类最多的元素 |
(1) B元素符号为____,A与C以原子个数比为1:1形成的化合物的电子式为___,用电子式表示C与E形成化合物的过程____, D形成的简单离子的结构示意图为____。
(2) F的氢化物是由____(极性或非极性)键形成的分子,写出实验室制备该氢化物的化学方程式____。
(3) 非金属性D____E(填大于或小于),请从原子结构的角度解释原因:__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com