
【题目】《科学美国人》评出2016年十大创新技术:碳呼吸电池、量子卫星、万能抗病毒药……,“碳呼吸电池”是一种新型能源装置,其工作原理如图。下列有关说法错误的是( )

A. 该装置是将化学能转变为电能
B. 金属铝是负极,多孔碳是正极
C. 正极的电极反应为2CO2-2e-=C2O42-
D. 将电池配备在火力发电站和汽车排气管上,不但可减少 CO2排放,而且还可以利用CO2
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】物质的量是一个将微观粒子与宏观物质联系起来的物理量。下列说法正确的是( )
A.1mol H2的体积为22.4 L
B.1mol SiO2含有6.02×1023个分子
C.1mol O2的质量为32g
D.0.1mol/L MgCl2溶液含0.1mol Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,某容积固定的密闭容器由可移动的活塞隔成左、右两室,左室充入等物质的量的氢气和氧气,右室充入一氧化碳和氧气的混合气。同时引燃左右两室的混合气,反应后恢复到室温。反应前后活塞位置如下图所示,则右室混合气体中一氧化碳和氧气的物质的量之比可能是(液态水的体积忽略不计)

①1:1 ②1:2 ③1:3 ④3:1
A. ①② B. ②④ C. ①④ D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。

已知:
Ⅰ. ![]()
Ⅱ. ![]() (苯胺、易被氧化)
(苯胺、易被氧化)
请根据所学知识与本题所给信息回答下列问题:
(1)X的分子式是__________;C的名称是___________。
(2)H的结构简式是_____________。
(3)反应②、④的类型是__________。
(4)反应⑤的化学方程式是____________;
(5) 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有_______种。
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有_______种。
(6)请用合成反应流程图表示出由A和其他无机物(溶剂任选)合成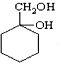 最合理的方案。
最合理的方案。
示例如下:

____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备干燥的氨气所需的药品是( )
A. 饱和氨水、浓硫酸 B. NH4Cl稀溶液、NaOH稀溶液、碱石灰
C. NaOH溶液、NH4Cl晶体、浓H2SO4 D. NH4Cl固体、消石灰、碱石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项中说明乙醇作为燃料的优点的是
①燃烧时只发生氧化反应 ②充分燃烧的产物不污染环境③乙醇是一种再生能源 ④燃烧时放出大量的热
A. ②③ B. ②④ C. ①③④ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸钠铝[NaaAlb(OH)c(CO3)d]可用作阻燃剂、抗酸剂等。其制备方法是:控制温度、pH,向NaHCO3稀溶液中加入Al(OH)3,并搅拌,充分反应后过滤、洗涤、干燥,得碱式碳酸钠铝。
(1)碱式碳酸钠铝[NaaAlb(OH)c(CO3)d]中a、b、c、d之间的关系为________。
(2)碱式碳酸钠铝作为阻燃剂的可能原因:①在分解过程中大量吸热;②本身及产物无毒且不可燃;③________________________。
(3)若pH过高,则对产品的影响是________________________。
(4)为确定碱式碳酸钠铝的组成,进行如下实验:
①准确称取2.880 g样品用足量稀硝酸溶解,得到CO2 0.448 L(已换算成标准状况下),并测得溶液中含有0.02 mol Al3+。
②加热至340 ℃以上时样品迅速分解,得到金属氧化物、CO2和H2O。当样品分解完全时,样品的固体残留率(固体样品的剩余质量/固体样品的起始质量×100%)为56.9%,根据以上实验数据确定碱式碳酸钠铝的组成(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烷烃的混合物,在标准状况下其密度为1.03 g·L-1 ,则关于该混合物组
成的说法正确的是( )
A. 一定有甲烷 B. 一定有乙烷
C. 不可能是甲烷和乙烷的混合物 D. 可能是乙烷和丙烷的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知吸热反应2CO(g)=2C(s)+O2(g),设ΔH和ΔS不随温度而变化,下列说法中正确的是( )
A.低温下能自发进行B.高温下能自发进行
C.任何温度下都能自发进行D.任何温度下都不能自发进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com