
【题目】下列说法正确的是
A. 葡萄糖、氨基酸在一定条件下都能发生酯化反应
B. 用过滤的方法可以分离乙酸乙酯和乙酸
C. 医用酒精是质量分数为95%的乙醇溶液
D. 往蛋白质溶液中加入浓的CuSO4溶液,蛋白质会发生盐析
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】原子序数小于36的X、Y、Z、M、N、W六种元素,原子序数依次增大。已知X是迄今为止形成化合物最多的元素。Y原子最外层电子数与核外电子总数之比为3∶4。M元素的常见氧化物有两种,其中一种常温下为气体,且是主要的大气污染物。Z、M、N 同周期,M2-、N-、Z+ 离子半径逐渐减小。W是第Ⅷ族元素中原子序数最小的元素。据此回答:
(1)写出W在周期表中位于哪一区:_____________,X与N按1:4形成的化合物中,X和N之间的σ键的类型:____________;
(2)用电子式表示Z与M形成化合物的过程_____________________________________;
(3)X、Y、M的电负性由小到大的顺序是____________________填元素符号);N3一与X、Y形成的一种化合物互为等电子体,则N3一的空间构型为________________;
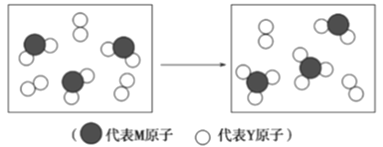
(4)下图表示由上述两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:____________________
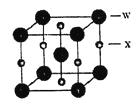
(5)X和W所形成的某种晶体结构如右图所示,写出: 基态W3+离子的结构示意图:_____________;
(6)N元素基态原子核外电子有_______种空间运动状态?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g)![]() CH3OH(g) △H3=-90.77kJ·mol-1
CH3OH(g) △H3=-90.77kJ·mol-1
回答下列问题:
(1)反应Ⅱ的△H2=______________________。
(2)反应Ⅲ能够自发进行的条件是__________(填“较低温度”、“ 较高温度”或“任何温度”)。
(3)恒温,恒容密闭容器中,对于反应Ⅰ,下列说法中能说明该反应达到化学平衡状态的是________。
A.混合气体的密度不再变化B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1D.甲醇的百分含量不再变化
(4)对于反应Ⅰ,不同温度对CO2的转化率及催化剂的效率影响如图所示,下列有关说法不正确的是____。

A.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率仍位于M
B.温度低于250℃时,随温度升高甲醇的产率增大
C.M点时平衡常数比N点时平衡常数大
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(5)若在1L密闭容器中充入3molH2和1molCO2发生反应Ⅰ,则图中M点时,产物甲醇的体积分数为_________________;该温度下,反应的平衡常数K=______________L2/mol2;若要进一步提高甲醇体积分数,可采取的措施有____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水(酸性)中的有机物可用C6H10O5表示[交换膜分别是只允许阴(阳) 离子通过的阴(阳)离子交换膜],下列有关说法中不正确的是
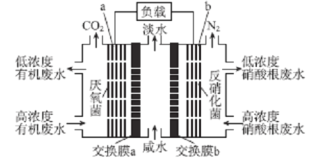
A.电池工作时,电子由a极经导线流向b极
B.交换膜a是阴离子交换膜
C.电极 b 的反应式:2NO3-+l0e-+12H+=N2↑+6H2O
D.相同时间内(相同状况下)生成CO2和N2的体积比为2:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法正确的是( )
A.ClO2是氧化产物
B.KClO3在反应中得到电子
C.H2C2O4在反应中被还原
D.1 mol KClO3参加反应有2 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)标准状况下,测得1.32 g 某气体的体积为0.672 L,则此气体的摩尔质量为___________________。
(2)三种正盐的混合溶液中含有c(Na+)=0.2 mol·L–1、c(Mg2+)=0.25 mol·L–1、c(Cl–)=0.4 mol·L–1,则c(SO42-)为________mol·L–1。
(3)0.12 mol FeCl2加入100 mL K2Cr2O7溶液中,恰好使溶液中Fe2+全部转化为Fe3+,Cr2O72–被还原为Cr3+。则K2Cr2O7溶液的物质的量浓度为____________ mol·L–1。
(4)现实验室要用质量分数为40%的浓氢氧化钠(密度为1.2 g·mL–1)来配制浓度为0.6 mol·L–1的稀氢氧化钠溶液100 mL,则需要这种浓碱的体积是__________ mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关于Cl2的说法中,错误的是
A. Cl2是一种黄绿色、密度比空气大的有毒气体
B. 红热的铁丝在Cl2中剧烈燃烧,产生白色烟雾
C. 工业上用Cl2和石灰乳为原料制造漂白粉
D. Cl2能与水反应生成盐酸和次氯酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列化合物的名称或结构简式:
① _______________________________,
_______________________________,
②CH2=C(CH3)CH=CH2_______________________________,
③CH2=CHCOOH _______________________________,
④2,5-二甲基-2,4-己二烯的结构简式:_________________________________。
(2)麻黄素又称黄碱,是我国特定的中药材麻黄中所含有的一种生物碱,经我国科学家研究发现其结构如图:

①麻黄素中含氧官能团的名称是_________________,属于____________类(填“醇”或“酚”)。
②下列各物质:
A. 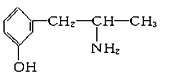 B.
B. 
C.  D.
D. 
E. 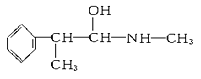
与麻黄素互为同分异构体的是________(填字母,下同),互为同系物的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为:2KClO3+4HCl(浓)===2KCl+2ClO2↑+Cl2↑+2H2O。
(1)请分析该反应中电子转移的情况(用双线桥法表示)___________________________。
(2)浓盐酸在反应中显示出来的性质是________
(3)若产生0.1 mol Cl2,则被氧化的HCl的物质的量为________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com