
【题目】下列有关物质的分类或性质与应用均正确的是( )
A. Al2O3的熔点很高,可用于制作耐高温材料
B. Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒
C. 硅晶体是良好的半导体,可用于制造光导纤维
D. Al(OH)3是一种强碱,可以与酸反应,可用作医用的胃酸中和剂
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.石油裂解主要是为了获得气态不饱和短链烃
B.煤是由有机物和无机物组成的复杂的混合物,其中含有焦炭、苯、甲苯等
C.甲醛俗称蚁醛,可用于制造酚醛树脂
D.生产口罩的熔喷布主要成分是聚丙烯,可通过丙烯加聚得到
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )
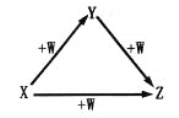
①C、CO ②AlCl3、 Al(OH)3 ③N2、NO ④S、SO2
A. ①② B. ②③ C. ③④ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列有关说法正确的是( )
A.在常温常压下,11.2LN2含有的分子数为0.5NA
B.在常温常压下,1mol氦气含有的原子数为2NA
C.71gCl2所含原子数为2NA
D.23g钠在化学反应中失去电子数目为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.01 mol的酸性混合溶液中加入0.01 mol铁粉,经搅拌后发生的变化应是 ( )
A. 铁溶解,析出0.01 mol Ag和0.005 mol Cu
B. 铁溶解,析出0.01 mol Ag并放出H2
C. 铁溶解,析出0.01 mol Ag,溶液中不再有Fe3+
D. 铁溶解,析出0.01 mol Ag,溶液中不再有Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯及其氯的化合物,有广泛的应用。请回答下列问题:
(1)亚氯酸(HClO2)中氯元素的化合价是____,其电离方程式是______________,NaClO2溶液显_________(填“酸性”、“中性”、“碱性”)。
(2)①向新制饱和氯水中加适量CaCO3制取次氯酸,其反应的总的离子方程式是:_______。
②可用Cl2除去工业废水中CN- ,生成无污染的CO2和N2,写出反应的离子方程式:_____。
(3)CsICl2受热发生非氧化还原反应,则其受热分解的化学方程式是: ______________。
(4)ClO2是一种黄色极易爆炸的强氧化性气体,较安全的制备方法是:NaClO3+SO2+H2SO4—NaHSO4+ClO2(未配平),氧化剂与还原剂的物质的量之比是 _______。
(5)工业上高氯酸可由高氯酸钠和浓硫酸经复分解反应制备:NaClO4+H2SO4(浓)→NaHSO+HClO(易爆)。也可以用铜做阴极、铂做阳极,电解盐酸制备HClO4,写出阳极的电极反应式 ___________________________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次硫酸氢钠甲醛(NaHSO2HCHO2H2O)俗称吊白块,不稳定,120℃时会分解。在印染、医药以及原子能工业中有广泛应用。以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
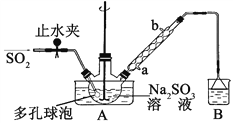
步骤1:在三颈烧瓶中加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,至溶液pH 约为4,制得NaHSO3溶液。
步骤2:将装置A 中导气管换成橡皮塞。向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80~90℃下,反应约3h,冷却至室温,抽滤;
步骤3:将滤液真空蒸发浓缩,冷却结晶。
(1)装置B 的烧杯中应加入的溶液是____________;冷凝管中冷却水从_____(填“a”或“b”)口进水。
(2)A中多孔球泡的作用是__________________________________________。
(3)冷凝管中回流的主要物质除H2O 外还有________ (填化学式)。
(4)写出步骤2中发生反应的化学方程式________________________________。
(5)步骤3中在真空容器中蒸发浓缩的原因是____________________________。
(6)为了测定产品的纯度,准确称取2.0g样品,完全溶于水配成100mL溶液,取20.00mL所配溶液,加入过量碘完全反应后(已知I2不能氧化甲醛,杂质不反应),加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重得到白色固体0.466g,则所制得的产品的纯度为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题目要求完成填空:
(1)下列物质中,电解质;非电解质A.氢氧化钠溶液 B.液氨 C.氯化钠晶体 D.二氧化碳 E.硫酸钡
(2)100mLFe2(SO4)3溶液中含有Fe3+11.2g,其中铁离子的物质的量n(Fe3+)= , 硫酸根离子的物质的量浓度c(SO ![]() )= , 取25mL溶液稀释到100mL,则稀释后溶液中Fe3+的物质的量浓度是c(Fe3+)= , 稀释后溶液中Fe2(SO4)3的质量m= .
)= , 取25mL溶液稀释到100mL,则稀释后溶液中Fe3+的物质的量浓度是c(Fe3+)= , 稀释后溶液中Fe2(SO4)3的质量m= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学式为C8H10的芳香烃,苯环上的一硝基(﹣NO2是一种官能团)取代物只有一种,该芳香烃的名称是( )
A.乙苯
B.邻二甲苯
C.间二甲苯
D.对二甲苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com