
A、CH4
| |||
B、CH2═CH2
| |||
C、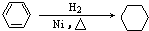 | |||
D、CH4
|


科目:高中化学 来源: 题型:
| A、铜锌原电池工作时,若有6.5g锌被溶解,电路中就有0.1mol电子通过 |
| B、原电池装置中,电子从正极流向负极 |
| C、可利用CH4和O2的反应设计成原电池 |
| D、在周期表中金属和非金属的分界处易寻找到催化剂和耐高温、耐腐蚀的合金材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18g水中含有的电子数为10NA |
| B、标准状态下,22.4L氦气中含NA个氦原子 |
| C、1molCl2与金属Na完全反应,可以得到2NA个电子 |
| D、在2mol/L的硝酸镁溶液中含有的硝酸根离子数位4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- | ||||
B、往硫酸铝铵NH4Al(SO4)2溶液中滴加Ba(OH)2溶液并加热,刚好使NH4+全部转化为NH3:NH4++Al3++2SO42-+2Ba2++4OH-
| ||||
C、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-
| ||||
| D、FeSO4溶液与稀硫酸、双氧水混合:Fe2++H2O2+2H+═Fe3++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
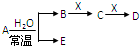 已知A、B、C、D、E、X是H、C、N、O、Na、Al、Cl、Fe等元素组成的常见单质或化合物,它们之间存在如图所示转化关系(部分生成物和反应条件已略去)
已知A、B、C、D、E、X是H、C、N、O、Na、Al、Cl、Fe等元素组成的常见单质或化合物,它们之间存在如图所示转化关系(部分生成物和反应条件已略去)| A、若E为氧化物,则X一定为Fe |
| B、若E为氧化物,则在A与水的反应中,氧化剂和还原剂的质量比为1:2 |
| C、若E为单质气体,D为白色沉淀,B可能是共价化合物,也可能是离子化合物 |
| D、若B为单质气体,X可能为C、Na、N2+等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、非金属性:X>Y>Z |
| B、X、Y、Z的最高价氧化物的水化物酸性由弱到强 |
| C、气体氢化物的稳定性,按X、Y、Z顺序递减 |
| D、X、Y、Z的最外层电子数依次减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠是银白色金属,硬度很大 |
| B、将金属钠放在坩埚里用酒精灯加热,生成淡黄色固体氧化钠 |
| C、金属钠在空气中燃烧,产生黄色火焰,生成过氧化钠 |
| D、金属钠的熔点很高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在原电池的负极和电解池的阴极上都是发生失电子的氧化反应 |
| B、用惰性电极电解饱和NaCl溶液,若有1mol电子转移,则生成1mol NaOH |
| C、用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2 |
| D、镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
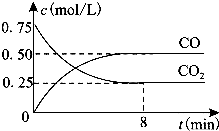 一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)=FeO(s)+CO(g)△H>0,1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示.
一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)=FeO(s)+CO(g)△H>0,1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示.| 容器 | 甲 | 乙 |
| 反应物投入量 | 3mol Fe、2mo lCO2 | 4mol FeO、3mol CO |
| CO的浓度(mol?L-1) | c1 | c2 |
| CO2的体积分数 | φ1 | φ2 |
| 体系压强(Pa) | P1 | P2 |
| 气态反应物的转化率 | a1 | a2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com