
【题目】将4molA气体和2molB气体置于2L的密闭容器中,混合后发生如下反应:2A(g)+ B(g)=2C(g),若经2s后测得C的浓度为1.2mol/L,下列说法符合题意是( )
A. 用物质A表示的反应速率为1.2 mol/(Ls)
B. 用物质B表示的反应速率为0.3mol/(Ls)
C. 2s时物质A的转化率为40%
D. 2s时物质B的浓度为0.6mol/L
【答案】B
【解析】
A.根据化学反应方程式可知:反应产生C的浓度为1.2mol/L,则反应消耗的A的浓度为1.2mol/L,则υ(A)=![]() =0.6mol/(L·s),A错误;
=0.6mol/(L·s),A错误;
B.根据化学反应方程式可知:反应产生C的浓度为1.2mol/L,则反应消耗的B的浓度为0.6mol/L,则υ(B)=![]() =0.3mol/(L·s),B正确;
=0.3mol/(L·s),B正确;
C.2s时物质A的转化浓度为1.2mol/L,开始时A的浓度为2mol/L,则A的转化率为(1.2mol/L ÷2mol/L)×100%=60%,C错误;
D.反应开始时B的浓度为1mol/L,转化浓度为0.6mol/L,所以2s时物质B的浓度为0.4mol/L,D错误;
故合理选项是B。


科目:高中化学 来源: 题型:
【题目】第三周期元素X、Y、Z、W的最高价氧化物溶于水可得四种溶液,0.01mol/L的这四种溶液pH与该元素原子半径的关系如图所示。下列说法正确的是
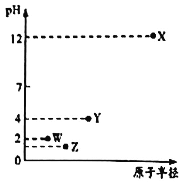
A.简单离子半径:X>Y>Z>W
B.Z与X形成的化合物的水溶液pH>7
C.气态氢化物的稳定性:Z>W>Y
D.X和Y的最高价氧化物对应的水化物恰好中和时,溶液中的微粒共有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式正确的是
A.用惰性电极电解饱和食盐水的化学方程式:2NaCl+H2O![]() H2↑+Cl2↑+2NaOH
H2↑+Cl2↑+2NaOH
B.苯和液溴的反应C6H6+Br2![]() C6H4Br2+H2
C6H4Br2+H2
C.氯化铁水解的离子方程式:Fe3++3H2OFe(OH)3+3H+
D.稀硝酸滴在石灰石上:CO32-+2H+=H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①写出漂白粉的有效成分的化学式_____;
②用系统命名法给有机物CH3CH(CH3)2命名________。
(2)①写出碳与浓硫酸反应的化学方程式______;
②写出乙醇与金属钠反应的方程式_______。
(3)H2O2和Fe3+都具有氧化性,氧化性强弱关系为H2O2____Fe3+(填“>”“<”或“=”),用有关的离子反应方程式证明以上结论____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)是一种高效清洁的火箭燃料。0.25molN2H4(g)完全燃烧生成氮气和气态水时,放出133.5kJ热量。则下列热化学方程中正确的是( )
A.![]() N2H4(g)+
N2H4(g)+![]() O2(g)=
O2(g)=![]() N2(g)+H2O(l) △H=+267kJmol-1
N2(g)+H2O(l) △H=+267kJmol-1
B.N2H4(g)+O2(g)=N2(g)+2H2O(l) △H=-133.5kJmol-1
C.N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=+534kJmol-1
D.N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.用相应的方程式解释:
(1)NaHSO3溶液显酸性:___________________
(2)NaHCO3溶液显碱性:____________________
(3)NH4Cl溶液显酸性:______________________
(4)明矾[KAl(SO4)2]净水:___________________
(5)FeCl3溶液蒸干得到Fe2O3固体:____________(第一步反应)
II.向2份0.1mol/LCH3COONa溶液中分别加入少量NH4NO3、Na2CO3固体(忽略溶液体积变化),则CH3COO-浓度的变化依次为_______、______(填“减小”、“增大”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】深埋在潮湿土壤中的铁管道,在硫酸盐还原菌(一种厌氧微生物)的作用下,能被硫酸根离子腐蚀,其电化学腐蚀原理如图所示。下列与此原理有关的说法错误的是
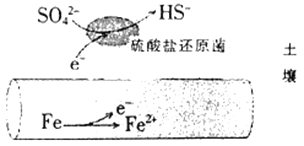
A.负极反应为SO42-+5H2O+8e-=HS-+9OH-
B.输送暖气的管道不易发牛此类腐蚀
C.这种情况下,Fe腐蚀的最终产物为FeO或Fe(OH)2
D.管道上刷富锌油漆可以延缓管道的腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①铅蓄电池总反应为: Pb(s) + PbO2(s) + 2H2SO4(aq) ![]() 2PbSO4(s) + 2H2O(l)
2PbSO4(s) + 2H2O(l)
②电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。
下列关于电池的叙述正确的是
A.充电电池的化学反应原理是氧化还原反应
B.铅蓄电池可以无限制地反复放电、充电,不会造成环境污染
C.铅蓄电池比锂电池的理论比能量高
D.铅蓄电池正极电极反应为:PbO2 +4H+ +2e— = Pb2+ +2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在20.0mL0.10mol·L-1氯水中滴入0.10mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。己知0.10mol·L-1氨水的电离度为1.32%,下列有关叙述正确的是

A. 该滴定过程应该选择酚酞作为指示剂
B. M点对应的盐酸体积为20.0mL
C. M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D. N点处的溶液中pH<12
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com