
【题目】[化学——选修2:化学与技术]
聚合硫酸铁(PFS)是谁处理中重要的絮凝剂,下图是以回收废铁屑为原料制备PFS的一种工艺流程。

回答下列问题
(1)废铁屑主要为表面附有大量铁锈的铁,铁锈的主要成分为_________。粉碎过筛的目的是_______
(2)酸浸时最合适的酸是_____,写出铁锈与酸反应的离子方程式_____________________。
(3)反应釜中加入氧化剂的作用是_________,下列氧化剂中最合适的是____________(填标号)。
A.KMnO4 | B. | C. | D. |
(4)聚合釜中溶液的pH必须控制在一定的范围内,pH偏小时Fe3+水解程度弱,pH偏大时则_______。
(5)相对于常压蒸发,减压蒸发的优点是______。
(6)盐基度B是衡量絮凝剂絮凝效果的重要指标,定义式为![]() (n为物质的量)。为测量样品的B值,取样品mg,准确加入过量盐酸,充分反应,再加入煮沸后冷却的蒸馏水,以酚酞为指示剂,用c
(n为物质的量)。为测量样品的B值,取样品mg,准确加入过量盐酸,充分反应,再加入煮沸后冷却的蒸馏水,以酚酞为指示剂,用c![]() 的标准NaOH溶液进行中和滴定(部分操作略去,已排除铁离子干扰)。到终点时消耗NaOH溶液V mL。按照上述步骤做空白对照试验,消耗NaOH溶液
的标准NaOH溶液进行中和滴定(部分操作略去,已排除铁离子干扰)。到终点时消耗NaOH溶液V mL。按照上述步骤做空白对照试验,消耗NaOH溶液![]() ,已知该样品中Fe的质量分数w,则B的表达式为__________
,已知该样品中Fe的质量分数w,则B的表达式为__________
【答案】(1)Fe2O3·xH2O 选取细小颗粒,增大反应物接触面积,提高“酸浸”反应速率 (2)硫酸 Fe2O3·xH2O+6H+=2Fe3++3SO42-+(x+3)H2O
(3)氧化Fe2+c (4)pH过大,容易生成Fe(OH)3,产率降低
(5)减压蒸馏,可防止温度过高,聚合硫酸铁分解 (6)![]()
【解析】
试题分析:(1)废铁屑主要为表面附有大量铁锈的铁,铁锈的主要成分为Fe2O3·xH2O。粉碎过筛的目的是控制铁屑的颗粒。
(2)由于不能引入杂质,则酸浸时最合适的酸是硫酸,铁锈与酸反应的离子方程式为Fe2O3·xH2O+6H+=2Fe3++3SO42-+(x+3)H2O。
(3)由于溶液中含有亚铁离子,则反应釜中加入氧化剂的作用是氧化Fe2+,由于不能引入杂质,则氧化剂中最合适的是绿色氧化剂双氧水。
(4)聚合釜中溶液的pH必须控制在一定的范围内,pH偏小时![]() 水解程度弱,pH偏大时则Fe3+转化为氢氧化铁沉淀而损失,造成产率降低。
水解程度弱,pH偏大时则Fe3+转化为氢氧化铁沉淀而损失,造成产率降低。
(5)相对于常压蒸发,减压蒸发的优点是可防止温度过高,聚合硫酸铁分解。
(6)做空白对照试验,消耗NaOH溶液![]() ,这说明与样品反应的盐酸的物质的量是(V0-V)c×10-3mol,所以样品中氢氧根的物质的量是(V0-V)c×10-3mol。已知该样品中Fe的质量分数w,则铁的物质的量是
,这说明与样品反应的盐酸的物质的量是(V0-V)c×10-3mol,所以样品中氢氧根的物质的量是(V0-V)c×10-3mol。已知该样品中Fe的质量分数w,则铁的物质的量是![]() ,因此B的表达式为
,因此B的表达式为![]() =
=![]() 。
。


科目:高中化学 来源: 题型:
【题目】丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈CH3CN 等,回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯睛(C3H3N)和副产物丙烯醛(CH2=CHCHO)的热化学方程式如下:
① C3H6(g)+NH3(g)+O2(g)=C3H3N(g)+3H2O(g)△H=-515kJ/mol
② C3H6(g)+O2(g)=C3H4O(g)+H2O(g) △H=-353kJ/mol
有利于提高丙烯腈平衡产率的反应条件是______;提高丙烯腈反应选择性的关键因素是_____.
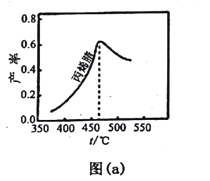
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃。低于460℃时,丙烯腈的产率________(填“是”或者“不是”)对应温度下的平衡产率,判断理由是_____;高于460℃时,丙烯腈产率降低的可能原因是________(双选,填标号)。
A.催化剂活性降低 B.平衡常数变大 C.副反应增多 D. 反应活化能增大
(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n(丙烯)约为_________ ,理由是_______。进料氨、空气、丙烯的理论体积约为____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向2 L密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:xA(g)+yB(g) ![]() pC(g)+qD(g)。已知:平均反应速率vC=
pC(g)+qD(g)。已知:平均反应速率vC=![]() vA;反应2 min时,A的物质的量减少了
vA;反应2 min时,A的物质的量减少了![]() ,B的物质的量减少了
,B的物质的量减少了![]() mol,有a mol D生成。
mol,有a mol D生成。
回答下列问题:
(1)反应2 min内,vA=________,vB=________。
(2)化学方程式中,x=________,y=__________,p=__________,q=________。
(3)反应平衡时,D为2a mol,则B的转化率为________。
(4)如果只升高反应温度,其他反应条件不变,平衡时D为1.5a mol,则该反应的ΔH________0。(填“>”“<”或“=”)
(5)如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较:①反应速率________(填“增大”“减小”或“不变”),理由是_____________________。
②平衡时反应物的转化率________(填“增大”“减小”或“不变”),理由是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中,一定条件下进行反应:NO(g)+CO(g)=1/2N2(g)+CO2(g) ΔH=-373.2 kJ/mol。如图曲线a表示该反应过程中,NO的转化率与反应时间的关系,若改变起始条件,使反应过程按照曲线b进行,可采取的措施是( )

A. 加催化剂 B. 向密闭容器中加入氩气
C. 降低温度 D. 增大反应物中NO的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列鉴别方法不可行的是
A.用水鉴别乙醇、苯和溴苯B.用溴水鉴别己烯、苯和四氯化碳
C.用酸性高锰酸钾溶液鉴别苯、乙醇和戊烷D.用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。下列A、B、C、D是中学常见的混合物分离或提纯的装置。

I.请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)碳酸钙悬浊液中分离出碳酸钙_____;
(2)氯化钠溶液中分离出氯化钠____;
(3)分离植物油和水____;
(4)海水淡化___;
(5)除去自来水中的Cl﹣等杂质____;
(6)从碘水中分离出I2____。
II.碘水中提取碘单质的方法如下:
(1)萃取分液
①下列可作为碘水中提取碘单质萃取剂的是____
A.酒精 B.苯
②分液漏斗在使用前必须先____
③查资料得知:ρ(H2O)>ρ(苯)>ρ(酒精),若用①中所选萃取剂萃取碘水中的碘单质,分液时,上层液体显___色。
(2)蒸馏
①装置A中a的名称是___,a中加入少量___防止加热时液体暴沸。冷凝装置中冷凝水应该____口进(填“上”或“下”)。
②已知碘和四氯化碳的熔沸点数据如表
熔点 | 沸点 | |
碘 | 113.7℃ | 184.3℃ |
四氯化碳 | -22.6℃ | 76.8℃ |
若用蒸馏法分离碘和四氯化碳的混合物,锥形瓶中先收集到的物质的名称是______。
Ⅲ.海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
[海水]![]() [粗盐]
[粗盐]![]() [食盐水]→[氯化钠晶体]
[食盐水]→[氯化钠晶体]
问题一:粗盐中含Ca2+、Mg2+、SO42﹣等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发,正确的操作顺序是____(填选项字母)
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
问题二:蒸发进行到____时,停止加热。
问题三:粗盐中含有少量泥沙、CaCl2、MgCl2及硫酸盐,将粗盐溶解后,先过滤将泥沙除去,再检验滤液中的SO42﹣,如何检验某未知溶液中的SO42﹣___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验现象或要求写离子方程式(描述现象的,需要写出所有涉及的离子方程式。
实验现象 | 离子方程式 |
(1)澄清石灰水中通入CO2出现白色沉淀,继续通,沉淀溶解,加热后又出白色沉淀。 | ___________ |
(2)湿法制备高铁酸钾(K2FeO4)的过程为,在氢氧化铁固体中加入KClO和KOH的混合液。写出该过程的离子方程式并配平。 | _______________ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com