
【题目】易溶于水的含氧有机物是
① 硝基苯 ② 苯 ③ 溴苯 ④ 乙醇 ⑤ 乙酸乙酯 ⑥ 乙酸 ⑦ 碳酸
A. ①⑤B. ②③C. ④⑥D. ⑤⑦
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】[化学——选修2:化学与技术]
聚合硫酸铁(PFS)是谁处理中重要的絮凝剂,下图是以回收废铁屑为原料制备PFS的一种工艺流程。

回答下列问题
(1)废铁屑主要为表面附有大量铁锈的铁,铁锈的主要成分为_________。粉碎过筛的目的是_______
(2)酸浸时最合适的酸是_____,写出铁锈与酸反应的离子方程式_____________________。
(3)反应釜中加入氧化剂的作用是_________,下列氧化剂中最合适的是____________(填标号)。
A.KMnO4 | B. | C. | D. |
(4)聚合釜中溶液的pH必须控制在一定的范围内,pH偏小时Fe3+水解程度弱,pH偏大时则_______。
(5)相对于常压蒸发,减压蒸发的优点是______。
(6)盐基度B是衡量絮凝剂絮凝效果的重要指标,定义式为![]() (n为物质的量)。为测量样品的B值,取样品mg,准确加入过量盐酸,充分反应,再加入煮沸后冷却的蒸馏水,以酚酞为指示剂,用c
(n为物质的量)。为测量样品的B值,取样品mg,准确加入过量盐酸,充分反应,再加入煮沸后冷却的蒸馏水,以酚酞为指示剂,用c![]() 的标准NaOH溶液进行中和滴定(部分操作略去,已排除铁离子干扰)。到终点时消耗NaOH溶液V mL。按照上述步骤做空白对照试验,消耗NaOH溶液
的标准NaOH溶液进行中和滴定(部分操作略去,已排除铁离子干扰)。到终点时消耗NaOH溶液V mL。按照上述步骤做空白对照试验,消耗NaOH溶液![]() ,已知该样品中Fe的质量分数w,则B的表达式为__________
,已知该样品中Fe的质量分数w,则B的表达式为__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知KMnO4与浓盐酸反应的化学方程式为:2KMnO4+16HCl(浓)=2MnCl2+8H2O+2KCl+5Cl2↑,回答下列问题:
(1)请用双线桥表示出该反应转移电子的方向和数目_______________________________
(2)被氧化的HCl占HCl总量的_______ 被还原的元素_________(填元素符号)
(3)当标准状况下有0.5mol氯气生成时,该反应转移的电子数为_____(设NA为阿伏加德罗常数的值)
(4)15.8g KMnO4与含1.2molHCl的浓盐酸完全反应(假设HCl无挥发),在反应后的溶液中加入足量的AgNO3溶液,可生成_____g沉淀.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A处通入干燥的氯气,打开B阀后,C处的红布条逐渐退色,关闭B阀时,C处的红布条看不到明显现象,则D瓶中装的是( )

A. 浓硫酸B. 浓NaOH溶液
C. 浓盐酸D. 饱和NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,m g气体A与n g气体B的分子数相同,下列说法中不正确的是
A. 两种气体A与B的相对分子质量之比为m∶n
B. 同质量气体A与B的分子数之比为n∶m
C. 同温同压下,A、B两气体的密度之比为n∶m
D. 相同状况下,同体积A、B两气体的质量之比为m∶n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现以CO、O2、熔融盐Z(Na2CO3)组成的燃料电池,采用电解法处理CO同时制备N2O5,装置如图所示,其中Y为CO2。下列说法不合理的是
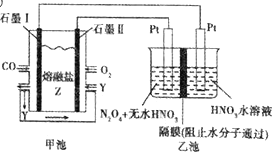
A. 若甲池消耗标准状况下的氧气2.24L,则乙池中产生氢气0.2mol
B. 石墨I是原电池的负极,发生氧化反应
C. 乙池中左端Pt极电极反应式:N2O4-2e-+2H2O===2N2O5+4H+
D. 甲池中的CO32-向石墨I极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为Fe3++Cr2+![]() Fe2++Cr3+。下列说法正确的是
Fe2++Cr3+。下列说法正确的是

A. 电池充电时,b极的电极反应式为Cr3++e-=Cr2+
B. 电池充电时,Cl-从a极穿过选择性透过膜移向b极
C. 电池放电时,a极的电极反应式为Fe3++3e-=Fe
D. 电池放电时,电路中每通过0. 1 mol电子,Fe3+浓度降低0. 1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示的一些物质或概念间的从属关系中正确的是

X | Y | Z | |
A | 过氧化钠 | 碱性氧化物 | 氧化物 |
B | 硫酸 | 化合物 | 电解质 |
C | 淀粉溶液 | 胶体 | 分散系 |
D | 置换反应 | 氧化还原反应 | 离子反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一混合物的水溶液,只可能含以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、 NH4+、Cl-、CO32-、SO42-,现取三份100 mL溶液进行如下实验:① 第一份加入AgNO3溶液有沉淀产生,② 第二份加过量NaOH溶液加热后收集到气体0.02 mol,无沉淀生成,同时得到溶液甲,③ 在甲溶液中通过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02 g,④ 第三份加足量BaCl2溶液后得白色沉淀,沉淀经足量盐酸洗涤干燥后质量为11.65 g。根据上述实验回答:
(1)一定不存在的离子是____________________,不能确定是否存在的离子是________________
(2)试确定溶液中肯定存在的阴离子及其浓度(可不填满):离子符号____________,浓度____________________
(3)试确定K+ 是否存在________ (填“是”或“否”),判断的理由是:____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com