
【题目】现以CO、O2、熔融盐Z(Na2CO3)组成的燃料电池,采用电解法处理CO同时制备N2O5,装置如图所示,其中Y为CO2。下列说法不合理的是
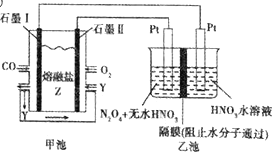
A. 若甲池消耗标准状况下的氧气2.24L,则乙池中产生氢气0.2mol
B. 石墨I是原电池的负极,发生氧化反应
C. 乙池中左端Pt极电极反应式:N2O4-2e-+2H2O===2N2O5+4H+
D. 甲池中的CO32-向石墨I极移动
【答案】C
【解析】
根据装置图,甲池为燃料电池,乙池为电解池,通CO一极为负极,电极反应式为CO-2e-+O2-=CO2,通O2一极为正极,电极反应式为O2+4e-=2O2-,乙池左端Pt连接电源的正极,即左端Pt为阳极,电极反应式为N2O4+2HNO3-2e-=2N2O5+2H+,乙池右端Pt为阴极,电极反应式为2H++2e-=H2↑;
根据装置图,甲池为燃料电池,乙池为电解池,通CO一极为负极,电极反应式为CO-2e-+O2-=CO2,通O2一极为正极,电极反应式为O2+4e-=2O2-,乙池左端Pt连接电源的正极,即左端Pt为阳极,电极反应式为N2O4+2HNO3-2e-=2N2O5+2H+,乙池右端Pt为阴极,电极反应式为2H++2e-=H2↑;
A、根据上述分析,根据转移电子物质的量相等,建立关系为O2~4e-~2H2,消耗氧气的物质的量为2.24L/22.4L·mol-1=0.1mol,则产生氢气的物质的量为0.1mol×2=0.2mol,故A说法正确;
B、根据上述分析,石墨I是原电池的负极,根据原电池工作原理,负极上发生氧化反应,故B说法正确;
C、乙池中左端Pt极电极反应式为N2O4+2HNO3-2e-=2N2O5+2H+,故C说法错误;
D、根据原电池工作原理,甲池中CO32-向石墨I极移动,故D说法正确;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列鉴别方法不可行的是
A.用水鉴别乙醇、苯和溴苯B.用溴水鉴别己烯、苯和四氯化碳
C.用酸性高锰酸钾溶液鉴别苯、乙醇和戊烷D.用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是聚合物胶黏剂、涂料等的单体,其一条合成路线如下(部分试剂及反应条件省略):

完成下列填空:
(1)反应①的反应类型是____________。反应④的反应条件是_____________。
(2)除催化氧化法外,由A得到![]() 所需试剂为___________。
所需试剂为___________。
(3)已知B能发生银镜反应。由反应②、反应③说明:在该条件下,_______________。
(4)写出结构简式,C________________ D________________
(5)D与1-丁醇反应的产物与氯乙烯共聚可提高聚合物性能,写出该共聚物的结构简式。_____________
(6)写出一种满足下列条件的丁醛的同分异构体的结构简式。____________
①不含羰基 ②含有3种不同化学环境的氢原子
已知:双键碳上连有羟基的结构不稳定。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
下列说法不正确的是

A. 固体1中主要含有Ca(OH)2、CaCO3、CaSO3
B. X可以是空气,且需过量
C. 捕获剂所捕获的气体主要是CO
D. 处理含NH4+废水时,发生反应的离子方程式为:NH4++NO2-==N2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)广泛存在于食品中,人们对其及相关产品进行了深入研究。
(1)H2C2O4 (s) ![]() H2O(g)+CO(g)+CO2(g) △H=+340kJ·mol-1,写出此反应的平衡常数表达式 K= ;密闭容器中,保持温度不变,下列有关选项正确的是( )
H2O(g)+CO(g)+CO2(g) △H=+340kJ·mol-1,写出此反应的平衡常数表达式 K= ;密闭容器中,保持温度不变,下列有关选项正确的是( )
A.恒容时,容器的压强不再变化,说明该反应已达到化学平衡状态
B.恒压时,容器的体积不再变化,说明该反应已达到化学平衡状态
C.气体摩尔体积不再发生变化,说明该反应已达到化学平衡状态
D.气体平均摩尔质量不再发生变化,说明该反应已达到化学平衡状态
(2)草酸分解所需燃料可以是CO,通过甲烷制备CO:
CH4(g)+CO2(g) 2CO(g)+2H2(g) △H >O。常温下,在2 L的密闭容器中通入4 mol CH4气体和6 mol CO2气体发生反应,5min后达到平衡,测得CO气体的浓度为0.1 mol·L-1。
①平衡时,该反应的平均反应速率v(CO2)= mol·L-1min-1。
②在不改变反应混合物用量的前提下,为了提高CH4气体的转化率,可采取的措施是 。
(3)电解饱和草酸溶液可以制得高档香料乙醛酸(H2C2O3),装置如下图1所示,写出复合膜电极的电极反应式 。

(4)在K3Fe(C2O4)3溶液中存在:[Fe(C2O4)3]3-Fe3++3C2O42-,常温下,该溶液中
[Fe(C2O4)3]3-的浓度与温度的关系如上图2所示,则A点的c(Fe3+) B点的c(Fe3+) (填“<”“>”或“=”);草酸是一种温和的还原剂,其他条件不变,向K3Fe(C2O4)3溶液中加入少量KMnO4固体,Fe3+的浓度 (填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苏轼的《格物粗谈》中记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”这里的“气”是指( )
A.甲烷B.乙烯C.氧气D.二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84”消毒液(有效成分为NaClO)可用于消毒和漂白,下列实验现象的分析,不正确的是 ( )
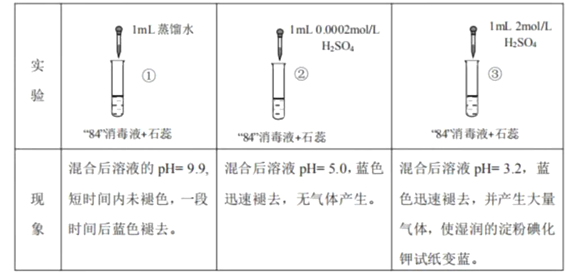
A. 对比实验①和②,②中蓝色迅速褪去的原因是发生了反应ClO+H+ ===HClO
B. 实验③中产生的气体是Cl2,由HClO分解得到:2HClO===Cl2↑+H2O
C. 对比实验②和③,溶液的pH可能会影响ClO 的氧化性或Cl 的还原性
D. 加酸可以提高“84”消毒液的漂白效果,但需要调控合适的pH才能安全使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
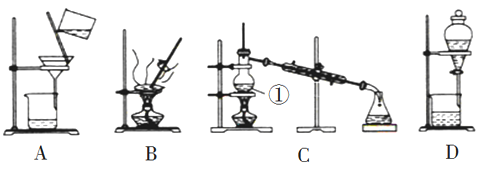
(1)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是__________装置B中玻璃棒不断搅拌,其作用是_________
(2)从氯化钠溶液中得到氯化钠固体,选择装置__________(填代表装置图的字母)。
(3)装置C中①的名称是__________,①中加入沸石的作用是_________,冷却水的方向是_____________________
(4)已知:在常温下,苯(C6H6)为一种无色、透明的液体,密度为 0.8786 g/cm3, 毒性较高,易挥发,易燃,有腐蚀性,沸点为 80.1℃,难溶于水,易溶于有机溶剂,可作为有机溶剂;碘(I2)为紫黑色晶体,易升华,易凝华,熔点 113.5℃,沸点 184.3℃,加热时碘升华为紫色蒸气,冷却后凝华成紫黑色固体.实验室常用苯来提取碘水中的碘,然后分液,最后蒸馏碘的苯溶液,得到单质碘。 其中采用装置C蒸馏碘的苯溶液时常用水浴加热装置C中仪器①,你认为不直接加热的原因是_______;同时锥形瓶置于盛有冰水的烧杯中,你认为其目的是________
(5)海带中含有丰富的碘,为了从海带中提取碘,第一步是灼烧海带,此操作除需要三脚架外,还需要用到下列的实验仪器是____________
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.镊子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com