
����Ŀ����84������Һ����Ч�ɷ�ΪNaClO��������������Ư�ף�����ʵ������ķ���������ȷ���� ( )
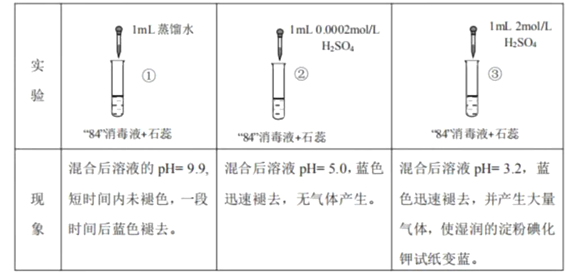
A. �Ա�ʵ��ٺ͢ڣ�������ɫѸ����ȥ��ԭ���Ƿ����˷�ӦClO+H+ ===HClO
B. ʵ����в�����������Cl2����HClO�ֽ�õ���2HClO===Cl2��+H2O
C. �Ա�ʵ��ںۣ͢���Һ��pH���ܻ�Ӱ��ClO �������Ի�Cl �Ļ�ԭ��
D. ���������ߡ�84������Һ��Ư��Ч��������Ҫ���غ��ʵ�pH���ܰ�ȫʹ��
���𰸡�B
��������
A. ���������Ư���ԣ�
B. ��������ʹʪ��ĵ��۵⻯����ֽ����������Ϊ�����������������£�������������������ӷ������з�Ӧ���ã�
C. �Ա�ʵ��ںۣ͢���Һ��������ǿ��������������
D. ͨ���Ա�����ʵ�飬�ɿ����ʵ���pH��������84������Һ��Ư��Ч����
A. �Ա�ʵ��ٺ͢ڣ�������ɫѸ����ȥ��Ҫ����Ϊ�����������Һ�еĴ���������ӷ�Ӧ�����˾���Ư���ԵĴ����ᣬ�����ӷ���ʽΪ��ClO +H+ = HClO����A����ȷ��
B. ��84������Һ����Ҫ�ɷ�Ϊ�Ȼ�����������ƣ�ʵ����в�������ʹʪ��ĵ��۵⻯����ֽ������������Cl2����Ҫ����Ϊ�����������·��������߷������з�Ӧ�������ӷ�Ӧ����ʽΪ��ClO +2H++ Cl = Cl2��+H2O����B�����
C. ��Һ��pHֵ��С������£������˴������壬ʹ�������������������ӷ���������ԭ��Ӧ������������˵����Һ��pH���ܻ�Ӱ��ClO �������Ի�Cl �Ļ�ԭ�ԣ���C����ȷ��
D. �Ա�����ʵ����Կ�����������������84������Һ��Ư��Ч����������̫��ʹ��Һ�в��������ж�������������Ҫ���غ��ʵ�pH���ܰ�ȫʹ�ã���D����ȷ��
��ѡB��


 ��ѧȫ��������ѵ��ϵ�д�
��ѧȫ��������ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ����������һ�����ҵ�ʯ�ͻ�ѧ��ҵ��չˮƽ�ı�־�� ( )
A.ʯ�Ͳ���B.�ϳ���ά�IJ���C.��ϩ�IJ���D.����IJ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������CO��O2��������Z(Na2CO3)��ɵ�ȼ�ϵ�أ����õ�ⷨ����COͬʱ�Ʊ�N2O5��װ����ͼ��ʾ������YΪCO2������˵������������
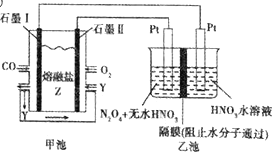
A. ���׳����ı�״���µ�����2.24L�����ҳ��в�������0.2mol
B. ʯīI��ԭ��صĸ���������������Ӧ
C. �ҳ������Pt���缫��Ӧʽ��N2O4��2e��+2H2O===2N2O5+4H+
D. �׳��е�CO32����ʯīI���ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(����)
A. ����ӵ����������������У��뽫�������ĸ����豸��ֱ����Դ�ĸ�������
B. ��ӦH2S(g)��ZnO(s)===H2O(g)��ZnS(s)��һ�������¿��Է����У��Ҧ�S<0����H>0
C. ���³�ѹ������ȼ�ϵ�ع�������2.24 L O2ʱ��ת�Ƶ��ӵ���ĿΪ0.4��6.02��1023
D. �����£�Ksp[Cu(OH)2]��2.6��10��19��pH��10�ĺ�Cu2������Һ�У�c(Cu2��)��2.6��10��11mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��һЩ���ʻ�����Ĵ�����ϵ����ȷ����

X | Y | Z | |
A | �������� | ���������� | ������ |
B | ���� | ������ | ����� |
C | ������Һ | ���� | ��ɢϵ |
D | �û���Ӧ | ������ԭ��Ӧ | ���ӷ�Ӧ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ2.3g������Ͷ�뵽100gˮ�У�������Һ���ܶ�Ϊ1.022g/cm3��
��1��д������ˮ��Ӧ�Ļ�ѧ����ʽ���������ת�Ƶķ������Ŀ��_________��
��2���÷�Ӧ�Ļ�ԭ����____________����ԭ������______________��
��3����Ӧ������������ڱ�״���µ������������Һ�����ʵ���Ũ�ȡ�______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ʊ������������һ����Ҫ���ʡ����������Ĺ̵���Ӧ[��N2(g)+3H2(g)![]() 2NH3(g)�͢�N2(g)+O2(g)
2NH3(g)�͢�N2(g)+O2(g)![]() 2NO(g)]����ƽ�ⳣ������ֵ(lg K)���¶ȵĹ�ϵ����ͼ������ͼ�е������ж�����˵����ȷ����
2NO(g)]����ƽ�ⳣ������ֵ(lg K)���¶ȵĹ�ϵ����ͼ������ͼ�е������ж�����˵����ȷ����

A. ��Ӧ�ٺ͢ھ�Ϊ���ȷ�Ӧ
B. �����¶ȣ���Ӧ�ٵķ�Ӧ���ʼ�С
C. �ڳ����£����÷�Ӧ�ٹ̵������÷�Ӧ�ڹ̵�����Ӧ�̶����ܴ�
D. ��1 000 ��ʱ����Ӧ�ٺͷ�Ӧ����ϵ��N2��Ũ��һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ͼ�ǽ���þ��±�ص���(X2)��Ӧ�������仯ʾ��ͼ��
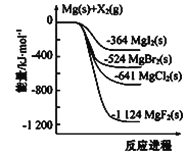
д��MgBr2(s)��Cl2(g)����MgCl��s����Br2��l�����Ȼ�ѧ����ʽ______________________________��
��2���״�ȼ�ϵ�أ��ṹ��ͼ�������ӽ���Ĥ�����������Һ��Ϊ1L2mol��L-1H2SO4��Һ�����������2mol e-����ת��ʱ������������Һ������֮��Ϊ______g�����跴Ӧ��ľ�������������ܽ⣩��

��3��250mLK2SO4��CuSO4�Ļ����Һ��c(SO42-)��0. 5mol��L��1����ʯī���缫������Һ����ͨ��һ��ʱ����������ռ���1.12L���壨��״���£����ٶ�������Һ�����Ϊ250mL��д�������缫��Ӧʽ______________ԭ�����Һ��c(K��)��__________________
��4��NaHSO3��Һ�ڲ�ͬ�¶��¾��ɱ�����![]() KIO3��������Ũ�Ⱦ�Ϊ0.020mol/L
KIO3��������Ũ�Ⱦ�Ϊ0.020mol/L![]() NaHSO3��Һ�����������ۣ�10ml
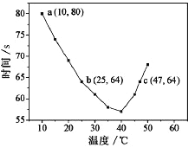
NaHSO3��Һ�����������ۣ�10ml![]() ��KIO3(����)������Һ90.0ml��ϣ���¼10��55�����Һ����ʱ�䣬ʵ������ͼ����ͼ������ͼ��a���Ӧ��
��KIO3(����)������Һ90.0ml��ϣ���¼10��55�����Һ����ʱ�䣬ʵ������ͼ����ͼ������ͼ��a���Ӧ��![]() NaHSO3��Ӧ����Ϊ________________
NaHSO3��Ӧ����Ϊ________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ֲ���纣���������к��зḻ�ĵ�Ԫ�أ���Ԫ���Ե����ӵ���ʽ���ڣ�ʵ������Ӻ�������ȡ��Ĺ������£�
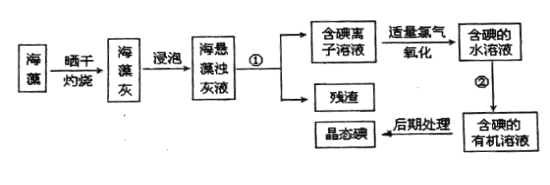
����д���пհף�
��1�����պ���ʱ������Ҫ���ż�.�������⣬����Ҫ�õ���ʵ��������________________����������������ѡ��������������ñ����ĸ��д�ڿհ״�����
A.�ձ� B.������ C.������ D.������ E.�ƾ��� F.����ǯ
��2��ָ����ȡ��Ĺ������йص�ʵ��������ƣ���________����________
��3����ȡ��Ĺ��̢��У�ͨ����________________���������ƣ��н��У����õ����Ǻ�������Ȼ�̼��Һ�����ú�ֲ㣬�²�Ϊ________________ɫ��
��4�����������������ӷ���ʽ��ʾ__________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com