
����Ŀ������ֲ���纣���������к��зḻ�ĵ�Ԫ�أ���Ԫ���Ե����ӵ���ʽ���ڣ�ʵ������Ӻ�������ȡ��Ĺ������£�
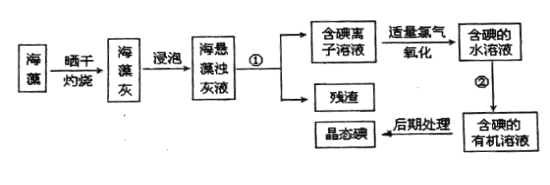
����д���пհף�
��1�����պ���ʱ������Ҫ���ż�.�������⣬����Ҫ�õ���ʵ��������________________����������������ѡ��������������ñ����ĸ��д�ڿհ״�����
A.�ձ� B.������ C.������ D.������ E.�ƾ��� F.����ǯ
��2��ָ����ȡ��Ĺ������йص�ʵ��������ƣ���________����________
��3����ȡ��Ĺ��̢��У�ͨ����________________���������ƣ��н��У����õ����Ǻ�������Ȼ�̼��Һ�����ú�ֲ㣬�²�Ϊ________________ɫ��
��4�����������������ӷ���ʽ��ʾ__________________________��
���𰸡�BDEF ���� ��ȡ ��Һ©�� �Ϻ� 2I- +Cl2=2Cl- +I2
��������
���������������յõ�����ң�������ˮ���ݵõ�����Һ�����˵õ��������ӵ���Һ��ͨ����������������Ϊ�ⵥ�ʣ�������ȡ����Һ�õ����ⵥ�ʵ��л���Һ������õ��ⵥ�ʣ�
��1�����չ�������һ��ʹ��(��)��������������ȡ��������ǯ������������Ҫ�������� ֧��Ȼ��������ż��ϣ����ż�����Ŀռ�žƾ��ƣ�
�ʴ�Ϊ��BDEF��
��2���ٷ�������Һ���ù��ˣ��ڽ��ⵥ�ʴ�ˮ��Һ����ȡ������Ӧ���õⵥ�����л��ܼ��е��ܽ�ȱ���ˮ�е��ܽ�ȴ���ص���ʵ�֣������л��ܼ����ⵥ�ʴ�ˮ��Һ����ȡ������
�ʴ�Ϊ�����ˣ���ȡ��
��3����ȡ���õ���Ҫ�����Ƿ�Һ©�������Ȼ�̼���ܶȴ���ˮ������ȡ���²��ǵ�����Ȼ�̼��Һ�����Ϻ�ɫ��
��Ϊ����Һ©�����Ϻ죻
��4��������ʹ����������Һ�еĵ���������Ϊ�ⵥ�ʣ����ӷ���ʽΪ��2I- +Cl2=2Cl- +I2��
����2I- +Cl2=2Cl- +I2��


 ���б�ˢ��ϵ�д�
���б�ˢ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����84������Һ����Ч�ɷ�ΪNaClO��������������Ư�ף�����ʵ������ķ���������ȷ���� ( )
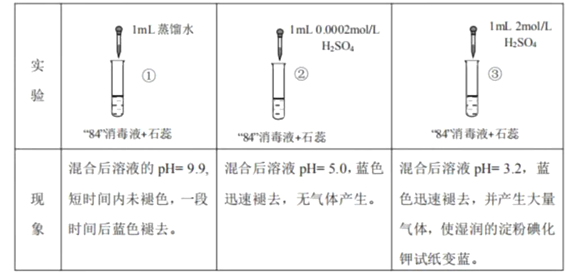
A. �Ա�ʵ��ٺ͢ڣ�������ɫѸ����ȥ��ԭ���Ƿ����˷�ӦClO+H+ ===HClO
B. ʵ����в�����������Cl2����HClO�ֽ�õ���2HClO===Cl2��+H2O
C. �Ա�ʵ��ںۣ͢���Һ��pH���ܻ�Ӱ��ClO �������Ի�Cl �Ļ�ԭ��
D. ���������ߡ�84������Һ��Ư��Ч��������Ҫ���غ��ʵ�pH���ܰ�ȫʹ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ�ã������װ�ûش����⣺
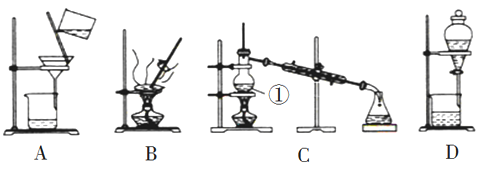
��1����װ��A��װ��B�ж��õ���������װ��A�в�������������__________װ��B�в��������Ͻ��裬��������_________
��2�����Ȼ�����Һ�еõ��Ȼ��ƹ��壬ѡ��װ��__________�������װ��ͼ����ĸ����
��3��װ��C�Тٵ�������__________�����м����ʯ��������_________����ȴˮ�ķ�����_____________________
��4����֪���ڳ����£�����C6H6��Ϊһ����ɫ������Һ�壬�ܶ�Ϊ 0.8786 g/cm3�� ���Խϸߣ��ӷ�����ȼ���и�ʴ�ԣ��е�Ϊ 80.1�棬������ˮ���������л��ܼ�������Ϊ�л��ܼ����⣨I2��Ϊ�Ϻ�ɫ���壬�����������������۵� 113.5�棬�е� 184.3�棬����ʱ������Ϊ��ɫ��������ȴ���������Ϻ�ɫ���壮ʵ���ҳ��ñ�����ȡ��ˮ�еĵ⣬Ȼ���Һ����������ı���Һ���õ����ʵ⡣ ���в���װ��C�����ı���Һʱ����ˮԡ����װ��C�������٣�����Ϊ��ֱ�Ӽ��ȵ�ԭ����_______��ͬʱ��ƿ����ʢ�б�ˮ���ձ��У�����Ϊ��Ŀ����________
��5�������к��зḻ�ĵ⣬Ϊ�˴Ӻ�������ȡ�⣬��һ�������պ������˲�������Ҫ���ż��⣬����Ҫ�õ����е�ʵ��������____________
A���ձ� B������ C�������� D�������� E���ƾ��� F������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̼����( Na2CO4)��һ�ֺܺõĹ�����������ϡ���ᷴӦ�Ļ�ѧ����ʽΪ��2Na2CO4+4HCl=4NaCl+2CO2 +O2+2H2O.���۹�̼����һ�㶼����̼���ƣ�Ϊ�ⶨij��̼������Ʒ(ֻ��Na2CO4��Na2CO3)�Ĵ��ȣ�ij��ѧ��ȤС������������ַ���ʵʩ��
����һ��![]()
��1�����������������Ʒֱ�Ϊ
��2�����������У�ʹ�õ����������� __(��������)��
��3��������������IJ�������
������������ͼ��װ��ʵ��װ�ã�QΪһ��������������ȡ������Ʒ�����У���Һ©����������ϡ�����������������ַ�Ӧ��

��4��Ϊ�ⶨ��Ӧ������������������ϡ����ǰ����ر� ���� (����K1������K2������K3��)������a�������� ��
��5����������Ӧֹͣ��ʹK1��K3���ڹر�״̬��K2���ڴ�״̬���ٻ�����Kl�� B��װ�Ĺ����Լ��� ��Ϊ��Ҫ������K1�� ��
��6��ʵ�����ʱ����ͲI����xmLˮ����Ͳ�����ռ�����ymL���壬����Ʒ�й�̼���Ƶ����������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��д����ͼ��������������������ƣ�

��___________����___________�� ��___________�� ��___________��
��2�������������У�ʹ��ʱ�������Ƿ�©ˮ����__________����������ţ���
��3����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص�Ũ�����Լ���ǩ�ϵIJ������ݡ����ø�Ũ��������480 mL 1 mol��L��l��ϡ���ᡣ

�ɹ�ѡ�õ������У� ����ͷ�ιܣ�����ƿ�����ձ�����ҩ�ף�����Ͳ����������ƽ��
��ش��������⣺
������ϡ����ʱ����ȱ�ٵ�������__________��__________��д�������ƣ���
�������㣬����480 mL l mol��L��l��ϡ������Ҫ����Ͳ��ȡ����Ũ��������Ϊ________mL������ȡ�õ�Ũ���Ỻ��ע�뵽ʢˮ���ձ�������Ͳ�ﻹ������Ũ���ᣬ���������ˮϴ�Ӻ�һ����ϴ��Һע���ձ�����ʹ���Ũ��______������ƫ������ƫ����������Ӱ��������
����ת������ƿǰ�ձ���Һ��Ӧ_______�������ʹ���Ũ��____������ƫ������ƫ����������Ӱ��������
������ʱ����ʹ��Һ�İ�Һ����̶�����ƽ�������ӻ�ʹŨ��______��������ƫ������ƫ����������Ӱ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ж�HA���������(����)��������
A. Ũ����ȵ�HCl��HA����Һ���Ƚ�c(H��) ��HClԼ��HA��100��
B. pH��ȵ�HCl��HA����Һ��c(HA)Լ��c(HCl)��100��
C. Ũ����ȵ�HCl��HA����Һ�����ͬʱ����þ��Ӧ��������HA��HCl��
D. pH��ȵ�HCl��HA����Һ�����ͬʱ����þ��Ӧ��������HA��HCl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A. �ڱ�״���£�11.2Lij���������Ϊ22g������������Է���������44g/mol
B. 16gO2��16gO3������ԭ�Ӹ���һ����
C. �ڱ�״���£�ˮ�������͵������Ӽ��ƽ���������
D. �ڱ�״���£�1molSO3�����ԼΪ22.4L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������(Ni2O3)������������ܵ��Ԫ������ⷨ�Ʊ��������£���NaOH��Һ��NiCl2��Һ��pH����7.5���������������ƹ�������е�⡣�������в�����Cl2������������������ClO-���Ѷ�����(�ɼ�д��Ni2+)����ΪNi3+���ٽ�Ni3+��һϵ�з�Ӧ��ת��ΪNi2O3�����װ����ͼ��ʾ������˵������ȷ����(����)

A. �������������Ƶ���������������Ũ�ȣ���ǿ��Һ�ĵ�������
B. ������������������Һ��pH����
C. �������У���Һ�е�Cl-�������ӽ���Ĥ�������ƶ�
D. ClO-����Ni2+�����ӷ���ʽΪ��ClO-+H2O+2Ni2+=Cl-+2Ni3++2OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������ȷ���ǣ� ��
A. ���������� B. ϡ��Ũ����
B. ϡ��Ũ����
C. ���˲��� D. �ⶨ��ҺpH
D. �ⶨ��ҺpH
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com