
【题目】下列说法正确的是
A. 34 g H2O2中含原子总数为4NA
B. 2.4g金属镁变成镁离子时得到的电子数目为0.2NA
C. 若气体的摩尔体积为22.4 L/mol,则所处条件一定为标准状况
D. 摩尔是用来衡量微观粒子多少的一种物理量
科目:高中化学 来源: 题型:
【题目】有关物质燃烧时火焰颜色描述错误的是 ( )
A.氢气在氯气中燃烧——苍白色B.钠在空气中燃烧——黄色
C.乙醇在空气中燃烧——淡蓝色D.硫在氧气中燃烧——绿色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标出下列氧化还原反应过程中有关变化
(1)用单线桥标出电子的转移方向和数目 ,其中氧化剂是 .
NO+N O2+2NaOH═2NaN O2+H2O
(2)用双线桥标出化合价的变化,其中还原剂与氧化剂的物质的量比值是 .
2MnO4﹣+8H++5S O2═2Mn2++5SO42﹣+4H2O.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火星探测器发回的信息表明,火星上存在针铁矿〔Goethite,化学式:FeO(OH)〕和黄钾铁矾(Jarosite),从而证明火星表面曾经存在过水.这一发现被《人民日报》等媒体评为2004世界十大新闻之首.已知两种矿物中铁的价态相同,则黄钾铁矾〔化学式记为:KFe3(SO4)2(OH)n〕中n值为
A. 4 B. 5 C. 6 D. 7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究氮、磷等单质及其化合物的反应有重要意义.
(1)试判断用于汽车净化的一个反应2NO(g)+2CO(g)═N2(g)+2CO2(g),在298K、100kPa下能否自发进行(填“能”或“否”).已知:在298K、100kPa下该反应的△H=﹣113.0kJmol﹣1 , △S=﹣145.3Jmol﹣1K﹣1 .
(2)25℃下,将a molL﹣1的氨水与0.005molL﹣1的硫酸等体积混合,反应平衡时溶液中c(NH4+)=2c(SO42﹣),用含a的代数式表示NH3H2O的电离常数Kb= .
(3)25℃时,Ksp(BaSO4)=1.1×10﹣10 , Ksp(BaCO3)=2.6×10﹣9 , 现将BaCl2溶液滴入浓度均为0.01molL﹣1的Na2SO4和Na2CO3的混合溶液中,当两种沉淀共存时,溶液中c (CO32﹣):c(SO42﹣)=(不考虑CO32﹣的水解)
(4)次磷酸(H3PO2)是一种一元中强酸,重要的精细化工产品.
①写出次磷酸的电离方程式: .
②已知某温度下0.01mol/L的NaOH溶液pH=10,将该NaOH溶液与等浓度等体积的H3PO2溶液混合,混合后溶液pH=7,则此时c(OH﹣)﹣c(H3PO2)= . 该温度下将pH=a的盐酸Vaml与pH=b的氢氧化钠Vbml混合后溶液呈中性,且a+b=10,则Va:Vb= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将废旧锌锰电池处理得到含锰混合物,既能减少它对环境的污染,又能实现废电池的资源化利用.
(1)回收二氯化锰:将废旧锌锰电很处理,得到含锰混合物,向该混合物加入浓盐酸并加热.
写出MnO(OH)与浓盐酸反应的化学方程式: .
(2)锰回收新方法:向含锰混合物加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止,其主要反应为:2MnOOH+MnO2+2H2C2O4+3H2SO4=3MnSO4+4CO2↑+6H2O
①与使用浓盐酸回收锰相比,新方法的优点是 (答1点即可).
②欲以MnSO4溶液为原料制备MnCO3 , 选用的加料方式 (填字母),原因是 . 己知:Ksp(MnCO3)=2.3×10﹣11、Ksp[Mn(OH)2]=2.1×10﹣13
A.将MnSO4溶液与Na2CO3溶液同时加入到反应容器中
B.将MnSO4溶液缓慢加入到盛有Na2CO3溶掖的反应容器中
C.将Na2CO3溶液缓慢加入到盛有MnSO4溶液的反应容器中
D.以上三种方式都无法得到MnCO3
(3)现以含锰混合物为原料制备锰锌铁氧体的主耍流程如图l 所示:
回答下列问题:
①MnxZn1﹣xFe2O4中铁元素化合价为 ,则锰元素的化合价为 .
②活性铁粉除汞时,铁粉的作用是 (填“氧化剂”或“还原剂”).
③酸浸时,MnO2与H2SO4、H2O2反应的离子方程式为 .
④除汞是以氮气为载气吹入滤液中,带出汞蒸气经KMnO4溶液进行吸收而实现的.在恒温下不同pH时,KMnO4溶液对飞的单位时间去除率及主要产物如图2 所示:
a.写出pH=10时KMnO4溶液吸收汞蒸气的离子方程式 ,
b.在强酸性环境中汞的单位时间去除率高,其原因除氢离子浓度增大使KMnO4溶液的氧化性增强外,还可能是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1) Fe(OH)2很不稳定,露置在空气中容易被氧化,Fe(OH)2被氧化的化学方程式为:______________________________ ,用硫酸亚铁晶体配制FeSO4溶液时你觉得还需加入少量的____________,防止FeSO4被氧化。
(2) 向FeCl3溶液中滴加KSCN溶液,溶液呈____色。
(3) 某气态氧化物化学式为RO2,在标准状况下,0.92g该氧化物的体积是448mL,则氧化物的相对分子质量为_________,R的摩尔质量为_______。
(4) 48g SO42-中含有的电子数为_________。
(5) NaClO2+4HCl(浓) ![]() NaCl+2Cl2↑+2H2O,此反应的氧化产物与还原产物的物质的量之比是____________,生成标准状况下4.48 L Cl2时,转移的电子数为_______。
NaCl+2Cl2↑+2H2O,此反应的氧化产物与还原产物的物质的量之比是____________,生成标准状况下4.48 L Cl2时,转移的电子数为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校研究性学习小组用已部分生锈(Fe2O3)的废铁屑,制作印刷电路板的腐蚀剂,即FeCl3溶液。实验操作过程如下:
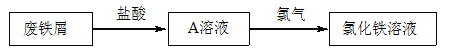
根据要求回答问题:
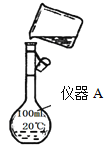
(1)用浓盐酸配制250mL 0.2molL-1稀盐酸,右图是某同学转移溶液的示意图,写出仪器 A的名称: 。
(2)图中有两处错误分别是 , 。
(3)废铁屑用盐酸处理后,还含有不溶性杂质,为获取澄清的A溶液,进行物质分离的操作名称是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com