
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
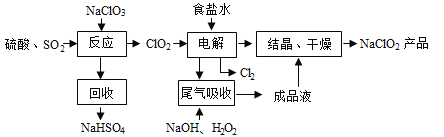
回答下列问题:
(1)NaClO2中Cl的化合价为_______。
(2)写出“反应”步骤中生成ClO2的化学方程式___________________。
(3)“电解”中阴极反应的主要产物是____________。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应中,氧化剂与还原剂的物质的量之比为______________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为________________。(计算结果保留两位小数)
【答案】(1)+3 (2)2NaClO3+SO2+H2SO4=2NaHSO4+ClO2↑
(3)NaClO2 (4)2:1 (5)1.57g
【解析】
试题分析:(1)在NaClO2中Na为+1价,O为-2价,根据正负化合价的代数和为0,可得Cl的化合价为+3价。
(2)NaClO3和SO2在H2SO4酸化条件下生成ClO2,其中NaClO2是氧化剂,还原产物为NaCl,根据电子守恒和原子守恒,此反应的化学方程式为2NaClO3+SO2+H2SO4=2NaHSO4+ClO2↑。
(3)食盐溶液中混有Mg2+和Ca2+,可利用过量NaOH溶液除去Mg2+,利用过量Na2CO3溶液除去Ca2+,向NaCl溶液加入ClO2,进行电解,阳极发生反应2Cl--2e-=Cl2↑,反应产生Cl2, 阴极发生反应产生NaClO2,可见“电解”中阴极反应的主要产物是NaClO2;
(4)根据图示可知,利用含有过氧化氢的NaOH溶液吸收ClO2气体,产物为NaClO2,则此吸收反应中,氧化剂为ClO2,还原产物为NaClO2,还原剂是H2O2,氧化产物是O2,每1mol的H2O2转移2mol电子,反应方程式是:2NaOH+2ClO2+H2O2=2NaClO2+O2+2H2O,氧化剂和还原剂的物质的量之比为2:1.
(5)每1克NaClO2的物质的量为n(NaClO2)=1g÷90.5g/mol=1/90.5mol,1/90.5mol获得电子的物质的量是n(e-)=1/90.5mol×4=4/90.5 mol,1molCl2获得电子的物质的量是2mol,根据电子转移数目相等,可知其相对于氯气的物质的量为n=1/90.5mol×4÷2=2/90.5mol,则氯气的质量为2/90.5mol× 71g/mol =1.57g,即NaClO2的有效氯含量为1.57g


科目:高中化学 来源: 题型:
【题目】将NaOH溶液与CuSO4溶液加入某病人的尿液中,微热时如果观察到红色沉淀,则说明该病人的尿液中含有
A.乙酸 B.乙醇 C.氯化钠 D.葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修5:有机化学基础】
污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。

请回答下列问题:
(1)上述流程中多次设计到过滤操作,实验室进行过滤操作时需要用到的硅酸盐仪器有玻璃棒、烧杯,_______________;其中玻璃棒的作用是___________________。
(2)用MnCO3能除去溶液中的Al3+和Fe3+,其原理是_____________(只用文字表述)
(3)工业上采用电解K2MnO4水溶液的方法来生产KMnO4,其中惰性电极作阳极,铁作阴极,请写出阳极的电极反应式__________________。
(4)下列各组试剂中,能准确测定一定体积燃煤尾气中SO2含量的是__________。(填编号)
a.NaOH溶液、酚酞试液 b.稀H2SO4酸化的KMnO4溶液
c.碘水、淀粉溶液 d.氨水、酚酞试液
(5)废气中SO2与稀硫酸酸化的软锰矿反应的化学方程式为_______________;已知废气中SO2浓度为6.4g/m3,软锰矿浆对SO2的吸收率可达90%,则处理1000m3燃煤尾气,可得到硫酸锰晶体(MnSO4·H2O,相对分子质量为169)质量为_________________kg(结果保留3 位有效致字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示的N2(g)和O2(g)反应生成NO(g)过程中的能量变化情况,判断下列说法正确的是
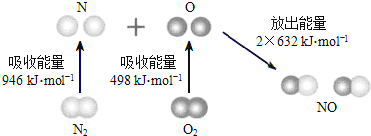
A.N2(g)与O2(g)反应生成NO(g)是放热反应
B.2molO原子结合生成O2(g)时需要放出498kJ能量
C.1molNO(g)分子中的化学键断裂时需要放出632kJ能量
D.N2(g)+O2(g)=2NO(g)△H=+1444kJ/mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】各电子层排布电子的总数遵循以下规则:①每层最多容纳2n2个电子;②原子最外层电子数≤8;③原子次外层电子数≤18。决定这3条规律的电子排布规则是( )。
A. 能量最低原则
B. 泡利不相容原理
C. 洪特规则
D. 能量最低原则和泡利不相容原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Al2O3为原料制取氢氧化铝,最好的方法是( )
A.将Al2O3溶于水
B.将Al2O3先溶于盐酸中,之后滴加氢氧化钠溶液
C.将Al2O3先溶于盐酸中,之后滴加氨水
D.将Al2O3先溶于NaOH溶液中,之后滴加盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用 X 射线对 BaSO4 穿透能力较差的特性,医学上在进行消化系统的 X 射线透视时,常用 BaSO4 作内服造影剂,这种检查手段称为钡餐透视.
(1)医学上进行钡餐透视时为什么不用 BaCO3?(用离子方程式表示)________________________________
(2)某课外活动小组为了探究 BaSO4 的溶解度,分别将足量 BaSO4 放入a.5mL 水 ;b.40mL 0.2molL-1Ba(OH)2 溶 液 c.20mL 0.5molL-1Na2SO4 溶 液 d.40mL 0.1molL-1H2SO4溶液中,溶解至饱和。
①以上各溶液中,Ba2+的浓度由大到小的顺序为_______________________________
A.b>a>c>d B.b>a>d>c C.a>d>c>b D.a>b>d>c
②已知 25℃时,Kap=1.1×10-10,上述条件下,溶液 b 中的 SO42-浓度为_________________molL-1,溶解 c中 Ba2+的浓度为_________________molL-1
③某同学取同体积的溶液 b 和溶液 d④直接混合,则混合液的 pH 为_________________(设混合溶液的体积为混合前两溶液的体积之和)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一瓶无色澄清的溶液,可能由以下离子中的几种组成:Na+、K+、NH4+、Fe2+、SO42-、I-、CO32-、Cl-、SO32-、MnO4-,请根据以下实验步骤及现象回答问题:
步骤一:取适量待测液,加入NaOH溶液并加热,得到溶液A,并产生刺激性气味的气体
步骤二:向溶液A加入足量稀盐酸和BaCl2溶液,得到溶液B、白色沉淀和有刺激性气味的气体
步骤三:往B溶液中通入适量Cl2,得到黄褐色溶液C
(1)下列有关该溶液说法正确的是__________。
A. 一定存在SO42-、I-、NH4+、SO32-
B. 一定不存在Fe2+、CO32-、MnO4-
C. 可能存在CO32-、Cl-、Na+、K+
D. 可用AgNO3溶液确认原溶液中是否存在Cl-
(2)步骤三得到黄褐色溶液的离子方程式是____________。
(3)若向原溶液中先加入足量的盐酸,再加入足量的________(填化学式)并加热,通过现象也能得出步骤一、二相同的结论。
(4)对于溶液中还可能存在的阳离子,确认其存在的实验方法是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分子中既有σ键,又有π键的是 ( )
①HCl ②H2O ③N2④H2O2⑤C2H4⑥C2H2
A. ①②③ B. ③④⑤⑥ C. ①③⑥ D. ③⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com