
【题目】为探究Na与C02反应产物,某化学兴趣小组按如图装置进行实验。
己知:CO+2Ag(NH3)2OH=2Ag↓+ (NH4)2CO3+2NH3

回答下列问题:
(1)写出A中反应的离子方程式_____________________________________;
(2)仪器X的名称是____________________,B中的溶液为_____________________;
(3)先称量硬质玻璃管的质量为mlg,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是m2g.再进行下列实验操作,其正确顺序是____________(填标号);
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,通入C02至E中出现浑浊 e.称量硬质玻璃管 f.冷却到室温
重复上述操作步骤,直至硬质玻璃管恒重,称得质量为m3g。
(4)加热硬质玻璃管一段时间,观察到以下现象:
①钠块表面变黑,熔融成金属小球;
②继续加热,钠迅速燃烧,产生黄色火焰。反应完全后,管中有大量黑色物质;
③F中试管内壁有银白物质产生。
产生上述②现象的原因是______________________________________;
(5)探究固体产物中元素Na的存在形式
假设一:只有Na2CO3;
假设二:只有Na2O;
假设三:Na2O和Na2CO3均有
完成下列实验设计,验证上述假设:
步骤 | 操作 | 结论 |
1 | 将硬质玻璃管中的固体产物溶于水后过滤; | 假设一成立 |
2 | 往步骤1所得滤液中_________________________________; 现象:____________________________________。 |
m1 | m2 | m3 |
66.7g | 69.0g | 72.lg |
(6)根据上述实验现象及下表实验数据,写出Na与CO2反应的总化学方程式____________________________________________。
【答案】CaCO3+2H+=Ca2++CO2↑+H2O 长颈漏斗 饱和碳酸氢钠溶液 d、a、b、f、c、e 钠的焰色反应为黄色,钠与二氧化碳反应有碳单质生成 加入足量BaCl2溶液(或足量CaCl2溶液)后滴入酚酞试液(或测pH) 溶液不变红(pH=7) 12Na+llCO2=6Na2CO3+C+4CO
【解析】
根据实验原理及实验装置图书写实验装置中发生的离子方程式,分析实验步骤,仪器名称;根据实验现象及钠的化合物的性质混合物的组成;根据图中数据根据质量差分析反应的产物,书写相关反应方程式。
(1)A是大理石与稀盐酸制取二氧化碳的反应,离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O,故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;
(2)仪器X的名称是长颈漏斗,B 中的溶液为饱和NaHCO3溶液,用于除去CO2中的HCl气体,故答案为:长颈漏斗;饱和碳酸氢钠溶液;
(3)先称量硬质玻璃管的质量为m1g,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是m2、d.打开K1和K2,通入CO2至E中出现浑浊、a.点燃酒精灯,加热、b.熄灭酒精灯、f.冷却到室温、c.关闭K1和K2、e.称量硬质玻璃管,重复上述操作步骤,直至硬质玻璃管恒重,称得质量为m3g,其正确顺序是 d→a→b→f→c→e,故答案为: d、a、b、f、c、e;
(4)钠的焰色反应为黄色,钠与二氧化碳反应有碳单质生成,反应完全后,管中有大量黑色物质,故答案为:钠的焰色反应为黄色,钠与二氧化碳反应有碳单质生成;
(5)探究固体产物中元素Na的存在形式:将硬质玻璃管中的固体产物溶于水后过滤,往步骤1所得滤液中加入足量BaCl2溶液(或足量CaCl2溶液),滴入酚酞试液,溶液不变红色,则假设一成立,故答案为:加入足量BaCl2溶液(或足量CaCl2溶液)后滴入酚酞试液(或测pH;溶液不变红(pH=7);
(6)反应前钠的质量为:m2-m1=69.0g-66.7g=2.3g,即0.1mol钠,若全部转化为碳酸钠,则碳酸钠的质量为:![]() ,物质的量为0.05mol,反应后产物的质量为:m3-m1=72.1g-66.7g=5.4g,则还生成碳,且碳的质量为0.1g,即
,物质的量为0.05mol,反应后产物的质量为:m3-m1=72.1g-66.7g=5.4g,则还生成碳,且碳的质量为0.1g,即![]() mol,结合质量守恒,钠和二氧化碳反应生成碳酸钠、碳,应该还生成一氧化碳,故反应方程式为:12Na+llCO2=6Na2CO3+C+4CO,故答案为:12Na+llCO2=6Na2CO3+C+4CO。
mol,结合质量守恒,钠和二氧化碳反应生成碳酸钠、碳,应该还生成一氧化碳,故反应方程式为:12Na+llCO2=6Na2CO3+C+4CO,故答案为:12Na+llCO2=6Na2CO3+C+4CO。


科目:高中化学 来源: 题型:
【题目】有A、B、C三种常见的金属单质,A在空气中燃烧生成淡黄色固体甲;B在空气中加热熔化但不滴落;C在一定条件下与水蒸气反应生成H2和一种黑色固体。
请根据以上信息回答下列问题:
(1)写出下列物质化学式:A_________B_________C_________甲_________
(2)按要求写出方程式:
①A在空气中燃烧的化学方程式:___________________________________________
②B与氢氧化钠溶液反应的离子方程式:_____________________________________
③C与水蒸气反应的化学方程式:___________________________________________
④甲与水反应的化学方程式:_______________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种气态烷烃和一种气态烯烃的混合物共9g,平均相对分子质量为22.5。使混合气通过足量溴水,溴水增重4.2g,则混合气中的烃可能是( )
A.甲烷和乙烯B.甲烷和丙烯C.乙烷和乙烯D.乙烷和丙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等物质的量的N2、O2、CO2混合气体通过一定量Na2O2后,体积变为原体积的8/9(同温同压),这时混合气体中N2、O2、CO2物质的量之比为( )
A. 6: 7: 3 B. 3: 3: 2
C. 3: 4: 1 D. 6: 9: 0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有一瓶无色澄清溶液,其中可能含H+、Na+、Mg2+、Ba2+、Cl、SO42、CO32离子。现进行以下实验:
A、用pH试纸检验溶液,发现溶液呈强酸性;
B、取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,无沉淀产生;
C、取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
①根据上述事实确定:该溶液中肯定存在的离子有_________________________;
肯定不存在的离子有___________________________。
②写出C中发生反应的离子方程式________________________________。
(2)①还原铁粉与高温水蒸气反应的化学方程式:_____________________________;
②除去Mg粉中的Al粉的试剂是__________________,反应的离子方程式为:___________________________________;
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
____Fe(OH)3 +____ClO-+____OH- =__FeO42-+___Cl-+_____ _______
(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是___________;
当有2mol H3PO4生成,转移的电子的物质的量为__________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列条件下,两瓶气体所含原子数一定相等的是( )
A.同质量、同体积的N2和COB.同温度、同体积的H2和N2
C.同体积、同密度的C2H4和C3H4D.同压强、同体积的N2O和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室回收废水中苯酚的过程如图所示。下列说法不正确的是( )
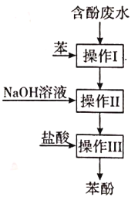
A. 操作Ⅰ为萃取,分液,萃取剂也可以用选用![]()
B. 苯酚钠在苯中的溶解度比在水中的小
C. 操作Ⅱ中得到的苯,可在操作Ⅰ中循环使用
D. 操作Ⅲ中要用蒸馏方法分离出苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源等(如图所示),下列有关说法正确的是
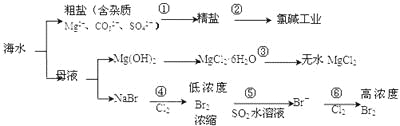
A.过程①加入的药品顺序为:Na2CO3溶液→BaCl2溶液→NaOH溶液→加盐酸后过滤
B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2
C.工业上通过电解饱和MgCl2溶液制取金属镁
D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若室温下0.1mol·L-1NaX溶液中pH=9,则该溶液中发生水解反应的X-占全部X-的( )
A.0.01%B.0.09%C.1.0%D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com