
(12��)��ѧ���������ɳ�����չ������أ���Դ�������������Լ��ճ�����ȶ��벻����ѧ��
(1)��ɽ�ǹ��Ҽ�����ϲ�ҵ���أ�����������ǽ������ϵ����ǡ�����ٳ����ֺ���IJ������� �� �� �� ���������ڸ����»�ԭSiCl4�Ǹߴ������������е�һ�����ڣ�д���÷�Ӧ�Ļ�ѧ����ʽ �� �������� ��
(2)����ʹ�û�ʯȼ�ϣ���ֱ�ӵ�Σ������ɡ�����ЧӦ���������ꡱ�Ȼ������⡣Ϊ�˷������꣬����úȼ��ʱ������ŷŵ�SO2��ij���Ṥ����ʹ��ʯ��������β�����漰�Ļ�ѧ����ʽΪ�� ���� ���� ���� ���� ���� ���� ���� ���� ����
(3)����β���е�NO��CO�Ѿ���Ϊ������п�������Ҫ��ȾԴ����������ȼ����һ�㲻����Ԫ�أ�β���е�NO�Ӻζ�����д���йػ�ѧ����ʽ ����������β����NO��CO��һ�ַ����ǣ���������������װһ����ת��װ�ã�ʹNO��CO��Ӧ������CO2��N2��д����Ӧ�Ļ�ѧ����ʽ ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
(12��)���������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӡ�
��1��Ŀǰ���ó��ٽ�CO2����״̬������̬��Һ̬֮�䣩���������������ѳ�Ϊһ�����ƣ���һ�����Ի����Ļ����������� ��
��2����CO2ת�����л������Чʵ��̼ѭ����CO2ת�����л�������Ӻܶ࣬�磺
���Ϸ�Ӧ�У�����ܵ��� ��ԭ����������ߵ��� ��
��3��Ϊ̽����CO2������ȼ�ϼ״��ķ�Ӧԭ�����ֽ�������ʵ�飺
�����Ϊ1L���ܱ������У�����1molCO2��3molH2��һ�������·�����Ӧ��
 CO2��g��+3H2��g�� CH3OH��g��+H2O��g����H=-49.0kJ/mol
CO2��g��+3H2��g�� CH3OH��g��+H2O��g����H=-49.0kJ/mol
���CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ��
�ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v��H2��= mol/��L��min��
�ڸ÷�Ӧ��ƽ�ⳣ������ʽΪ �������¶ȣ�ƽ�ⳣ������ֵ��
�����������С�����䡱����
�����д�ʩ����ʹn��CH3OH��/n��CO2��������� .
A�������¶� B������He��g����ʹ��ϵѹǿ����
C����H2O��g������ϵ�з��� D���ٳ���1molCO2��3molH2
��4�������Ǻϳɰ�����Ҫԭ�ϣ��ϳɰ���Ӧ���Ȼ�ѧ����ʽ���£�
�ٵ��ϳɰ���Ӧ�ﵽƽ��ı�ijһ������������ı�N2��H2��NH3����������Ӧ������ʱ��Ĺ�ϵ����ͼ��ʾ��
ͼt1ʱ����ƽ���ƶ������������� ��
���б�ʾƽ��������NH3������ߵ�һ��ʱ���� ��
���¶�ΪT��Cʱ����3amolH2��amolN2������л������ܱ������У���������������ƶ�����ַ�Ӧ����N2��ת����Ϊ50%���������ͬ�¶��½�3amolH2��amolN2��2amolNH3�������������У�ƽ��ʱH2��ת����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��09��10�꽨�����и߶���ѧ����ĩ���Ի�ѧ�� ���ͣ������
(12��)���������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӡ�
��1��Ŀǰ���ó��ٽ�CO2����״̬������̬��Һ̬֮�䣩���������������ѳ�Ϊһ�����ƣ���һ�����Ի����Ļ����������� ��
��2����CO2ת�����л������Чʵ��̼ѭ����CO2ת�����л�������Ӻܶ࣬�磺
���Ϸ�Ӧ�У�����ܵ��� ��ԭ����������ߵ��� ��
��3��Ϊ̽����CO2������ȼ�ϼ״��ķ�Ӧԭ�����ֽ�������ʵ�飺
�����Ϊ1L���ܱ������У�����1molCO2��3molH2��һ�������·�����Ӧ�� CO2��g��+3H2��g�� CH3OH��g��+H2O��g����H=-49.0kJ/mol
CO2��g��+3H2��g�� CH3OH��g��+H2O��g����H=-49.0kJ/mol
���CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ��
�ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v��H2��= mol/��L��min��
�ڸ÷�Ӧ��ƽ�ⳣ������ʽΪ �������¶ȣ�ƽ�ⳣ������ֵ��
�����������С�����䡱����
�����д�ʩ����ʹn��CH3OH��/n��CO2��������� .
| A�������¶� | B������He��g����ʹ��ϵѹǿ���� |
| C����H2O��g������ϵ�з��� | D���ٳ���1molCO2��3molH2 |


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012���������ϴ�ѧ���и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
(12��)��ѧ���������ɳ�����չ������أ���Դ�������������Լ��ճ�����ȶ��벻����ѧ��
(1)��ɽ�ǹ��Ҽ�����ϲ�ҵ���أ�����������ǽ������ϵ����ǡ�����ٳ����ֺ���IJ������� �� �� �� ���������ڸ����»�ԭSiCl4�Ǹߴ������������е�һ�����ڣ�д���÷�Ӧ�Ļ�ѧ����ʽ �� ���� �� �� ��
(2)����ʹ�û�ʯȼ�ϣ���ֱ�ӵ�Σ������ɡ�����ЧӦ���������ꡱ�Ȼ������⡣Ϊ�˷������꣬����úȼ��ʱ������ŷŵ�SO2��ij���Ṥ����ʹ��ʯ��������β�����漰�Ļ�ѧ����ʽΪ�� ���� ���� ���� ���� ���� ���� ���� ���� ����
(3)����β���е�NO��CO�Ѿ���Ϊ������п�������Ҫ��ȾԴ����������ȼ����һ�㲻����Ԫ�أ�β���е�NO�Ӻζ�����д���йػ�ѧ����ʽ ����������β����NO��CO��һ�ַ����ǣ���������������װһ����ת��װ�ã�ʹNO��CO��Ӧ������CO2��N2��д����Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��09-10�꽨�����и߶���ѧ����ĩ���Ի�ѧ�� ���ͣ������
(12��)���������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӡ�
��1��Ŀǰ���ó��ٽ�CO2����״̬������̬��Һ̬֮�䣩���������������ѳ�Ϊһ�����ƣ���һ�����Ի����Ļ����������� ��
��2����CO2ת�����л������Чʵ��̼ѭ����CO2ת�����л�������Ӻܶ࣬�磺
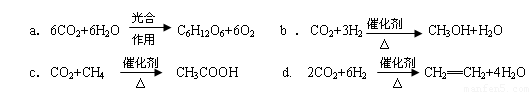
���Ϸ�Ӧ�У�����ܵ��� ��ԭ����������ߵ��� ��
��3��Ϊ̽����CO2������ȼ�ϼ״��ķ�Ӧԭ�����ֽ�������ʵ�飺
�����Ϊ1L���ܱ������У�����1molCO2��3molH2��һ�������·�����Ӧ��
 CO2��g��+3H2��g�� CH3OH��g��+H2O��g����H=-49.0kJ/mol
CO2��g��+3H2��g�� CH3OH��g��+H2O��g����H=-49.0kJ/mol
���CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ��
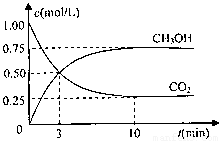
�ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v��H2��= mol/��L��min��
�ڸ÷�Ӧ��ƽ�ⳣ������ʽΪ �������¶ȣ�ƽ�ⳣ������ֵ��
�����������С�����䡱����
�����д�ʩ����ʹn��CH3OH��/n��CO2��������� .
A�������¶� B������He��g����ʹ��ϵѹǿ����
C����H2O��g������ϵ�з��� D���ٳ���1molCO2��3molH2
��4�������Ǻϳɰ�����Ҫԭ�ϣ��ϳɰ���Ӧ���Ȼ�ѧ����ʽ���£�
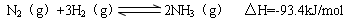
�ٵ��ϳɰ���Ӧ�ﵽƽ��ı�ijһ������������ı�N2��H2��NH3����������Ӧ������ʱ��Ĺ�ϵ����ͼ��ʾ��
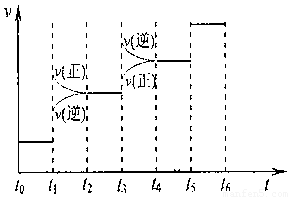
ͼt1ʱ����ƽ���ƶ������������� ��
���б�ʾƽ��������NH3������ߵ�һ��ʱ���� ��
���¶�ΪT��Cʱ����3amolH2��amolN2������л������ܱ������У���������������ƶ�����ַ�Ӧ����N2��ת����Ϊ50%���������ͬ�¶��½�3amolH2��amolN2��2amolNH3�������������У�ƽ��ʱH2��ת����Ϊ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com