
【题目】以下实验操作可能会导致实验结果偏高的是( )
A. 配制一定物质的量浓度的溶液:移液后未洗涤烧杯
B. 配制一定物质的量浓度的溶液:定容时仰视刻度线
C. 配制一定物质的量浓度稀硫酸时:用量筒量取浓硫酸时俯视读数
D. 用浓硫酸与烧碱的稀溶液反应来测定中和热的数值
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 0.1 mol·L-1 KSCN溶液中:Fe3+、NH4+ 、Br-、SO42 -
B. ![]() =106的溶液中:NH4+ 、K+、AlO2- 、NO3-
=106的溶液中:NH4+ 、K+、AlO2- 、NO3-
C. 能使甲基橙变红的溶液中:Cu2+、Mg2+、SO42 -、Cl-
D. 0.1 mol·L-1 Ca(NO3)2溶液中:Na+、NH4+ 、CO32 -、CH3COO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氟化氮![]() 是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和
是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和![]() ,请根据要求回答下列问题:
,请根据要求回答下列问题:
(1)反应过程中,被氧化与被还原的元素原子的物质的量之比为 ______ .
(2)写出该反应的化学方程式 ______ ![]() 若反应中生成
若反应中生成![]()
![]() ,转移的电子数目为 ______ 个
,转移的电子数目为 ______ 个![]()
(3)![]() 是一种无色、无臭的气体,但一旦
是一种无色、无臭的气体,但一旦![]() 在空气中泄漏,还是易于发现
在空气中泄漏,还是易于发现![]() 你判断该气体泄漏时的现象是 ______ .
你判断该气体泄漏时的现象是 ______ .
(4)一旦![]() 泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除
泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除![]() 、NaF、
、NaF、![]() 外,还肯定有 ______
外,还肯定有 ______ ![]() 填化学式
填化学式![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置或操作进行相应实验,能达到实验目的的是

A. 用图1所示装置收集SO2气体
B. 用图2所示装置检验溴乙烷与NaOH醇溶液共热产生的乙烯
C. 用图3所示装置从食盐水中提取NaCl
D. 用图4所示装置制取并收集O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A和2 mol B气体置于1 L的密闭容器中,混合后发生如下反应:2A(s) + B(g)=2C(g)。若经2 s后测得C的浓度为1.2 mol/L,下列说法正确的是( )
A. 用物质A表示的反应速率为0.6mol/(L·s)
B. 用物质B表示的反应速率为1.2mol/(L·s)
C. 2 s时物质A的转化率为30%
D. 2 s时物质B的浓度为0.6 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素是构成我们生活的世界中一切物质的“原材料”。
(1)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。
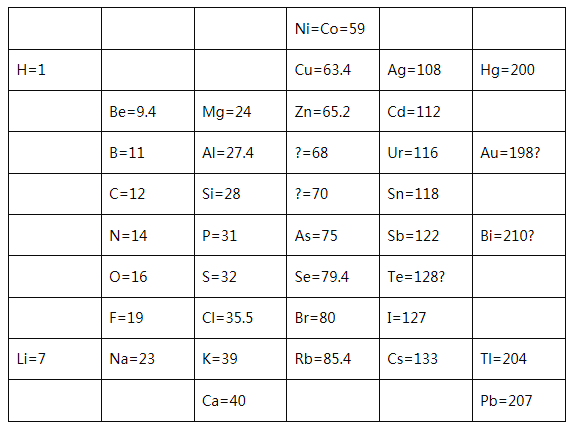
①门捷列夫将已有元素按照相对原子质量排序,同一_________(填“横行”或“纵列”)元素性质相似。结合表中信息,猜想第4列方框中“?=70”的问号表达的含义是______,第5列方框中“Te=128?”的问号表达的含义是________。
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量递增呈现周期性变化,而是随着原子序数(核电荷数)递增呈现周期性变化。其本质原因是_____(填字母序号)。
A. 随着核电荷数递增,元素主要化合价呈现周期性变化
B. 随着核电荷数递增,原子核外电子排布呈现周期性变化
C. 随着核电荷数递增,原子半径呈现周期性变化
(2)短周期元素A、B、D、E、G、J在周期表中的位置如下:
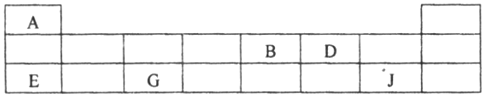
根据上表回答问题:
①第三周期的四种元素中离子半径最小的是_________ (用元素符号填答)。
②B、D的非金属性由大到小的顺序是__________ (用元素符号填答)。
③E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为i.H++OH-=H2O、ii.___、iii.___。
④用电子式表示A2D形成过程_______________。
(3)元素Y的一种含氧酸化学式为 H3YO3,其结构式可表示为:![]() 。该酸为______元酸,请写出该酸与过量氢氧化钠溶液反应的化学方程式_____。(用对应元素符号填答)(已知信息:氢氧原子结合成的一种原子团“—OH”叫羟基,含氧酸中只有羟基氢才可电离出 H+。)
。该酸为______元酸,请写出该酸与过量氢氧化钠溶液反应的化学方程式_____。(用对应元素符号填答)(已知信息:氢氧原子结合成的一种原子团“—OH”叫羟基,含氧酸中只有羟基氢才可电离出 H+。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向0.6molFeBr2溶液中通入amolCl2。下列叙述不正确的是( )
A. 当a=0.2时,发生的反应为:2Fe2++Cl2=2Fe3++2Cl-
B. 当a=0.9时,发生的反应为:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
C. 若溶液中Br- 有一半被氧化时,c(Fe3+):c(Br-):c(Cl-)=l:1:3
D. 当0<a<0.3时,溶液中始终满足2c(Fe2+)+3c(Fe3+)+c(H+)=c(Cl-)+c(Br-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是( )
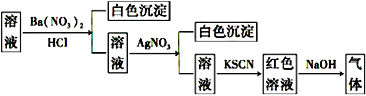
A. 原溶液中一定含有SO42-B. 原溶液中一定含有NH4+
C. 原溶液中一定含有Cl-D. 原溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,气体被还原的是
A. 乙烯使Br2的四氯化碳溶液褪色 B. 氨气使AlCl3溶液产生白色沉淀
C. 氯气使KBr溶液变黄 D. 二氧化碳使Na2O2固体变白
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com