
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH4+、Mg2+、Ba2+、CO32﹣、SO42﹣、Cl﹣,现取三份100mL溶液进行如下实验:根据上述实验,以下推测正确的是( )
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量KOH溶液加热后,收集到气体0.08mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g.
A. Na+一定存在
B. 100mL溶液中含0.01mol CO32﹣
C. Cl﹣一定存在
D. Ba2+一定不存在,Mg2+可能存在
【答案】A
【解析】
根据题意分析,第一份溶液加入AgNO3溶液有沉淀产生,推得可能含有Cl-、CO32-、SO42-中的至少一种;第二份溶液加足量KOH溶液加热后收集到气体,推得一定含有NH4+,一定不存在Mg2+;第三份溶液利用发生的离子反应,经过计算、推得一定存在CO32-、SO42-,一定不存在Ba2+;根据溶液中阴阳离子的电荷守恒,即可推出Na+是否存在,由Na+物质的量的变化分析Cl-的情况。
根据题意,Ba2+和SO42-可发生离子反应生成BaSO4沉淀,因此两者不能大量共存。Ba2+和CO32-可发生离子反应生成BaCO3沉淀,因此两者也不能大量共存。
第一份加入AgNO3溶液有沉淀产生,可能发生Cl-+Ag+═AgCl↓、CO32-+2Ag+═Ag2CO3↓、SO42-+2Ag+═Ag2SO4↓,所以可能含有Cl-、CO32-、SO42-中的至少一种;
第二份加足量KOH溶液加热后,收集到气体0.08mol,能和KOH溶液加热产生气体的只能是NH4+,而没有沉淀产生说明一定不存在Mg2+(Mg2+可以和OH-反应生产氢氧化镁沉淀)。故可确定一定含有NH4+,一定不存在Mg2+,根据反应NH4++OH-![]() NH3↑+H2O,产生NH3为0.08mol,可得NH4+也为0.08mol。
NH3↑+H2O,产生NH3为0.08mol,可得NH4+也为0.08mol。
第三份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤。干燥后,沉淀质量为4.66g。部分沉淀溶于盐酸为BaCO3,部分沉淀不溶于盐酸为BaSO4,发生反应CO32-+Ba2+═BaCO3↓、SO42-+Ba2+═BaSO4↓,因为BaCO3+2HCl═BaCl2+CO2↑+H2O而使BaCO3溶解。因此溶液中一定存在CO32-、SO42-,一定不存在Ba2+。由条件可知BaSO4为4.66g,物质的量为0.02mol,SO42-物质的量浓度为:![]() =0.2mol/L,BaCO3为12.54g-4.66g═7.88g,物质的量为0.04mol,则CO32-物质的量为0.04mol,CO32-物质的量浓度为
=0.2mol/L,BaCO3为12.54g-4.66g═7.88g,物质的量为0.04mol,则CO32-物质的量为0.04mol,CO32-物质的量浓度为![]() =0.4mol/L,由上述分析可得,溶液中一定存在CO32-、SO42-、NH4+,一定不存在Mg2+、Ba2+,而CO32-、SO42-、NH4+物质的量分别为0.04mol、0.02mol、0.08mol,CO32-、SO42-所带负电荷分别为0.04mol×2、0.02mol×2,共0.12mol,NH4+所带正电荷为0.08mol,根据电荷守恒可知,一定含有钠离子,钠离子的物质的量最小是0.04mol,氯离子不能确定。
=0.4mol/L,由上述分析可得,溶液中一定存在CO32-、SO42-、NH4+,一定不存在Mg2+、Ba2+,而CO32-、SO42-、NH4+物质的量分别为0.04mol、0.02mol、0.08mol,CO32-、SO42-所带负电荷分别为0.04mol×2、0.02mol×2,共0.12mol,NH4+所带正电荷为0.08mol,根据电荷守恒可知,一定含有钠离子,钠离子的物质的量最小是0.04mol,氯离子不能确定。
A、Na+一定存在,故A正确;B、100mL溶液中含0.04mol碳酸根离子,故B错误;C、氯离子是否存在无法确定,故C错误;D、Mg2+、Ba2+一定不存在,故D错误;故选A。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D的原子序数依次增大,B和D同主族;X、Y、N分别是由以上四种元素中两种组成的化合物,Z是由以上三种元素组成的化合物;若X与Y的摩尔质量相同,Y为淡黄色固体,N常温下是液体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定正确的是( )
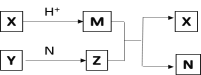
A. 相对分子质量M>N,沸点M>N
B. 原子半径:D>B>C>A
C. Z 为 NaOH
D. M是一种非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~D是中学化学实验中常见的几种温度计装置示意图.
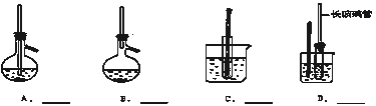
①酒清和浓硫酸混合加热制乙烯
②电石跟水反应制乙炔
③分离苯和硝基苯的混合物
④苯和溴的取代反应
⑤石油的分馏实验
⑥浓盐酸和二氧化锰混合加热制氯气
⑦测定硝酸钾在水中溶解度
⑧食盐和浓硫酸混合加热制氯化氢
⑨苯的硝化反应
(1)请从①~⑧中选出必须使用温度计的实验,把编号填入最适宜的装置图A~C的空格中。A________B________C________D________
(2)下列括号内的物质为所含的少量杂质,请选用适当的试剂和分离装置将杂质除去。
试剂:a.水,b.氢氧化钠,c.食盐,d.溴水,e.生石灰,f.溴的四氯化碳溶液
分离装置:A.分液装置,B.过滤装置,C.蒸馏装置,D.洗气装置
1﹣氯丙烷(乙醇)_____;乙烷(乙烯)_____;苯(苯酚)____;溴化钠溶液(碘化钠)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)用工业FeCl3粗品(含Ca、Mn、Cu等杂质离子)制取高纯铁红,实验室常用萃取剂X(甲基异丁基甲酮)萃取法制取高纯铁红的主要实验步骤如下:
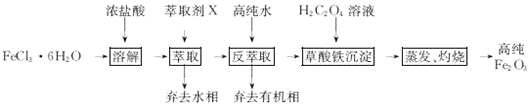
已知:HCl(浓)+FeCl3![]() HFeCl4
HFeCl4
试回答下列问题:
(1)用萃取剂X萃取,该步骤中:
①Ca、Mn、Cu等杂质离子几乎都在 (填“水”或“有机”)相。
②若实验时共用萃取剂X 120 mL,萃取率最高的方法是 (填字母)。
a.一次性萃取,120 mL
b.分2次萃取,每次60 mL
c.分3次萃取,每次40 mL
(2)用高纯水反萃取,萃取后水相中铁的存在形式是 (写化学式);反萃取能发生的原因是 。
(3)所得草酸铁沉淀需用冰水洗涤,其目的是 。
(4)测定产品中铁的含量需经酸溶、还原为Fe2+,然后在酸性条件下用标准K2Cr2O7溶液滴定,已知铬的还原产物为Cr3+,写出该滴定反应的离子方程式,并用单线桥标出电子转移的方向和数目 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以环戊烷为原料制备环戊二烯的合成路线如图,则( )
![]()
A. A的结构简式是![]()
B. ①②的反应类型分别是取代、消去
C. 反应②③的条件分别是浓硫酸加热、光照
D. 酸性KMnO4溶液褪色可证明![]() 已完全转化成
已完全转化成![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对牙膏的探究要用到许多化学知识。
(1)下表列出了三种牙膏中的摩擦剂,请在表中填写三种摩擦剂所属的物质类别。
牙膏 | 某儿童牙膏 | 某防臭牙膏 | 某透明牙膏 |
摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
摩擦剂的物质类别(指酸、碱、两性氢氧化物、盐、氧化物) | ________ | ________ | ________ |
(2)根据你的推测,牙膏摩擦剂的溶解性属于_________(填“易溶”或“难溶”)。
(3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。某学生设计了一种实验室制备碳酸钙的实验方案,其流程图为:
![]()
![]()
请写出上述方案中有关反应的化学方程式:
①____________________________________________________________;
②___________________________________________________________;
③____________________________________________________________。
(4)请你仍用石灰石作原料(其他试剂自选),设计实验室制备碳酸钙的另一种实验方案,依照(3)所示,将你的实验方案用流程图表示出来:
![]() _______________。
_______________。
你设计的方案的优点为_____________________________________________________。
(5)检验牙膏中是否含有碳酸盐的实验方法是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com