
【题目】LiPF6是锂离子电池中广泛应用的电解质。某工厂用LiF、PCl5为原料,低温反应制备LiPF6,其流程如下:

已知:HCl的沸点是﹣85.0℃,HF的沸点是19.5℃。
(1)第①步反应中无水HF的作用是______________。反应设备不能用玻璃材质的原因是______________________(用化学方程式表示)。无水HF有腐蚀性和毒性,工厂安全手册提示:如果不小心将HF沾到皮肤上,可立即用2%的___________溶液冲洗。
(2)该流程需在无水条件下进行,第③步反应中PF5极易水解,其产物为两种酸,写出PF5水解的化学方程式:_______________________________。
(3)第④步分离采用的方法是_________;第⑤步分离尾气中HF、HCl采用的方法是______。
(4)LiPF6产品中通常混有少量LiF。取样品wg,测得Li的物质的量为nmol,则该样品中LiPF6的物质的量为______mol(用含w、n的代数式表示)。
【答案】(1)作溶剂和反应物 SiO2+4HF=SiF4↑+2H2O NaHCO3
(2)PF5+4H2O=H3PO4+5HF
(3)过滤 冷凝
(4)![]() mol
mol
【解析】试题分析:(1)根据题目中的流程可以看出,固体+液体→新物质+饱和溶液,所以无水HF的作用是反应物和溶剂;玻璃的主要成分中含有二氧化硅,能和HF发生反应,化学方程式为SiO2+4HF═SiF4↑+2H2O;HF属于弱酸,必须用弱碱性溶液来除去(比如2%的NaHCO3溶液);(2)根据题目中的信息“PF5极易水解,其产物为两种酸”,则根据元素组成可知,两种酸分别是H3PO4和HF,所以反应的方程式为PF5+4H2O═H3PO4+5HF,(3)第④步分离的是固体(LiPF4(s))和液体(HF(l)),所以采用过滤的方法;分离尾气中HF、HCl,可以利用二者沸点的差异(HF分子之间存在氢键)进行分离,所以采用冷凝法;(4)设LiPF6为xmol,LiF为ymol;根据Li守恒,有x+y=n,根据质量守恒有152x+26y=w,解得x=(w-26n):126moL。


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】下列反应中HNO3既表现出酸性又表现出强氧化性的是
A.稀硝酸与CuO反应
B.稀硝酸与NaOH 溶液反应
C.浓硝酸与灼热的碳反应
D.浓硝酸与铜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化铬是化学合成中的常见物质,三氯化铬易升华,在高温下能被氧气氧化。制备三氯化铬的流程如图所示:

(1)重铬酸铵分解产生的三氧化二铬(Cr2O3难溶于水)需用蒸馏水洗涤,如何用简单方法判断其已洗涤干净? 。
(2)已知CCl4沸点为76.8℃,为保证稳定的CCl4气流,适宜的加热方式是。
(3)用如图装置制备CrCl3时,反应管中发生的主要反应为:Cr2O3+3CCl4![]() 2CrCl3+3COCl2,则向三颈烧瓶中通入N2的作用:① ;② 。
2CrCl3+3COCl2,则向三颈烧瓶中通入N2的作用:① ;② 。

(4)Cr对环境会造成严重的污染,废水中的Cr3+可用石灰乳进行沉降,写出沉降的离子方程式________________________。
(5)样品中三氯化铬质量分数的测定:称取样品0.3000g,加水溶解并定容于250mL
容量瓶中。移取25.00mL于碘量瓶(一种带塞的锥形瓶)中,加入1g Na2O2,充分加热煮沸,适当稀释,然后加入过量2mol·L–1H2SO4至溶液呈强酸性,此时铬以![]() 存在,再加入1.1g KI,加塞摇匀,充分反应后铬以Cr3+存在,于暗处静置5min后,加入0.5mL指示剂,用0.0250mol·L–1标准Na2S2O3溶液滴定至终点,平行测定三次,平均消耗标准Na2S2O3溶液21.00mL。(已知:2Na2S2O3+I2
存在,再加入1.1g KI,加塞摇匀,充分反应后铬以Cr3+存在,于暗处静置5min后,加入0.5mL指示剂,用0.0250mol·L–1标准Na2S2O3溶液滴定至终点,平行测定三次,平均消耗标准Na2S2O3溶液21.00mL。(已知:2Na2S2O3+I2![]() Na2S4O6+2NaI)
Na2S4O6+2NaI)
①滴定实验可选用的指示剂名称为,判定终点的现象是;若滴定时振荡不充分,刚看到局部变色就停止滴定,则会使样品中无水三氯化铬的质量分数的测量结果(填“偏高”“偏低”或“无影响”)。
②加入Na2O2后要加热煮沸,其主要原因是,如果没有加热煮沸,则会使样品中无水三氯化铬的质量分数的测量结果(填“偏高”“偏低”或“无影响”)。
③加入KI时发生反应的离子方程式为。
④样品中无水三氯化铬的质量分数为(结果保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
A.CO2和H2S B.SO2和SiO2 C.NH4Cl和HCl D.CCl4和KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用化学知识解决生活中的问题,下列家庭小实验或说法不合理的是
A. 用米汤检验食盐中是否含碘酸钾(KIO3)
B. 用食醋除去暖水瓶中的薄层水垢
C. 医用酒精的浓度通常为75%,可用于杀菌消毒
D. 用灼烧并闻气味的方法区别纯棉织物和纯羊毛织物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
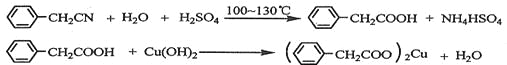
制备苯乙酸的装置示意图如下(加热和夹持装置等略):
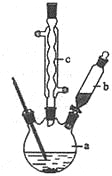
已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250mL三口瓶a中加入70mL70%硫酸,并向三口烧瓶中放入少量______,其作用是_______。
(2)将a中的溶液加热至100℃,缓缓滴加20g苯乙腈到硫酸溶液中,然后升温至130℃继续反应。用仪器b缓缓滴加苯乙腈的原因是 _________ ;仪器c的名称是 。反应结束后加适量冷水,再分离出苯乙酸粗品。加人冷水的目的是 。分离苯乙酸粗品操作中用到的玻璃仪器除烧杯外还有_________ 。
(3)提纯粗苯乙酸后最终得到21g纯品,则苯乙酸的产率是 。(保留两位有效数字)
(4)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于氧化还原反应,又属于吸热反应的是( )。
A. 铝片与稀盐酸的反应
B. Ba(OH)2·8H2O和NH4Cl的反应
C. 灼热的炭与CO2的反应
D. 甲烷在氧气中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(13分)乙酸正丁酯是一种水果香味的无色透明液体,常用于调制香料和药物。实验室用正丁醇和乙酸制备,反应原理如下:
CH3COOH+CH3CH2CH2CH2OH![]() CH3COOCH2CH2CH2CH3+H2O
CH3COOCH2CH2CH2CH3+H2O
某兴趣小组拟用如图装置制备少量乙酸正丁酯:

步骤1:加料。向干燥的100ml圆底烧瓶中加入37ml正丁醇、22ml冰醋酸及10滴浓硫酸(试剂加入顺序未确定),摇匀后,加入几粒沸石。然后安装分水器(先在分水器上端小心加水至分水器支管口处,然后再放出1~2ml的水)及回流冷凝管。
步骤2:加热回流。通过活塞控制分水器中水层液面的高度。反应完毕,停止加热。
步骤3:冷却(不可以拆卸回流冷凝管)。冷却至室温后,将烧瓶中的混合物与分水器中的酯层合并,转入分液漏斗中。
步骤4:依次用10ml水,10ml 10%碳酸钠溶液洗至中性(pH=7),再水洗一次,向洗涤后的有机相中加入适量的无水硫酸镁固体。放置一段时间后过滤、蒸馏、收集124~126℃馏分,得产品)
步骤5:用一干燥的小烧杯称产品,重量为29.0g。
相关物质的性质如下表:
物质名称 | 沸点/℃ | 熔点/℃ | 密度/g·cm-3 | 水中溶解度 |
正丁醇 | 117.3 | -89.5 | 0.80 | 7.1g/100g |
乙酸 | 118 | 16.6 | 1.0492 | 互溶 |
乙酸正丁酯 | 126.1 | -78 | 0.8826 | 1.4g/100g |
根据题意完成下列填空:
(1)加料时,三种试剂的加入顺序为 。
(2)该实验中,冷凝水从 (填“a”或“b”)口通入,使用分水器的目的是 。
(3)步骤2中判断反应结束的现象是 。
(4)步骤3中从分液漏斗中得到酯的操作 ,用10% Na2CO3溶液洗涤有机相,是为了除去有机相中的 (填结构简式)。
(5)步骤4中加入无水硫酸镁固体的作用是 。
(6)实验中正丁醇的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)己二酸 是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位。实验室合成己二酸的反应原理和实验装置示意图如下:
是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位。实验室合成己二酸的反应原理和实验装置示意图如下:
![]()

可能用到的有关数据如下:

实验步骤如下;
I、在三口烧瓶中加入16 mL 50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。
II、水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。
III、当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止。
IV、趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤得粗产品。V、粗产品经提纯后称重为5.7g。
请回答下列问题:
(1) 仪器b的名称为__________。
(2) 向三口烧瓶中滴加环己醇时,要控制好环己醇的滴入速率,防止反应过于剧烈导致温度迅速上升,否则.可能造成较严重的后果,试列举一条可能产生的后果:
_________________________________________________________________。
(3) 已知用NaOH溶液吸收尾气时发生的相关反应方程式为:
2NO2+2NaOH=NaNO2+NaNO3+H2O NO+NO2+2NaOH =2NaNO2+H2O ;如果改用纯碱溶液吸收尾气时也能发生类似反应,则相关反应方程式为:
_____________________________、________________________________。
(4)为了除去可能的杂质和减少产品损失,可分别用冰水和 洗涤晶体。
(5)粗产品可用 法提纯(填实验操作名称)。本实验所得到的己二酸产率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com