
����Ŀ����һ���������ܱ������м���2mol A��0.6mol C��һ������B�������塣һ�������·�����Ӧ��������Ũ����ʱ��仯�������ͼ����ʾ��ͼ��Ϊt2ʱ�̺�ı䷴Ӧ��������ƽ����ϵ�з�Ӧ������ʱ��仯����������ĸ��ζ����ı�һ�ֲ�ͬ����������֪t3��t4��Ϊʹ�ô�����ͼ����t0��t1��c��B��δ������
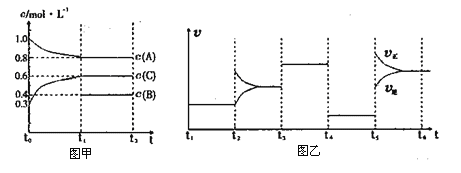
����˵������ȷ����
A. �÷�ӦΪ���ȷ�Ӧ
B. B��t0~t1�ε�ת����Ϊ60%
C. t4~t5�θı������Ϊ��Сѹǿ
D. ���¶��¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K=0.84
���𰸡�B
������������ͼ�ң�t4��t5��ѧƽ�ⲻ�ƶ�������ѧ��Ӧ���ʽ��ͣ�˵��t4����ѹǿ������Ӧǰ������ϵ��֮����ȣ�����ͼ�ף�A��Ũ�ȱ仯Ϊ0.2mol��L��1��C��Ũ�ȱ仯Ϊ0.3mol��L��1����˻�ѧ��Ӧ����ʽΪ2A(g)��B(g)![]() 3C(g)��A������ͼ�ң�t5��t6���滯ѧ��Ӧ���ʶ����ߣ���������Ӧ������У����t5ʱ�������¶ȣ�������ӦΪ���ȷ�Ӧ����A˵����ȷ��B��û��ָ�����������ʵ�ת���ʣ���B˵������C������������������C˵����ȷ��D��ƽ�ⳣ���ı���ʽΪK=
3C(g)��A������ͼ�ң�t5��t6���滯ѧ��Ӧ���ʶ����ߣ���������Ӧ������У����t5ʱ�������¶ȣ�������ӦΪ���ȷ�Ӧ����A˵����ȷ��B��û��ָ�����������ʵ�ת���ʣ���B˵������C������������������C˵����ȷ��D��ƽ�ⳣ���ı���ʽΪK=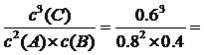 0.84����D˵����ȷ��
0.84����D˵����ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҿ����û�������������Ӧ�Ʊ�����ͪ����Ӧԭ����ʵ��װ�ã����ּг�װ���ԣ����£�

�й����ʵ��������ʼ��±���
���� | �е㣨�棩 | �ܶȣ�g��cm��3��20�棩 | �ܽ��� |
������ | 161.1��97.8��* | 0.96 | ������ˮ���� |
����ͪ | 155.6��95.0��* | 0.95 | ����ˮ���������� |
ˮ | 100.0 | 1.0 |
*�����е����ݱ�ʾ���л�����ˮ�γɵľ��й̶���ɵĻ����ķе㡣
ʵ����ͨ��װ��B������Na2Cr2O7��Һ�ӵ�ʢ��10 mL��������A�У���55 ~ 60����з�Ӧ����Ӧ��ɺ�������ˮ�������ռ�95 ~ 100�����֣��õ���Ҫ������ͪ��Ʒ��ˮ�Ļ���
��1��װ��D������Ϊ____________________________��
��2������Na2Cr2O7��Һ������������Ӧ��![]() ����Ӧ���ҽ�������ϵ�¶�Ѹ������������Ӧ���ࡣ
����Ӧ���ҽ�������ϵ�¶�Ѹ������������Ӧ���ࡣ
�ٵμ�����Na2Cr2O7��Һ�IJ���Ϊ____________________________________________��
�������ܷ��뻷��ͪ��ˮ��ԭ����__________________________________________��
��3������ͪ���ᴿ��Ҫ��������һϵ�еIJ�����
a������ȥ���Ѻ��ռ�151~156�����
b��ˮ��������(���ѷе�34.6�棬��ȼ��)��ȡ����ȡҺ�����л���
c������
d����Һ���м���NaCl���������ͣ����ã���Һ
e��������ˮMgSO4���壬��ȥ�л�����������ˮ
�������ᴿ�������ȷ˳����________________________________________________��
��B��ˮ����������ȡ��Ŀ����______________________________________________��
����������c��d��ʹ�õIJ����������ձ�����ƿ���������⣬����Ҫ�IJ���������__________������d�У�����NaC1�����������_____________________________��
��4���ָ�������ʱ������õ�����Ʒ���Ϊ6 mL������ͪ�IJ���Ϊ____________������������ȷ��0.1%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ᱽ����![]() ��һ����Ȼ����ҩ���һ���������ܷ�������ת����
��һ����Ȼ����ҩ���һ���������ܷ�������ת����
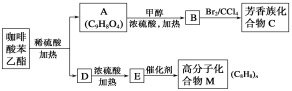
��ش��������⣺
��1��A�����еĹ�������_______________________________��
��2���߷��ӻ�����M�Ľṹ��ʽ��_______________________________��
��3��д��A��B��Ӧ�Ļ�ѧ����ʽ��_________________________��A��B�ķ�Ӧ����Ϊ__________��
��4��E��M�ķ�Ӧ����ʽΪ_____________________��B��C�ķ�Ӧ����Ϊ__________��
��5��A��ͬ���칹���кܶ��֣�����ͬʱ��������������ͬ���칹����________�֡�
�ٱ�����ֻ������ȡ���� ���ܷ���������Ӧ������̼��������Һ��Ӧ �������Ȼ�����Һ������ɫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���˴Ź����������о��л���ṹ�������ֶ�֮һ��������ȩ�Ľṹ��ʽΪCH3-CHO���ں˴Ź����������������壬������֮��Ϊ3��1��
��1���ṹʽΪ![]() ���л���ں˴Ź������������շ�����֮��Ϊ __________��
���л���ں˴Ź������������շ�����֮��Ϊ __________��
��2��ij�����л��������ͼ������ʺɱ�Ϊ46.0��̼����������Ϊ52.2%�������������Ϊ13.0%���˴Ź���������ֻ��һ�����շ壬����л������Է�������Ϊ___________����ṹ��ʽ�� _________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�ָ�������Fe3S4��þ�Ķ��ε�أ��乤��ԭ��Ϊ��Fe3S4+4Mg![]() 3Fe+4MgS��װ����ͼ��ʾ������˵������ȷ����
3Fe+4MgS��װ����ͼ��ʾ������˵������ȷ����
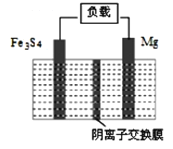
A. �ŵ�ʱ����·��ת��0.5mol�����������ӽ���Ĥ���ƶ�0.5molS2��
B. �ŵ�ʱ�������ĵ缫��ӦʽΪFe3S4+8e����3Fe+4S2��
C. ���ʱ�������ĵ缫��ӦʽΪMgS+2e����Mg+S2��
D. ���ʱ��S2���������ӽ���Ĥ������Ҳ�Ǩ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����п�����ͼװ������ȡ����İ�����

��1��д��A��������Ӧ�Ļ�ѧ����ʽ_____________________________________��
��2��U�ι�B�����ŵ�ҩƷ��__________________��
��3��ʵ������ȡ��������ʱ����ʵ������ȡ���������巢��װ����ͬ����______________������ĸ����
A. ���� B������C������ D��������̼
��4���Թ�C�Ĺܿڴ�Ҫ����һС��������������������___________________________��
��5��������ʾ�����������ڴ����е�ȼ����Ӧ���ɵ�����ˮ����Ϊ��֤����ʵ��ijͬѧ�����һ��ʵ�鷽����װ�ü�D����д���÷�Ӧ�Ļ�ѧ����ʽ__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ᶼ����Ҫ�Ĺ�ҵԭ�ϡ�
��1����״���£���500 L��������ˮ�γ�1 L��ˮ����˰�ˮ�����ʵ���Ũ��Ϊ__mol�� L-1��������λ��Ч���֣�����ҵ�ϳ��ù�����ˮ���ն������÷�Ӧ�Ļ�ѧ����ʽΪ__��
��2�����������ǹ�ҵ�����кϳ��������Ҫ;�����ϳɵĵ�һ���ǽ����Ϳ����Ļ����ͨ�����ȵIJ���Ͻ������ںϽ����Ĵ��£�����������һ���������÷�Ӧ�Ļ�ѧ����ʽΪ__��
���з�Ӧ�еİ��백�������еİ�������ͬ����__��
A��2Na+2NH3===2NaNH2+H2�� B��2NH3+3CuO===3Cu+N2+3H2O
C��4NH3+6NO===5N2+6H2O D��HNO3+NH3===NH4NO3
��ҵ�е�β��������ֻ��NO��NO2�����ռ�������գ���Ӧ�����ӷ���ʽΪ2NO2+2OH��===NO2-+NO3-+H2O��NO+NO2+2OH��===������+H2O����ƽ�÷���ʽ����______________
��3����27.2 g Cu��Cu2O�Ļ�����м���ijŨ�ȵ�ϡHNO3500 mL����Ӧ�����в���������ֻ��NO��������ȫ�ܽ����������Һ������������ֻ��Cu2+���м���1 L 1 mol��L-1��NaOH��Һʹ��������ǡ����ȫ��������ʱ��Һ�����ԣ����ó�������Ϊ39.2 g��
��Cu��ϡHNO3��Ӧ�����ӷ���ʽΪ__��
��Cu��Cu2O �����ʵ���֮��Ϊ__��
��HNO3�����ʵ���Ũ��Ϊ__mol��L-1��
��4����H2SO4��HNO3�Ļ����Һ20 mL������0.25 molL��1Ba��OH��2��Һʱ�����ɳ���������w��g����Ba��OH��2��Һ�����V��mL���Ĺ�ϵ��ͼ��ʾ��C ����Һ�����ԣ�����ԭ���Һ��H2SO4�����ʵ���Ũ��Ϊ__mol��L-1��HNO3�����ʵ���Ũ��Ϊ__mol��L-1��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��a��b��c��d��ԭ��������������,a��b�ļ۵�����֮�͵���c��d������������֮��,������Ԫ�����������b2da3��bca2���ں��������εĻ����Һ�еμ����ᣬ������ɫ���������ʵ�������������Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��

A. ԭ�Ӱ뾶��b>c>a>d B. ��̬�⻯�����ȶ��ԣ�a>d
C. d�������ﳣ����̫���ܵ�� D. ��ҵ�ϵ��c���Ȼ���ұ������c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
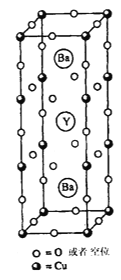
����Ŀ��1911�꣬��ѧ�ҷ��ֹ���4.2K����ʱ����ͻȻ�������㡪�������³����ԡ�1986�꣬��ѧ���ַ�����Nb3Ge��23K�¾��г�������1987��2�£������ͼ������߶�����������Һ������(�е�77 K)�ĸ��³����壬�侧����ͼ��ʾ��Ԫ�����ΪBa-Y-Cu-O(�ٽ��¶�93 K)���ƶ��˹��ʸ��³����о���������Ժʿ���2016��ȹ�����߿�ѧ��������
�ش��������⣺
��1����Nbλ�ڵ������ڣ�Nb����Χ�����Ų�ʽΪ4d45s1��Nbλ��_______��
��2�����й���GeԪ��������ȷ����______(������ѡ����ѡ��)
A��Ge����������������Ϊ���۾��� B��Ge����p���Ĺ��ɽ���
C��Ge�ĵ�һ�����ܱ�As��Se��ҪС D��Ge�ĵ縺�Ա�C��
��3��Ge(CH3)2Cl2���ӵ�����ԭ��Ge���ӻ���ʽ��______________
��4��NH3Ҳ����������������_______(����ڡ���С�ڡ�)109��28�䣬NH3�ķе�(239.6 K)����N2�е����Ҫԭ����___________________________
��5��ͼʾ���ϵ����뻯ѧʽ(��λʱ)Ϊ___________________����Y(��)Ԫ�صĻ��ϼ�Ϊ+3����Cu��ƽ�����ϼ�Ϊ_______
��6������ͭ���������������ܶѻ����侧����Cuԭ�ӵ��������Ϊa cm������ͭ�ľ����ܶ�Ϊ�� g/cm3������٤������ΪNA����ͭ�����ԭ������Ϊ________ (ֻ��һ��ϵ������a���ѡ�NA��ʾ)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com