
【题目】M被广泛用于医药、香料的合成,其一种合成路线如下(反应试剂与反应条件已省略)
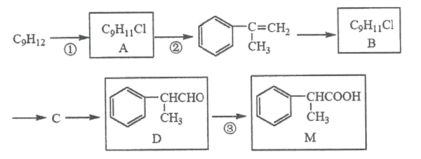
已知A与B互为同分异构体。
(1)1molD最多能与______molH2发生加成反应。
(2)反应①所需的试剂和条件是____________,反应③的反应类型是____________。
(3)反应②的化学方程式是____________。
(4)写出检验D已经完全转化为M的方法____________。
(5)写出一种符合下列要求的M的同分异构体的结构简式____________。
i. 苯环上的一氯代物只有两种 ii. 能发生水解反应 iii. 分子中含有两个甲基
(6)写出以![]() 和
和![]() 为原料制备
为原料制备![]() 的合成路线流程图。
的合成路线流程图。
已知:![]()
___________
【答案】4 氯气、光照 氧化反应 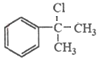 +NaOH
+NaOH![]()
![]() +NaCl+H2O 取样,加入溶液调至碱性,向其中加入新制氢氧化铜悬浊液,加热煮沸,若无砖红色沉淀产生,说明已经完全转化为
+NaCl+H2O 取样,加入溶液调至碱性,向其中加入新制氢氧化铜悬浊液,加热煮沸,若无砖红色沉淀产生,说明已经完全转化为  或
或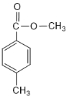

【解析】
由A反应后产物结构,可知C9H12为![]() ,与氯气在光照条件下反应生成A,A发生消去反应生成
,与氯气在光照条件下反应生成A,A发生消去反应生成![]() ,
,![]() 与HCl发生加成反应生成B,A、B互为同分异构体,且B水解产物C可以发生氧化反应生成D,结合D的结构
与HCl发生加成反应生成B,A、B互为同分异构体,且B水解产物C可以发生氧化反应生成D,结合D的结构![]() ,可知C为
,可知C为![]() 、B为
、B为![]() ,则A为
,则A为 。D发生氧化反应生成M,结合题目分析解答。
。D发生氧化反应生成M,结合题目分析解答。
(1)D中苯环和醛基都能和氢气发生加成反应,则1mol D最多能与4mol H2发生加成反应;
(2)反应①为烃的卤代反应,所需试剂与条件是氯气、光照;反应③中醛基被氧化生成羧基,则该反应的反应类型是氧化反应;
(3)反应②为卤代烃的消去反应,其反应方程式为: +NaOH
+NaOH![]()
![]() +NaCl+H2O;
+NaCl+H2O;
(4)D中醛氧化生成羧基得到M,检验D已完全转化为M,检验反应后混合液中没有醛基即可,检验的方法:取样,加入NaOH溶液调至碱性,向其中加入新制氢氧化铜悬浊液,加热,若无砖红色沉淀产生,说明D已经完全转化为M;
(5)M的同分异构体符合下列条件:i.苯环上的一氯代物只有两种,说明苯环上含有2种氢原子;ii.能发生水解反应,说明含有酯基;iii.分子中含有两个甲基,则符合条件的结构简式为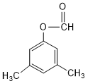 、
、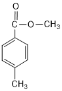 ;
;
(6)根据需要合成的目标物中有新环,以及中含有一个双键,因此可以利用已知信息进行加成反应,然后再将其与H2加成以合成目标产物,具体合成路线如下: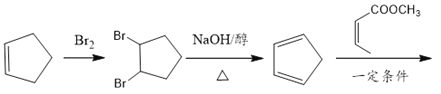
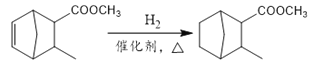 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】碳是常见的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程:
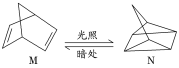
ΔH=+88.6kJ·mol-1。则M、N相比,较稳定的是_____。
(2)已知CH3OH(l)的燃烧热ΔH=-726.5kJ·mol-1,CH3OH(l)+![]() O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a________726.5(填“>”“<”或“=”)。
O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a________726.5(填“>”“<”或“=”)。
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)===2Al2O3(s)+3TiC(s) ΔH=-1176kJ·mol-1,则反应过程中,每转移1mol电子放出的热量为________。
(4)煤气化制合成气(CO和H2)
已知:①C(s)+H2O(g)CO(g)+H2(g)ΔH1=+131.3kJ·mol-1
②C(s)+2H2O(g)CO2(g)+2H2(g)ΔH2=+90kJ·mol-1
则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物N(![]() )是一种常见的有机合成中间体,在生产中用途广泛。以有机物A为原料合成M和N的路线如下所示:
)是一种常见的有机合成中间体,在生产中用途广泛。以有机物A为原料合成M和N的路线如下所示:
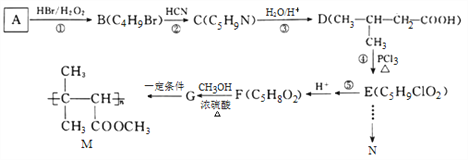
已知:I. ![]()
II. ![]()
请回答下列问题:
(1)A分子中共面的原子数最多为________个,-CN的电子式为_______________。
(2)②的反应类型为________________, E分子中所含官能团的名称为____________,G的结构简式为_____________________。
(3)写出反应⑤的化学方程式__________________________________________,写出M在酸性条件下水解的化学方程式_________________________________。
(4)D的同分异构体中,能发生银镜反应,且能与钠反应放出H2的共有______种,写出核磁共振氢谱有4组峰,且峰面积比为1:1:2:6的一种同分异构体的结构简式:____________________。
(5)结合信息,写出用E和乙醇为原料制备化合物N的合成路线:(其他试剂任选)_____________
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面三种方法都可以制得Cl2:
①MnO2+4HCl(浓) ![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
③O2+4HCl(g)  2H2O+2Cl2
2H2O+2Cl2
这三种氧化剂的氧化性由强到弱的顺序是( )
A.O2>MnO2>KMnO4
B.KMnO4>MnO2>O2
C.MnO2>KMnO4>O2
D.O2>KMnO4>MnO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为减轻大气污染,必须要加强对工业废气和汽车尾气的治理,根据所学知识回答下列问题:
(1)化石燃料包括煤、石油和________。
(2)酸雨是指pH____(填“>”“<”或“=”)5.6的降水,煤的燃烧是导致酸雨形成的主要原因,而正常雨水的pH约为5.6,原因是__________________ (用化学方程式表示)。
(3)煤的气化是高效、清洁利用煤的重要途径,可将煤炼成焦炭,再将焦炭在高温下与水蒸气反应生成一氧化碳和氢气的化学方程式为_________,该反应的基本类型是_________。
(4)在汽车尾气排放口加装“三效催化净化器”,在不消耗其他物质的情况下,可将尾气中的一氧化碳、一氧化氮转化为参与大气循环的气体和无毒的气体,该反应的化学方程式为__________________。
(5)在新能源汽车未普及时,如图所示为一种“节能减排”的有效措施,以下对乙醇作汽车燃料的描述错误的是__________(填字母)。
![]()
A.原料来源丰富 B.是可再生能源 C.燃烧完全没有污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.甲烷分子(CH4)失去一个H+,形成甲基阴离子(CH3-),变化过程中微粒的键角发生了改变,但碳原子的杂化类型没有改变
B.冰与干冰都是分子晶体,其晶胞中分子的空间排列方式类似
C.因为H2SO3和H2CO3的非羟基氧原子不同,所以它们的酸性不同
D.乳酸[CH3CH(OH)COOH]分子中有2个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于合成氨N2(g)+3H2(g) ![]() 2NH3(g)ΔH=-92.4 kJ·mol-1反应,达到平衡后,以下分析正确的是
2NH3(g)ΔH=-92.4 kJ·mol-1反应,达到平衡后,以下分析正确的是
A. 升高温度,对正反应的反应速率影响更大
B. 增大压强,对正反应的反应速率影响更大
C. 减小反应物浓度,对逆反应的反应速率影响更大
D. 加入催化剂,对逆反应的反应速率影响更大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学学习小组设计了相关实验来探究元素周期律。该组同学为验证卤素单质氧化性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
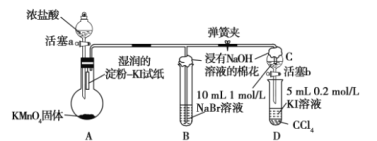
实验过程及现象:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸;
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹;
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a;
Ⅳ.打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡,静置后![]() 层溶液变为紫红色。
层溶液变为紫红色。
请回答下列有关问题。
(1)B中溶液由黄色变为棕红色时发生反应的离子方程式为______。
(2)验证氯气的氧化性强于碘的实验现象是______。
(3)B和C仪器口放置浸有![]() 溶液的棉花的作用是______。
溶液的棉花的作用是______。
(4)由此实验得出的结论:同主族元素从上到下,原子的得电子能力逐渐______(填“减弱”或“增强”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像正确的是( )
A.向CaIOH)2和NaOH的混合溶液中通入CO2 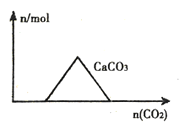
B.向1L浓度均为0.1mol/L的NaAlO2、Ba(OH)2的混合溶液中加入0.1mol/L的稀H2SO4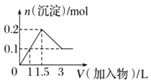
C.向1L浓度分别为0.1mol/L和0.3mol/L的AlCl3、NH4Cl的混合溶液中加入0.1mol/L的稀NaOH溶液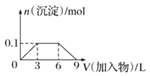
D.向氢氧化钠溶液中滴加明矾溶液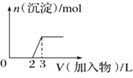
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com