
【题目】下列有关金属的工业制法中正确的是
A.制钛:用金属钠在高温下氧化TiCl4
B.炼铁:用焦炭和空气反应产生的CO在高温下还原铁矿石中铁的氧化物
C.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液
D.制镁:用海水为原料,经一系列过程制得氧化镁固体,用氢气还原氧化镁得到镁
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
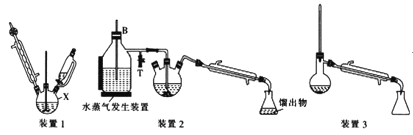
【题目】苯胺(又名氨基苯)是最重要的胺类物质之一,可作为炸药中的稳定剂、汽油中的防爆剂,也可作为医药磺胺药的原料等。苯胺为无色油状液体,有特殊气味,可用水蒸气蒸馏提纯。用纳米铁粉还原硝基苯制备苯胺的原理及装置图(略去夹持装置和加热装置)如下:
4![]() +9Fe+4H2O
+9Fe+4H2O![]() 4
4![]() +3Fe3O4
+3Fe3O4
已知部分有机物的一些数据如下表:
名称 | 密度(gmL-1) | 熔点(℃) | 沸点(℃) | 溶解性 | 备注 |
硝基苯 | 1.2037 | 5.7 | 210.8 | 难溶于水,易溶于乙醇、乙醚 | |
苯胺 | 1.0217 | -6.3 | 184.4 | 难溶于水,易溶于乙醇、乙醚 | 空气中易变质 |
乙醚 | 0.7134 | -116.3 | 34.6 | 微溶于水,易溶于乙醇 |
Ⅰ.合成:在装置1中的仪器X中,加入9g纳米铁粉、20mL水、1mL冰醋酸,加热至煮沸,煮沸3~5min后冷却至室温,再将7.0mL硝基苯逐滴加入(该反应强烈放热),搅拌、加热、回流半小时,至反应完全。
Ⅱ.分离提纯:将装置1改为装置2进行水蒸气蒸馏,取装置2中的馏出物约5~6mL,转移至分液漏斗中,分离出有机层后,水层加入1.3gNaCl固体,用乙醚萃取3次(每次用7.0mL乙醚),合并有机层和乙醚萃取液,加入粒状NaOH干燥,过滤后转移至干燥的圆底烧瓶中,水浴蒸去乙醚,残留物再利用装置3蒸馏并收集温度T℃时的馏分。
请回答下列问题:
(1)由苯制取硝基苯的化学方程式为__。
(2)仪器X的名称是__;加入硝基苯时,“逐滴加入span>”的目的是__。
(3)分离提纯过程中加入NaCl固体的作用是__。
(4)装置2和装置3都需要通冷凝水,冷凝水的作用是__;装置2中长导管B的作用是__。
(5)萃取分液操作过程中要远离明火和热源,原因是__。
(6)温度T的范围为__,实验结束得到6.0mL产物,则苯胺的产率为__(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的叙述正确的是
A.乙醇是良好的有机溶剂, 75 % 的酒精还可以灭活新冠病毒
B.苯酚有毒,沾到皮肤上可用 65 ℃的以上热水洗涤
C.乙烯、聚氯乙烯和苯分子中碳原子的杂化方式相同
D.有机物![]() 的名称是2-甲基-2-丁烯
的名称是2-甲基-2-丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
①晶体中分子间作用力越大, 分子越稳定
②原子晶体中共价键越强, 熔点越高
③干冰是 CO2 分子通过氢键和分子间作用力有规则排列成的分子晶体
④在Na2O和Na2O2晶体中,阴、阳离子数之比相等
⑤正四面体构型的分子,键角都是109°28',其晶体类型可能是原子晶体或分子晶体
⑥分子晶体中都含有化学键
⑦含4.8 g碳元素的金刚石晶体中的碳碳键的物质的量为0.8 mol
A.①②③④⑤B.②④⑦C.⑤⑥⑦D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
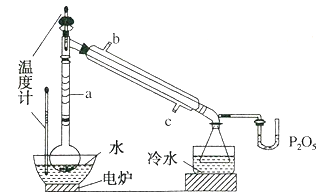
【题目】硼酸三甲酯用作柠檬类水果的熏蒸剂。实验室合成硼酸三甲酯的原理及装置如下:Na2B4O710H2O+2H2SO4+12CH3OH![]() 2NaHSO4+4(CH3O)3B+17H2O
2NaHSO4+4(CH3O)3B+17H2O
已知:
硼酸三甲酯 | 甲醇 | |
溶解性 | 与乙醚、甲醇混溶,能水解 | 与水混溶 |
沸点/℃ | 68 | 64 |
硼酸三甲酯与甲醇混合物的共沸点为54℃ | ||
实验步骤如下:
①在圆底烧瓶中加入44.8g甲醇和191.gNa2B4O710H2O(硼砂,式量为382),然后缓慢加入浓H2SO4并振荡;加热烧瓶中的液体;通过分馏柱回流一段时间。
②先接收51~55℃的馏分,再接收55~60℃的馏分。
③将两次馏分合并,加入氯化钙进行盐析分层,上层为硼酸三甲酯,分离。
④精馏得高纯硼酸三甲酯19.2g。
回答下列问题:
(1)图中仪器a的名称为__;直形冷凝管冷却水应从__(填“b”或“c”)接口进入。
(2)本实验加热方式为__,优点是__。
(3)加入氯化钙盐析分层的主要目的是__。
(4)U型管中P2O3的作用是__。
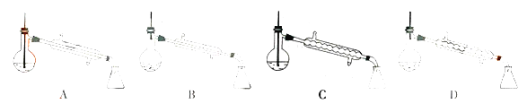
(5)图中,步骤④的仪器选择及安装都正确的是__,应收集__℃的馏分。
(6)本次实验的产率是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。则下列结论正确的是( )

A.反应进行的前3min内,用X表示的反应速率v(X)=0.3mol/(L·min)
B.容器中发生的反应可表示为:3X(g)+Y(g)2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K增大
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】航天飞船可用肼![]() 和过氧化氢
和过氧化氢![]() 为动力源.已知1g液态肼和足量液态过氧化氢反应生成氮气和水蒸气时放出
为动力源.已知1g液态肼和足量液态过氧化氢反应生成氮气和水蒸气时放出![]() 的热量.下列说法中错误的是( )
的热量.下列说法中错误的是( )
A.该反应中肼作还原剂
B.液态肼的燃烧热![]() 为
为![]()
C.该动力源的突出优点之一是生成物对环境污染小
D.肼和过氧化氢反应的热化学方程式为:![]() ;
;![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温、恒压下,1molA和1molB在一个容积可变的容器中发生反应:A(g)+2B(g)![]() 2C(g)。一段时间后达到平衡,生成amolC。下列说法不正确的是( )
2C(g)。一段时间后达到平衡,生成amolC。下列说法不正确的是( )
A.起始时和达到平衡时容器中的压强之比为1:1
B.平衡时物质A、B的转化率之比为1:2
C.平衡时A的转化率为![]()
D.当v正(A)=v逆(B)时,可判定反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤的烟气中常含有大量的NOx、CO、SO2等有害气体,治理污染、消除有害气体对环境的影响是化学工作者研究的重要课题。
Ⅰ.已知氮氧化物可采用强氧化剂Na2S2O8氧化脱除,过程如下所示:
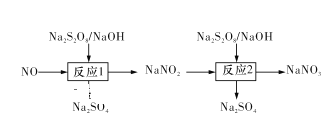
(1)写出反应1的离子方程式:____ 。
(2)反应2为NO2-+S2O82-+2OH-=NO3-+2SO42-+H2O。此反应在不同温度下达到平衡时,NO2-的脱除率与Na2S2O8初始浓度的关系如图1所示。
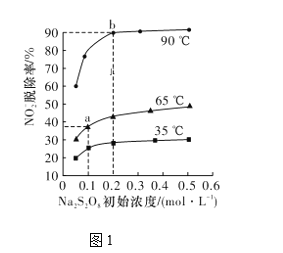
①比较a、b点的反应速率:va正____vb逆(填“>”“<”或“=”)。
②根据图像可以判断该反应为吸热反应,理由是____________。
Ⅱ.沥青混凝土可作为反应2CO(g)+O2(g)![]() 2CO2(g)的催化剂。图2表示在相同的恒容密闭容器、相同的起始浓度、相同的反应时间段下,使用相同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
2CO2(g)的催化剂。图2表示在相同的恒容密闭容器、相同的起始浓度、相同的反应时间段下,使用相同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
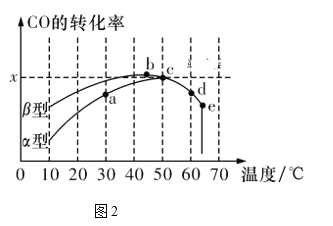
(3)下列关于图2的说法正确的是________。
A.在均未达到平衡状态时,同温下β型沥青混凝土中CO转化速率比α型要大
B.b点时CO与O2分子之间发生有效碰撞的几率在整个实验过程中最高
C.a、b、c、d四点中,达到平衡状态的只有b、c两点
D.e点转化率出现突变的原因可能是温度升高后催化剂失去活性
(4)已知c点时容器中O2浓度为0.02 mol/L,则50 ℃时,在α型沥青混凝土中CO转化反应的平衡常数K=_____________(用含x的代数式表示)。
Ⅲ.利用图3所示装置(电极均为惰性电极)可吸收SO2。
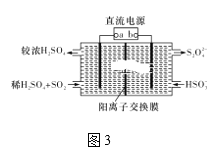
(5)直流电源b极为____,阳极发生的反应为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com