
����Ŀ������˵������ȷ����
�پ����з��Ӽ�������Խ�� ����Խ�ȶ�
��ԭ�Ӿ����й��ۼ�Խǿ�� �۵�Խ��
�۸ɱ��� CO2 ����ͨ������ͷ��Ӽ��������й������гɵķ��Ӿ���
����Na2O��Na2O2�����У�������������֮�����
���������幹�͵ķ��ӣ����Ƕ���109��28'���侧�����Ϳ�����ԭ�Ӿ������Ӿ���
���Ӿ����ж����л�ѧ��
�ߺ�4.8 g̼Ԫ�صĽ��ʯ�����е�̼̼�������ʵ���Ϊ0.8 mol
A.�٢ڢۢܢ�B.�ڢܢ�C.�ݢޢ�D.�ۢ�
���𰸡�B
��������
�ٷ��ӵ��ȶ���ȡ���ڷ����ڹ��ۼ��ܵĴ�С������Ӽ��������أ����Ӽ�������ֻӰ�����ʵ��������ʣ��ٲ���ȷ��
��ԭ�Ӿ����й��ۼ�Խǿ���ƻ������������Խ�����۵�Խ�ߣ�����ȷ��
��CO2���Ӽ䲻���γ�������۲���ȷ��
����Na2O��Na2O2�����У������ӷֱ�ΪO2-��O22-�������Ӷ�ΪNa+��������������֮�ȶ�Ϊ1��2������ȷ��
���������幹�͵ķ��ӣ�AB4�ͣ���CH4�������Ƕ���109��28����A4�ͣ���P4��������Ϊ60�����ݲ���ȷ��
��ϡ�������ǵ�ԭ�ӷ��ӣ���ϡ�������γɵķ��Ӿ����в����л�ѧ��������ȷ��
��4.8 g̼ԭ��Ϊ![]() =0.4mol�����ʯ�У�ÿ��C������4��C�γ���4��C-C���ۼ�����ƽ��ÿ��̼ԭ���γ�4��
=0.4mol�����ʯ�У�ÿ��C������4��C�γ���4��C-C���ۼ�����ƽ��ÿ��̼ԭ���γ�4��![]() =2�����ۼ������Թ��ۼ������ʵ���Ϊ0.4mol ��2=0.8 mol������ȷ��
=2�����ۼ������Թ��ۼ������ʵ���Ϊ0.4mol ��2=0.8 mol������ȷ��
�ۺ����Ϸ������ڢܢ���ȷ��
��ѡB��


 ��Ȥ������ҵ���ϿƼ�������ϵ�д�
��Ȥ������ҵ���ϿƼ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£�Ũ�ȶ���1 mol/L����������X2��Y2�����ܱ������з�Ӧ��������Z������t min��ø����ʵ�Ũ�ȷֱ�Ϊc(X2)=0.4 mol/L��c(Y2)=0.6 mol/L��c(Z2)=0.4 mol/L����÷�Ӧ�Ļ�ѧ����ʽ�ɱ�ʾΪ
A.2X2��3Y2![]() 2X2Y3B.3X2��2Y2
2X2Y3B.3X2��2Y2![]() 2X3Y2
2X3Y2
C.X2��2Y2![]() 2XY2D.2X2��Y2
2XY2D.2X2��Y2![]() 2X2Y
2X2Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016��12��1�չ��ʴ�����Ӧ�û�ѧ���ϻ����������ϳɵ�������Ԫ������Ϊ113�� (��дΪNh)��115��(Mc)��117��(Ts)��118��(Og)������˵����ȷ����
A. 113��Ԫ�ص�������Ϊ����������
B. 115��Ԫ��λ�ڵ������ڵ�VA��
C. 117��Ԫ�ص�ij��ԭ�ӣ����ں�176�����ӣ���ԭ����![]() Ts
Ts
D. 118��Ԫ�ص�ԭ���������8������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����![]() ��Ӧ�У���ʾ�÷�Ӧ����������
��Ӧ�У���ʾ�÷�Ӧ����������
A.v��A���� 0.5 mol/��L��s��B.v��B���� 0.3 mol/��L��s��
C.v��C���� 0.8 mol/��L��s��D.v��D���� 1.8 mol/��L��min��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() Ϊԭ������������������ֶ�����Ԫ�أ�A�����ڱ�ԭ�Ӱ뾶��С��Ԫ�أ�
Ϊԭ������������������ֶ�����Ԫ�أ�A�����ڱ�ԭ�Ӱ뾶��С��Ԫ�أ�![]() ͬ���������ڣ�C��L���������K���3����Eԭ�ӵĺ����������Bԭ����������2��������˵������ȷ���ǣ� ��
ͬ���������ڣ�C��L���������K���3����Eԭ�ӵĺ����������Bԭ����������2��������˵������ȷ���ǣ� ��
A.������EԪ�ص���������������������ά
B.![]() ����Ԫ���γɵĻ�������һ��ֻ�����ۼ�
����Ԫ���γɵĻ�������һ��ֻ�����ۼ�
C.��Ԫ��![]() ��ɵ�ij�ֻ��������
��ɵ�ij�ֻ��������![]() ��Ӧ����
��Ӧ����![]()
D.Ԫ��A��![]() �γɵij����������У����ȶ�����õ���AD
�γɵij����������У����ȶ�����õ���AD
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����һ��������N2��H2��Ӧ����NH3����ش�
������Ӧ���������ΪE1���������������ΪE2����E1��E2����÷�ӦΪ________(����ȡ����ȡ�)��Ӧ��
����֪��1 molH��H����1 mol N��H����1 mol N��N���ֱ���Ҫ��������436 kJ��391 kJ��946 kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ________________��
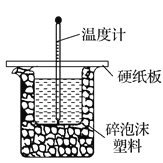
��2��ʵ������50 mL 0.50 mol��L��1������50mLijŨ�ȵ�NaOH��Һ����ͼ��ʾװ���з�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ���װ�������ԵĴ�������һ����ȱ��һ�ֲ���������������������Ϊ____________��ʵ�����ṩ��0.50 mol��L��1��0.55 mol��L��1����Ũ�ȵ�NaOH��Һ��Ӧѡ��_____________mol��L��1��NaOH��Һ����ʵ�顣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؽ����Ĺ�ҵ�Ʒ�����ȷ����
A�����ѣ��ý������ڸ���������TiCl4
B���������ý�̿�Ϳ�����Ӧ������CO�ڸ����»�ԭ����ʯ������������
C�����ƣ��ú�ˮΪԭ���Ƶþ��Σ��ٵ�ⴿ����NaCl��Һ
D����þ���ú�ˮΪԭ�ϣ���һϵ�й����Ƶ�����þ���壬��������ԭ����þ�õ�þ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�����۵���Դ�������ɽոѡ��Ӳݵȷ����ᆳ����ͺ�����ģ��йع������£�(C6H10O5)n(��ά��)+nH2O![]() 3nCO2��+3nCH4��+����
3nCO2��+3nCH4��+����
(1)�������̵�ʵ��������_________��
(2)��ʹ����������ʱ����Ҫע���������_________��
(3)������������վ������_________��ת��Ϊ���ܣ���������Ϊ_________��Դ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й������У���ȷ����
A. һ���¶��£���0.1mol/L�İ�ˮ�еμ���ͬŨ�ȵĴ��ᣬc(NH4+)/c(NH3��H2O) ��С
B. ��֪Ksp(BaSO4) = 1.1��10��10�� Ksp(BaCO3) = 2.58��10��9�����Բ��ܽ�BaSO4ת��ΪBaCO3
C. ��������Һ�ζ�ǿ����Һʱ���ü�����ָʾ��
D. ����FeCl3��Һʱ��Ϊ������ˮ�⣬�ɼ�����������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com