
【题目】常温下,向浓度均为0.1 molL-1、体积均为100 mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,lg![]() 随加入NaOH的物质的量的变化情况如图所示。下列叙述正确的是
随加入NaOH的物质的量的变化情况如图所示。下列叙述正确的是

A. HX的酸性弱于HY的
B. a点由水电离出的c(H+)=1×10-12 molL-1
C. c点溶液中:c(Y-)>c(HY)
D. b点时酸碱恰好完全中和
【答案】C
【解析】
A.未加氢氧化钠时,相同浓度溶液中,HX的![]() =12,而HY的
=12,而HY的![]() <9,由于c(H+)×c(OH-)=Kw,则HX溶液中氢离子浓度更大,故HX的酸性强于HY,A错误;
<9,由于c(H+)×c(OH-)=Kw,则HX溶液中氢离子浓度更大,故HX的酸性强于HY,A错误;
B.a点溶液![]() =12,结合c(H+)×c(OH-)=10-14可知c(OH-)=10-13 mol/L,水电离出的c(H+)等于溶液中c(OH-),即a点由水电离出的c(H+)=10-13 mol/L,B错误;
=12,结合c(H+)×c(OH-)=10-14可知c(OH-)=10-13 mol/L,水电离出的c(H+)等于溶液中c(OH-),即a点由水电离出的c(H+)=10-13 mol/L,B错误;
C.HY为0.01mol,c点加入NaOH为0.005mol,HY反应后剩余0.005mol,生成0.005molNaY,此时c点溶液为等浓度的HY、NaY混合溶液,c点溶液中![]() =6,结合c(H+)×c(OH-)=10-14可知c(H+)=10-4mol/L,溶液呈酸性,说明HY的电离程度大于Y-的水解程度,则溶液中c点溶液中:c(Y-)>c(HY),C正确;
=6,结合c(H+)×c(OH-)=10-14可知c(H+)=10-4mol/L,溶液呈酸性,说明HY的电离程度大于Y-的水解程度,则溶液中c点溶液中:c(Y-)>c(HY),C正确;
D.HY为0.01mol,b点加入NaOH为0.008mol,二者按物质的量1:1反应,故HY有剩余,D错误。
答案选C。


科目:高中化学 来源: 题型:
【题目】雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-。某同学收集了该地区的雾霾,经必要的预处理后得试样溶液,设计并完成了如图的实验:

已知:3NO3-+8Al+5OH-+2H2O![]() 3NH3↑+8AlO2-
3NH3↑+8AlO2-
根据以上的实验操作与现象,该同学得出的结论不正确的是()。
A. 试样中肯定存在NH4+、Mg2+、SO42-和NO3-
B. 试样中可能存在Na+、Cl-
C. 试样中一定不含Al3+
D. 该雾霾中可能存在NaNO3、NH4Cl和MgSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2SO2+O2![]() 2SO3是制备硫酸的重要反应,下列说法正确的是
2SO3是制备硫酸的重要反应,下列说法正确的是
A. 催化剂V2O5不改变该反应的逆反应速率
B. v(SO2)=l.0mol·L-1min-1表示的速率比v(O2)=0.01mol·L-1s-1表示的速率大
C. SO2气体通入Ba(NO3)2溶液中,溶液出现浑浊现象,说明有BaSO3沉淀生成
D. 保持容器体积不变,充入N2使容器压强增大,正逆反应速率均不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度T1和T2时,分别将0.50 mol CH4和1.20 mol NO2充入体积为1 L的密闭容器中,发生如下反应:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g),测得n(CH4)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g),测得n(CH4)随时间变化数据如下表:
时间/min | 0 | 10 | 20 | 40 | 50 | |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | …… | 0.15 |
下列说法正确的是( )
A. T1时0~10 min NO2的平均反应速率为0.15 mol·L-1·min -1
B. T2时CH4的平衡转化率为70.0%
C. 保持其他条件不变,T1时向平衡体系中再充入0.30 mol CH4和0.80 mol H2O(g),平衡向正反应方向移动
D. 保持其他条件不变,T1时向平衡体系中再充入0.50 mol CH4和1.20 mol NO2,与原平衡相比,达新平衡时N2的浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.焰色反应是化学变化
B.CO2通入CaCl2溶液中会产生白色沉淀
C.Fe3+遇KSCN溶液会产生红色沉淀
D.25 ℃,Na2CO3在水中的溶解度比NaHCO3大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是( )
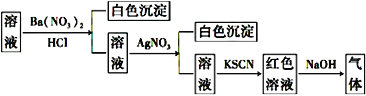
A. 原溶液中一定含有SO42-B. 原溶液中一定含有NH4+
C. 原溶液中一定含有Cl-D. 原溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】16.8gFe跟一定量浓 HNO3 反应,Fe 全部溶解,共收集NO、NO2的总体积为 11.2 L(标准状况),所得溶液中 H+的物质的量为0.02mol,请回答:
(1)反应中被还原的硝酸为_______mol。
(2)生成的 NO 与 NO2 的物质的量之比为______。
(3)写出该反应的离子方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是
A.Cu能与浓硝酸反应,但不能与浓盐酸反应
B.Cu与浓硝酸反应比与稀硝酸反应快
C.N2与O2在常温、常压下不反应,高压放电时可反应
D.块状石灰石与盐酸反应比粉末状石灰石与盐酸反应慢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com