
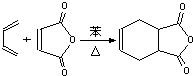
 双烯合成也称狄尔斯-阿德耳(Diels-Alder)反应,他们因此获得1950年的诺贝尔化学奖.如图:
双烯合成也称狄尔斯-阿德耳(Diels-Alder)反应,他们因此获得1950年的诺贝尔化学奖.如图:| ①KMnO4/OH-②H+ |
| CrO3,吡啶 |
| CH2Cl2 |
| 500℃ |
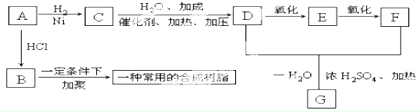
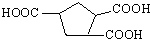 可由烃A和酯B按下列路线合成:
可由烃A和酯B按下列路线合成:
 过程.
过程. ,合信息观察反应,可知A与B应该发生Diels-Alder反应,故A为
,合信息观察反应,可知A与B应该发生Diels-Alder反应,故A为 ,B为
,B为 ;
; ,根据原子守恒,可知酯为HCOOCH3,炔为CH≡CH;
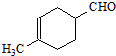
,根据原子守恒,可知酯为HCOOCH3,炔为CH≡CH; 是一个成环反应,逆推可知由CH2=CHCHO和
是一个成环反应,逆推可知由CH2=CHCHO和 ,发生Diels-Alder反应生成该有机物,根据已知③,CH3CH=CH2与Cl2在500℃下发生取代反应生成Cl-CH2CH=CH2,Cl-CH2CH=CH2在NaOH溶液中发生水解生成HO-CH2CH=CH2,根据已知②,HO-CH2CH=CH2转化为CH2=CH-CHO.
,发生Diels-Alder反应生成该有机物,根据已知③,CH3CH=CH2与Cl2在500℃下发生取代反应生成Cl-CH2CH=CH2,Cl-CH2CH=CH2在NaOH溶液中发生水解生成HO-CH2CH=CH2,根据已知②,HO-CH2CH=CH2转化为CH2=CH-CHO. ,合信息观察反应,可知A与B应该发生Diels-Alder反应,故A为
,合信息观察反应,可知A与B应该发生Diels-Alder反应,故A为 ,B为
,B为 ,则A与B反应生成C的化学方程式为:
,则A与B反应生成C的化学方程式为: ,
, ;
; ,根据原子守恒,可知酯为HCOOCH3,炔为CH≡CH,故答案为:HCOOCH3;CH≡CH;
,根据原子守恒,可知酯为HCOOCH3,炔为CH≡CH,故答案为:HCOOCH3;CH≡CH; 是一个成环反应,逆推可知由CH2=CHCHO和
是一个成环反应,逆推可知由CH2=CHCHO和 ,发生Diels-Alder反应生成该有机物,根据已知③,CH3CH=CH2与Cl2在500℃下发生取代反应生成Cl-CH2CH=CH2,Cl-CH2CH=CH2在NaOH溶液中发生水解生成HO-CH2CH=CH2,根据已知②,HO-CH2CH=CH2转化为CH2=CH-CHO,合成路线流程图为:
,发生Diels-Alder反应生成该有机物,根据已知③,CH3CH=CH2与Cl2在500℃下发生取代反应生成Cl-CH2CH=CH2,Cl-CH2CH=CH2在NaOH溶液中发生水解生成HO-CH2CH=CH2,根据已知②,HO-CH2CH=CH2转化为CH2=CH-CHO,合成路线流程图为: ,
, .
.


科目:高中化学 来源: 题型:
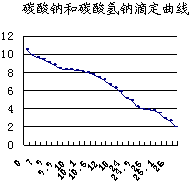 (1)滴定法是中学化学一种常见的实验方法,其根据指示剂的颜色变化指示滴定终点,然后目测标准溶液消耗体积,计算分析结果.常用的指示剂有酚酞(变色范围8.2~10.0)和甲基橙(变色范围3.1~4.4).如图为碳酸钠和碳酸氢钠混合溶液滴定曲线(横坐标为加入HCl的量,纵坐标为pH的变化),现以0.1000mol?L-1的盐酸来测定amL某浓度碳酸钠溶液的浓度,可以选用
(1)滴定法是中学化学一种常见的实验方法,其根据指示剂的颜色变化指示滴定终点,然后目测标准溶液消耗体积,计算分析结果.常用的指示剂有酚酞(变色范围8.2~10.0)和甲基橙(变色范围3.1~4.4).如图为碳酸钠和碳酸氢钠混合溶液滴定曲线(横坐标为加入HCl的量,纵坐标为pH的变化),现以0.1000mol?L-1的盐酸来测定amL某浓度碳酸钠溶液的浓度,可以选用| 实验步骤 | 结果分析 |
| 步骤1:取少量样品于试管中,加入适量蒸馏水使之溶解, | 有白色沉淀生成,说明产品中含有NaCl. |
| 步骤2:另取少量样品于锥形瓶中,加入适量蒸馏水使之溶解,加入几滴酚酞,用0.1000mol?L-1盐酸滴定至溶液由红色变无色,记录消耗盐酸的体积V1. | 说明产品中含有NaHCO3. |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠原子有强还原性,钠离子有弱氧化性 |
| B、若电解熔融的氯化钠,则钠离子被氧化成钠原子 |
| C、钠很活泼,在一定条件下可以置换出金属活动性顺序表钠后面的金属 |
| D、钠是电和热的良导体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能用丁达尔效应鉴别 |
| B、都是电解质 |
| C、将NaOH溶液加入FeCl3溶液中有红褐色沉淀生成,加入Fe(OH)3胶体则没有沉淀 |
| D、能用过滤的方法分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com