
| A、钠原子有强还原性,钠离子有弱氧化性 |
| B、若电解熔融的氯化钠,则钠离子被氧化成钠原子 |
| C、钠很活泼,在一定条件下可以置换出金属活动性顺序表钠后面的金属 |
| D、钠是电和热的良导体 |


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
| A、氢氧化镁和稀盐酸反应 |
| B、Ba(OH)2溶液滴入稀硫酸中 |
| C、澄清石灰水和稀硝酸反应 |
| D、醋酸溶液与氢氧化钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
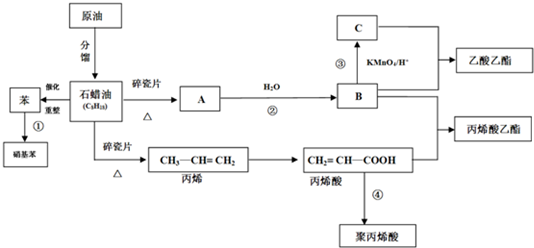
查看答案和解析>>
科目:高中化学 来源: 题型:
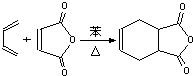 双烯合成也称狄尔斯-阿德耳(Diels-Alder)反应,他们因此获得1950年的诺贝尔化学奖.如图:
双烯合成也称狄尔斯-阿德耳(Diels-Alder)反应,他们因此获得1950年的诺贝尔化学奖.如图:| ①KMnO4/OH-②H+ |
| CrO3,吡啶 |
| CH2Cl2 |
| 500℃ |
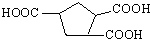 可由烃A和酯B按下列路线合成:
可由烃A和酯B按下列路线合成:
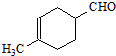 过程.
过程.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Mg2+、NO3-、Cl- |
| B、K+、Na+、HCO3-、Cl- |
| C、K+、Na+、SO42-、Cl- |
| D、NH4+、Na+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴加石蕊试液显红色的溶液:Fe3+、NH4+、C1-、SCN- |
| B、含 有大量HCO3-的溶液:NH4+、Ca2+、Mg2+、I- |
| C、c(S2-)=0.1 mol?L-1的溶液中:Na+、NH4+、ClO-、SO42- |
| D、含有大量ClO-的溶液:H+、Mg2+、I-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
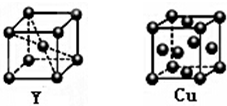 X、Y、Z、R为前四周期元素,X为地壳中含量最多的金属元素,Y元素的焰色反应为黄色,Z是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂,R基态原子3d轨道的电子数是4s轨道电子数的3倍.
X、Y、Z、R为前四周期元素,X为地壳中含量最多的金属元素,Y元素的焰色反应为黄色,Z是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂,R基态原子3d轨道的电子数是4s轨道电子数的3倍.查看答案和解析>>
科目:高中化学 来源: 题型:
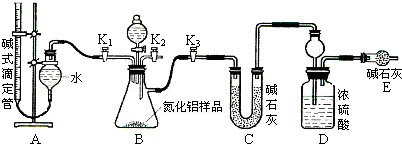
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com