
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. 新制饱和氯水中:Al3+、Cu2+、SO42-、Br-
B. 使甲基橙变红的溶液中:Mg2+、Fe3+、NO3-、SCN-
C.  =1×10-13mol·L-1的溶液中:Na+、K+、C1-、AlO2-
=1×10-13mol·L-1的溶液中:Na+、K+、C1-、AlO2-
D. 由水电离的c(H+)=1×10-13mol·L-1的溶液中:Ca2+、Ba2+、Cl-、HCO3-
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知在100 ℃下,水的离子积KW=1×10-12,下列说法正确的是( )
A. 0.05 mol/L的H2SO4溶液pH=1
B. 0.001 mol/L的NaOH溶液pH=11
C. 0.005 mol/L的H2SO4溶液与0.01 mol/L的NaOH溶液等体积混合,混合后溶液pH为6,溶液显酸性
D. 完全中和pH=3的H2SO4溶液50 mL,需要pH=11的NaOH溶液50 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.常温常压下28g氮气所含有的分子数目为NA
B.标准状况下,22.4L水中含有NA个水分子
C.2.3g金属钠变为钠离子时失去的电子数为0.2NA
D.1molL﹣1KCl溶液中含有Cl﹣的个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(本题共8分)现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第三周期元素的简单离子中半径最小 |
(1)写出元素T的原子结构示意图 。
(2)元素Y与元素Z相比,金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________(填序号)。
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈
d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式:_____ _________。
(4)元素T和氢元素可形成一种18电子的化合物Q,元素X与氢元素也能按原子个数比为1∶2形成一种18电子化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. MgO(s)+C(s)=Mg(s)+CO(g)在室温下不能自发进行,说明该反应的△H<0
B. 加水稀释0.1mol·L-1的CH3COONa溶液后,溶液中 的值增大
的值增大
C. 氟元素的非金属性强于溴元素,由此可推出酸性:HF>HBr
D. 用等物质的量浓度的NaOH溶液中和等体积且pH均为2的盐酸和醋酸溶液,盐酸消耗的NaOH溶液体积更多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )
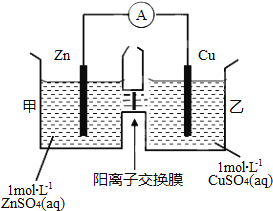
A. 铜电极上发生氧化反应
B. 电池工作一段时间后,甲池的c(SO42-)减小
C. 电池工作一段时间后,乙池溶液的总质量增加
D. 阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铵[(NH4)2SO4]一种优良的氮肥(俗称肥田粉),适用于一般土壤和作物,能使枝叶生长旺盛,提高果实品质和产量,增强作物对灾害的抵抗能力,可作基肥、追肥和种肥,与氢氧化钙在加热的条件下可以生成氨气。根据所学知识回答下列问题:
(1)基态S原子的价电子排布式为____________,能量最高的电子所处的能层的符号为_________。
(2)SO42-空间构型为__________,中心原子的轨道杂化方式是________,写出一个与SO42-互为等电子体的分子的化学式__________。
(3)氨气的沸点(-33.5℃)高于硫化氢的沸点(-60.4℃)的主要原因是:_____________________________。
(4)O、N、S的第一电离能从大到小的顺序是___________________。
(5)硫酸铜溶液中通入过量的氨气会生成[Cu(NH3)4]SO4,1mol的[Cu(NH3)4]2+中σ键的个数为________。
(6)以四氯化钛、碳化钙、叠氮酸盐作原料,可以生成碳氮化钛化合物。其结构如下图所示,这种碳氮化钛化合物的化学式为________。若将该晶体的晶胞重新切割,使碳原子位于新晶胞的上下面心,则氮原子在新晶胞中的位置是__________________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com