
【题目】很多含氯化合物都是重要的漂白剂
Ⅰ、亚氯酸钠(NaClO2)是一种常见漂白剂,某探究小组开展如下实验,回答下列问题:
制取NaClO2晶体按如下图装置进行制取。
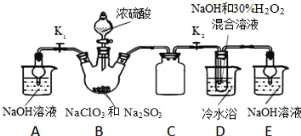
已知:NaClO2饱和溶液在低于38℃时析出NaClO23H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
(1)装置C的作用是_____________;
(2)已知装置B中的产物有ClO2气体,则装置D中反应生成NaClO2的化学方程式为___________________;装置B中反应后的溶液中阴离子除了ClO2﹣、ClO3﹣、Cl﹣、ClO﹣、OH﹣外还可能含有的一种阴离子是______;检验该离子的方法是____________________;
(3)请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。
①减压,55℃蒸发结晶;②________;③用38℃~60℃热水洗涤;④低于60℃干燥;得到成品.
(4)如果撤去D中的冷水浴,可能导致产品中混有的杂质是_______________。
Ⅱ、ClO2也是一种常见漂白剂,用ClO2处理过的饮用水常含有一定量有害的ClO![]() 。我国规定饮用水中ClO
。我国规定饮用水中ClO![]() 的含量应不超过0.20 mg·L-1。测定水样中ClO2、ClO
的含量应不超过0.20 mg·L-1。测定水样中ClO2、ClO![]() 的含量的过程如下:
的含量的过程如下:
①量取25.00 mL水样加入到锥形瓶中,并调节水样的pH为7.0~8.0。
②加入足量的KI晶体。此过程发生反应2ClO2+2I-===2ClO![]() +I2。
+I2。
③加入少量淀粉溶液,再向上述溶液中滴加1.00×10-3 mol·L-1 Na2S2O3溶液至溶液蓝色刚好褪去,消耗Na2S2O3溶液7.45 mL。此过程发生反应:2S2O![]() +I2===S4O
+I2===S4O![]() +2I-。
+2I-。
④调节第③步所得溶液至pH≤2.0,此过程发生反应ClO![]() +4H++4I-===Cl-+2I2+2H2O。
+4H++4I-===Cl-+2I2+2H2O。
⑤再向溶液中滴加1.00×10-3 mol·L-1 Na2S2O3溶液至蓝色刚好褪去,消耗Na2S2O3溶液30.00 mL
根据上述数据计算并判断该水样中ClO![]() 的含量是否符合国家规定。
的含量是否符合国家规定。
______________。
【答案】防止D瓶溶液倒吸到B瓶中 2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2 SO42﹣ 取样,先加足量的盐酸,再加BaCl2溶液,若产生白色沉淀,则说明含有SO42﹣ 趁热过滤 NaClO3和NaCl 符合
【解析】
Ⅰ、装置B中制备得到ClO2,所以B中为NaClO3和Na2SO3在浓H2SO4的作用下生成ClO2和Na2SO4,反应方程式为2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O;C可防止倒吸,起到安全瓶的作用;D中加入过氧化氢和氢氧化钠,在低温下与ClO2反应生成NaClO2,反应方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2。
(1)装置D中发生气体反应,装置内压强降低,装置C的作用是安全瓶,防止D瓶溶液倒吸到B瓶中;
(2)装置D中生成NaClO2,Cl元素的化合价降低,双氧水应表现还原性,有氧气生成,结合原子守恒可知,还有水生成,配平后方程式为:2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;B制得的气体中含有SO2,在装置D中被氧化生成硫酸,溶液中可能存在SO42-,用氯化钡溶液检验SO42-,具体操作:取少量反应后的溶液,先加足量的盐酸,再加BaCl2溶液,若产生白色沉淀,则说明含有SO42-;
(3)从溶液中制取晶体,一般采用蒸发结晶、过滤、洗涤、干燥的方法,为防止析出晶体NaClO23H2O,应趁热过滤;
(4)由题目信息可知,应控制温度38℃~60℃,高于60℃时NaClO2分解成NaClO3和NaCl,所以如果撤去D中的冷水浴,可能导致产品中混有的杂质是NaClO3和NaCl;
(5)由2ClO2+2I-===2ClO2-+I2和2S2O32-+I2===S4O62-+2I-得:2ClO2-~I2~2Na2S2O3,所以n(ClO2-) 生成= n(Na2S2O3)=1×10-3mol·L-1×7.45×10-3L=7.45×10-6 mol,
由ClO2-+4H++4I-===Cl-+2I2+2H2O和2S2O3-+I2===S4O6-+2I-得:ClO2-~2I2~4Na2S2O3,所以n(ClO2-) 总 = ![]() n(Na2S2O3) =
n(Na2S2O3) =![]() ×1×10-3 mol·L-1×30.00×10-3 L=7.50×10-6 mol,
×1×10-3 mol·L-1×30.00×10-3 L=7.50×10-6 mol,
原水样中c(ClO2-)=(7.50×10-6 mol-7.45×10-6 mol)÷0.025 L=2.00×10-6 mol·L-1,ClO2-的含量为2.00×10-6 mol·L-1×67.5×103 mg·mol-1=0.135 mg·L-1<0.2 mg·L-1,该水样中ClO2-的含量符合国家规定。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某研究小组成员在讨论鉴别浓硫酸和稀硫酸的方案时,收集了如下方案:
操作 | 结论 | |
甲 | 将火柴梗分别放入其中 | 变黑者为浓硫酸 |
乙 | 分别加入金属铝片 | 产生刺激性气味者为浓硫酸 |
丙 | 分别加入盛水的试管中 | 放热者为浓硫酸 |
丁 | 分别在 | 变白者为浓硫酸 |
(1)其中可行的是______
(2)对其中一个操做稍做改进就能成为可行方案的是______,改进方法是______。
(3)请给出另外两种鉴别方案,完成表格。
操作 | 结论 | |
A | __________ | ___________ |
B | ___________ | __________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收。
(1)在人体中进行的![]() 转化时,②中的Fe3+作______________剂;
转化时,②中的Fe3+作______________剂;
(2)“服用维生素C,可使食物中的Fe3+ 还原成Fe2+”这句话指出,维生素C在这一反应中作_____剂,具有__________________性。
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通常利用SiO2 和碳反应来制取硅,写出反应的化学方程式___________________。
工业上还可以利用镁制取硅,反应为2Mg+SiO2 = 2MgO+Si,同时会发生副反应:2Mg + Si = Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:

(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
a.石灰石 b.锌粒 c.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 ___________________________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃.用化学方程式表示这两个反应①________________________②___________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路。课外活动小组为确认生产后的废液的组成,进行如下实验:(1)取10mL废液加入足量的AgNO3溶液,生成沉淀 8.61g。(2)另取10mL废液放入铜片充分反应,铜片质量减少了0.256g。下列关于原废液组成的判断不正确的是( )
A.一定含有Fe 2+、Fe 3+、Cu2+、ClˉB.c(Clˉ) = 6mol / L,c(Fe 2+) = 0.6mol /L
C.c(Fe2+)︰c(Fe3+) = 3︰1D.c(Fe2+)︰c(Cu2+) = 2︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
①常温下,强酸溶液的pH=a,将溶液的体积稀释到原来10n倍,则pH=a+n;
②已知BaSO4的Ksp=c(Ba2+)·c(SO42-),所以在BaSO4溶液中有c(Ba2+)= c(SO42-)=![]()
③将0.1mol·L-1的NaHS和0.1mol·L-1Na2S溶液等体积混合,所得溶液中有c(S2-)+2c(OH-)=2c(H+)+c(HS-)+3c(H2S)
④在0.1 mol·L-1氨水中滴加0.1mol·L-1盐酸,刚好完全中和时pH=a,则由水电离产生的c(OH-)=10-amol·L-1
A.①④B.②③C.③④D.①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某电镀铜厂有两种废水,分别含有CN-和Cr2O72-等有毒离子,拟用NaClO和Na2S2O3按照下列流程进行处理。
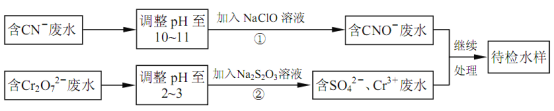
完成下列填空:
(1)HCN有剧毒,电子式是___,其分子属于___(填“极性”、“非极性”)分子。
(2)选用最详尽描述核外电子运动状态的方式,来表示氮原子的最外层电子:___,氮原子核外有___种能量不同的电子。
(3)下列事实能说明氯与硫两元素非金属性相对强弱的是___。
a.相同条件下水溶液的酸性:HClO3>H2SO3
b.稳定性:HCl>H2S
c.相同条件下水溶液的pH:Na2S>NaCl
d.还原性:S2->Cl-
(4)写出流程②的离子方程式:___。
(5)反应②中,每消耗1.5mol Cr2O72-转移电子的数目为___个。
(6)取少量待检水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀,用平衡移动原理解释产生该现象的原因___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得0.5 mol·L1CH3COONa溶液、0.5 mol·L1 CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。下列说法正确的是

A. 随温度升高,纯水中c(H+)>c(OH)
B. 随温度升高,CH3COONa溶液的c(OH)减小
C. 随温度升高,CuSO4溶液的pH变化是Kw改变与水解平衡移动共同作用的结果
D. 随温度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因为CH3COO、Cu2+水解平衡移动方向不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林(![]() )是有机合成过程中的中间体。
)是有机合成过程中的中间体。
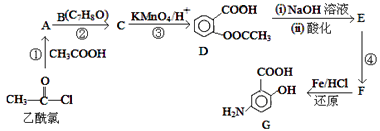
已知:Ⅰ.![]()
Ⅱ.![]() (具有较强的还原性)
(具有较强的还原性)
(1)反应④的试剂和条件为______;反应①的反应类型为______;反应②的作用是_____;
(2)B的结构简式为_______;
(3)下列关于G的描述正确的是______;
A.具有两性,既能与酸反应也能与碱反应
B.能发生加成、消去、取代和氧化反应
C.能聚合成高分子化合物
D.1molG与足量NaHCO3溶液反应放出2molCO2
(4)D与足量的NaOH溶液反应的化学方程式为_______;反应②的化学方程式为_________;
(5)符合下列条件的C的同分异构体
a.属于芳香族化合物,且含有两个甲基
b.既能发生银镜反应又能发生水解反应
其中核磁共振氢谱有4组峰,且峰面积之比为6∶2∶1∶1的是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com