


科目:高中化学 来源: 题型:
| A、仅④ | B、②和④ |
| C、③和④ | D、仅② |
查看答案和解析>>
科目:高中化学 来源: 题型:
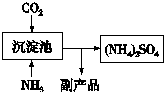
| ① |
| ② |
| ③ |
| ④ |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溴水与碘化钾溶液:Br2+2I-=2Br-+I2 |
| B、钠与水:Na+H2O=Na++OH-+H2↑ |
| C、碳酸钙与稀盐酸:CO32-+2H+=CO2↑+H2O |
| D、硫酸铜溶液与氢氧化钡溶液:Cu2++2OH-=Cu(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na元素的相对原子质量 |
| B、S元素的相对原子质量 |
| C、O元素的相对原子质量 |
| D、Se元素各同位素的丰度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
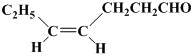 )不溶于水,是一种昂贵的食用香料,也是重要的医药中间体.M的一条合成路线如下(部分反应试剂和条件略去),且D与M互为同分异构体.
)不溶于水,是一种昂贵的食用香料,也是重要的医药中间体.M的一条合成路线如下(部分反应试剂和条件略去),且D与M互为同分异构体.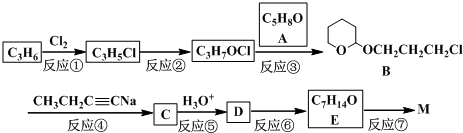
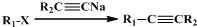
| 反应试剂 |
| 反应条件 |
| 反应试剂 |
| 反应条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
 锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).
锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com