
【题目】石油分流产品正丁烷可以按以下合成路线进行转化(生成物中的无机物忽略)

提示:
问题:
(1)D中所含官能团的名称:_____________
(2)下列反应中属于取代反应的是:______________
A.① B.② C.④ D.⑤
(3)写出反应⑦的化学方程式:________________
写出反应⑧的化学方程式:___________________
(4)高聚物X的结构简式:_________________
(5)A是直链结构,可以使Br2的CCl4溶液褪色,生成的产物最多有__________种
(6)与G具有相同官能团的同分异构体有___________种
(7)反应③的目的是_____________
【答案】 烃基、溴原子 B、D nCH3-CH=CH-COOCH3→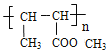 或nCH2=CHCH2COOCH3→
或nCH2=CHCH2COOCH3→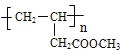 OHC-CHO+4[Ag(NH3)2]OH
OHC-CHO+4[Ag(NH3)2]OH![]() H4NOOC-COONH4+4Ag↓+6NH3+2H2O
H4NOOC-COONH4+4Ag↓+6NH3+2H2O  3 15 保护 碳碳双键不被氧化
3 15 保护 碳碳双键不被氧化
【解析】本题考查有机物的推断和合成,从官能团的性质入手,根据问题(5)A是直链结构,且能使溴的四氯化碳溶液褪色,说明A含有碳碳双键,根据题给信息,A在臭氧、氢气、Pd的作用下产生甲醛,且N能与银氨溶液反应,说明N中含有醛基,因此A可能结构简式为CH3-CH2-CH=CH2,也可能为CH2=CH-CH=CH2,假设A的结构简式为CH3CH2CH=CH2,则N为CH3CH2CHO,根据反应流程,Q为CH3CH2COOH,与乙二醇发生酯化反应,生成可能是CH3CH2COOCH2CH2OH,或CH3CH2COOCH2CH2OOCCH2CH3,无论那种形式,都不能发生聚合反应,因此A的结构简式为CH2=CH-CH=CH2,则N为OHCCHO,Q为HOOC-COOH,与乙二醇发生缩聚反应,X的结构简式为: ,反应①发生加成反应,反应②根据条件,应发生卤代烃的水解,反应③与溴的四氯化碳溶液反应,发生加成反应,说明B和C中含有碳碳双键,D与酸性高锰酸钾溶液发生羟基的氧化反应,E与甲醇在浓硫酸的作用下发生酯化反应,说明E中含有羧基,推出反应①中的溴原子应加成到 “CH2=”上,B的结构简式可能是CH2=CH-CH2-CH2Br,也可能是CH3-CH=CH-CH2Br,如果B是CH2=CH-CH2-CH2Br,C的结构简式为CH2=CH-CH2-CH2OH,D的结构简式为CH2BrCHBrCH2CH2OH,E的结构简式为CH2BrCHBrCH2COOH,F为CH2BrCHBrCH2COOCH3,G的结构简式:CH2=CHCH2COOCH3,反应⑦发生加聚反应,则H的结构简式:
,反应①发生加成反应,反应②根据条件,应发生卤代烃的水解,反应③与溴的四氯化碳溶液反应,发生加成反应,说明B和C中含有碳碳双键,D与酸性高锰酸钾溶液发生羟基的氧化反应,E与甲醇在浓硫酸的作用下发生酯化反应,说明E中含有羧基,推出反应①中的溴原子应加成到 “CH2=”上,B的结构简式可能是CH2=CH-CH2-CH2Br,也可能是CH3-CH=CH-CH2Br,如果B是CH2=CH-CH2-CH2Br,C的结构简式为CH2=CH-CH2-CH2OH,D的结构简式为CH2BrCHBrCH2CH2OH,E的结构简式为CH2BrCHBrCH2COOH,F为CH2BrCHBrCH2COOCH3,G的结构简式:CH2=CHCH2COOCH3,反应⑦发生加聚反应,则H的结构简式: ,如果B是CH3-CH=CH-CH2Br,则C结构简式为CH3CH=CHCH2OH,D的结构简式为CH3CHBrCHBrCH2OH,E的结构简式为CH3CHBrCHBrCOOH,F的结构简式为CH3CHBrCHBrCOOCH3,G结构简式为CH3CH=CHCOOCH3,H的结构简式:
,如果B是CH3-CH=CH-CH2Br,则C结构简式为CH3CH=CHCH2OH,D的结构简式为CH3CHBrCHBrCH2OH,E的结构简式为CH3CHBrCHBrCOOH,F的结构简式为CH3CHBrCHBrCOOCH3,G结构简式为CH3CH=CHCOOCH3,H的结构简式: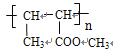 ,(1)根据上述分析,D中含有官能团是羟基和溴原子;(2)根据上述分析,属于取代反应是②⑤,故选项BD正确;(3)反应⑦的化学反应方程式:nCH2=CHCH2COOCH3→
,(1)根据上述分析,D中含有官能团是羟基和溴原子;(2)根据上述分析,属于取代反应是②⑤,故选项BD正确;(3)反应⑦的化学反应方程式:nCH2=CHCH2COOCH3→ 或者nCH3-CH=CH-COOCH3→
或者nCH3-CH=CH-COOCH3→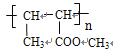 ;反应⑧OHC-CHO+4[Ag(NH3)2]OH
;反应⑧OHC-CHO+4[Ag(NH3)2]OH![]() H4NOOC-COONH4+4Ag↓+6NH3+2H2O;(4)X的结构简式为
H4NOOC-COONH4+4Ag↓+6NH3+2H2O;(4)X的结构简式为 ;(5)发生1,2-加成,生成CH2BrCH2BrCH=CH2,发生1,4-加成,生成CH2Br-CH=CH-CH2Br,两个碳碳双键都发生加成,产物是CH2BrCHBr-CHBrCH2Br,共有3种;(6)如果是甲酸某酯,存在形式可能是
;(5)发生1,2-加成,生成CH2BrCH2BrCH=CH2,发生1,4-加成,生成CH2Br-CH=CH-CH2Br,两个碳碳双键都发生加成,产物是CH2BrCHBr-CHBrCH2Br,共有3种;(6)如果是甲酸某酯,存在形式可能是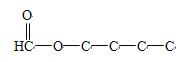
(碳碳双键有三种位置)、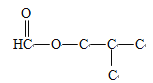
(碳碳双键两种位置)、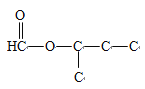 (碳碳双键三种位置),如果是乙酸某酯,则形式为
(碳碳双键三种位置),如果是乙酸某酯,则形式为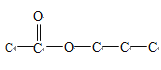 (碳碳双键有两种位置)、
(碳碳双键有两种位置)、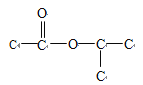 (碳碳双键有一种),如果是丙酸某酯,其形式:
(碳碳双键有一种),如果是丙酸某酯,其形式: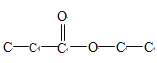 (碳碳双键有两种位置),如果是丁酸某酯,其形式:
(碳碳双键有两种位置),如果是丁酸某酯,其形式: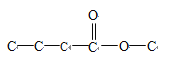 (碳碳双键有两种位置)、
(碳碳双键有两种位置)、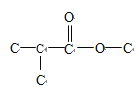 (碳碳双键有一种位置),除去本身,共有15种结构;(7)保护碳碳双键不被氧化。
(碳碳双键有一种位置),除去本身,共有15种结构;(7)保护碳碳双键不被氧化。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:①CO(g)+![]() O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是________________________________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下3.36 L CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为____________mol,放出的热量为____________kJ(用含有a和b的代数式表示)。
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH1=-574 kJ·mol-1①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若1 mol CH4还原NO2至N2,整个过程中放出的热量为867 kJ,则ΔH2=____________。
(4)某氮肥厂氨氮废水中的氮元素多以NH![]() 和NH3·H2O形式存在,该废水的处理流程中,NH
和NH3·H2O形式存在,该废水的处理流程中,NH![]() 在微生物作用的条件下经过两步反应被氧化成NO
在微生物作用的条件下经过两步反应被氧化成NO![]() 。两步反应的能量变化示意如图所示:
。两步反应的能量变化示意如图所示:
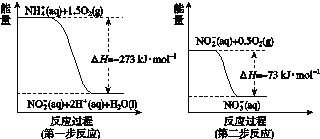
1 mol NH![]() (aq)全部氧化成NO
(aq)全部氧化成NO![]() (aq)的热化学方程式是________________。
(aq)的热化学方程式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃下,现有0.1mol·L-1的H2SO4和0.1 mol·L-1一元弱酸HA两种溶液
(1)实验测得0.1 mol·L-1一元弱酸HA 的pH为4,则HA的电离平衡常数Ka= ;
(2)0.1mol·L-1的H2SO4中水电离出的C(H+)为 ;
(3)向0.1mol·L-1的硫酸中加入一定体积的pH=13的NaOH溶液,反应后溶液的pH为2,则所需NaOH溶液与硫酸的体积比为 ;
(4)向0.1 mol·L-1一元弱酸HA加入一定体积的水,在此过程中,下列数值变大的是 ;
①c(H+) ② 电离度(α) ③c(OH-) ④ Ka ⑤c(A-)/ c(HA) ⑥n(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铜[xCuCO3·yCu(OH)2],呈孔雀绿颜色.又称为孔雀石,是一种名贵的矿物宝石。它与铜与空气中的氧气、二氧化碳和水蒸气等物质反应产生的物质。CuSO4溶液与Na2CO3溶液反应可以得到碱式碳酸铜,我们将对其组成进行相关探究。
[沉淀制备]
称取12. 5 g胆矾(CuSO4 5H2O)溶于87. 5mL蒸馏水中,滴加少量稀硫酸(体积可以忽略不计),充分搅拌后得到CuSO4溶液。向其中加入Na2CO3溶液,将所得蓝绿色悬浊液过滤,并用蒸馏水洗涤,再用无水乙醇洗涤,最后低溫烘干备用。
[实验探究]我们设计了如下装置,用制得的蓝绿色固体进行实验。

根据以上实验回答下列问题
(1)配制硫酸铜溶液的过程中滴加稀硫酸的作用是___________,所得硫酸铜溶液的溶质质量分数为_________
(2)实验室通常使用加热亚硝酸钠和氯化铵混合溶液的方法制取N2,该反应的化学方程为:__________。
⑶D装置加热前,需要首先打开活塞K,通入适量N2,然后关闭K,再点燃D处酒精灯。通入N2的作
用___________, B为安全瓶,其作用原理为_________,C中盛装的试剂应是__________。
(4)加热D后观察到的现象是________________。
(5)经查阅文献知:Ksp[CaCO3]=2.8×10-9,Ksp[BaCO3]=5.1×10-9,经讨论认为需要用Ba(OH)2溶液代替澄清石灰水来定量测定蓝绿色固体的化学式,其原因是______________
a.Ba(OH)2的碱性比Ca(OH)2强
b.Ba(OH)2溶解度大于Ca(OH)2,能充分吸收CO2
c.相同条件下,CaCO3的溶解度明显大于BaCO3
d.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
(6)待D中反应完全后,打开活塞K,再次滴加NaNO2溶液产生N2,其目的是______________。若装置F中使用Ba(OH)2溶液,实验结束后经称量,装置E的质量增加0.27g,F中产生沉淀1.97g。则该蓝绿色固体的化学式为_____________。[写成xCuCO3·yCu(OH)2的形式]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源。下图是从海水中提取某些原料的流程图。

下列有关说法正确的是( )
A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.工业上通过氯碱工业制取金属钠
C.从第③步到第⑤步的目的是浓缩、富集溴单质
D.第②步的反应条件是高温加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是
A.蒸发:应使混合物中的水分完全蒸干后,才能停止加热
B.蒸馏:开始蒸馏时应先加热再开冷凝水;蒸馏完毕,应先关冷凝水再撤酒精灯
C.分液:下层液体从分液漏斗下口放出后,再将上层液体从下口放出到另一烧杯
D.量取:用规格为10mL的量筒量取8.0mL液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在正规化学试卷的开始处总有“可能用到的相对原子质量”一项,如H:1 C:12 Cl:35.5 S:32 Cu:64等。请问这些数值准确的说法应该是
A. 某种核素的相对原子质量
B. 某种核素的原子质量
C. 某种元素的平均相对原子质量
D. 某种元素的平均相对原子质量的近似值
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com