
【题目】25℃下,现有0.1mol·L-1的H2SO4和0.1 mol·L-1一元弱酸HA两种溶液
(1)实验测得0.1 mol·L-1一元弱酸HA 的pH为4,则HA的电离平衡常数Ka= ;
(2)0.1mol·L-1的H2SO4中水电离出的C(H+)为 ;
(3)向0.1mol·L-1的硫酸中加入一定体积的pH=13的NaOH溶液,反应后溶液的pH为2,则所需NaOH溶液与硫酸的体积比为 ;
(4)向0.1 mol·L-1一元弱酸HA加入一定体积的水,在此过程中,下列数值变大的是 ;
①c(H+) ② 电离度(α) ③c(OH-) ④ Ka ⑤c(A-)/ c(HA) ⑥n(A-)
【答案】(1)1.0×10-7 mol ·L-1
(2)5.0×10-14mol ·L-1
(3)19:11
(4)②③⑤⑥
【解析】
试题分析:(1)HA的电离平衡常数Ka=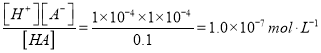 ;(2)0.1mol·L-1的H2SO4中,硫酸电离的C(H+)=0.2mol·L-1,水电离出的C(H+)为
;(2)0.1mol·L-1的H2SO4中,硫酸电离的C(H+)=0.2mol·L-1,水电离出的C(H+)为![]() 5.0×10-14mol ·L-1;(3)
5.0×10-14mol ·L-1;(3)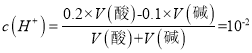 ,则所需NaOH溶液与硫酸的体积比为19:11;(4)①酸溶液越稀释c(H+)越小;② 弱酸越稀越电离,电离度(α)增大;③酸溶液越稀释c(H+)越小,
,则所需NaOH溶液与硫酸的体积比为19:11;(4)①酸溶液越稀释c(H+)越小;② 弱酸越稀越电离,电离度(α)增大;③酸溶液越稀释c(H+)越小,![]() 不变,所以c(OH-)增大;④ Ka只与温度有关,Ka不变;⑤
不变,所以c(OH-)增大;④ Ka只与温度有关,Ka不变;⑤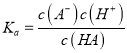 不变,c(H+)变小,c(A-)/ c(HA)增大;⑥弱酸越稀越电离,电离度(α)增大,所以n(A-)增大。
不变,c(H+)变小,c(A-)/ c(HA)增大;⑥弱酸越稀越电离,电离度(α)增大,所以n(A-)增大。


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
【题目】胶体区别于其它分散系的本质是
A. 胶体的分散质粒子直径在1nm~100nm之间
B. 胶体粒子带电荷并且在一定条件下能稳定存在
C. 胶体粒子不能穿过半透膜,能通过滤纸空隙
D. 光束通过胶体时有丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用含碳化合物合成新燃料是发展低碳经济的重要方法,已知CO(g)+2H2(g) ![]() CH3OH(g)过程能量情况如下图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )
CH3OH(g)过程能量情况如下图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )

A.该反应的ΔH=+91 kJ·mol-1
B.加入催化剂,该反应的ΔH变小
C.反应物的总能量大于生成物的总能量
D.如果该反应生成液态CH3OH,则ΔH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)+Br2(l)=2HBr(g);△H=-72kJ/mol.蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
化学物质 | H2(g) | Br2(g) | HBr(g) |
1mol分子中的化学键断裂时需要吸收的能量/KJ | 436 | a | 369 |
则表中a为( )
A.404 B.260 C.230 D.200
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
实验编号 | 起始浓度/mol·L-1 | 反应后溶液的PH | |
c(HA) | c(KOH) | ||
① | 0.1 | 0.1 | 9 |
② | X | 0.2 | 7 |
下列判断不正确的是
A. 实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B. 实验①反应后的溶液中:c(OH-)= c(K+)-c(A_)=![]() mol·L-1
mol·L-1
C. 实验②反应后的溶液中:c(A-)+c(HA)>0.1mol·L-1
D. 实验②反应后的溶液中:c(K+)=c(A-)> c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、l0lkPa下,煤炭、氢气、天然气和甲醇(CH3OH)四种燃料的热值(指一定条件下,单位质量的物质完全燃烧所放出的热量)依次是33kJ·g-1、143 kJ·g-1、56 kJ·g-1、23 kJ·g-1。则下列热化学方程式正确的是
A. C(s)+l/2O2(g)=CO(g) △H= -396kJ·mol-1
B. 2H2(g)+O2(g)=2H2O(l) △H= -286 kJ·mol-1
C. CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= -896 kJ·mol-1
D. CH3OH(l)+O2(g)=CO2(g)+2H2O(l) △H= -736 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。
(1)天然气和可燃冰(mCH4·nH2O)既是高效洁净的能源,也是重要的化工原料,
①甲烷分子的空间构型为__________,可燃冰(mCH4·nH2O)属于________晶体。
②已知25℃、101kPa时,1g甲烷完全燃烧生成液态水放出55.65kJ热量,则该条件下反应
CH4(g)+2O2(g)=CO2(g)+2H2O(l)的△H=______kJ·mol-1
(2)用甲烷-氧气碱性(KOH溶液)燃料电池作电源,电解CuCl2溶液。反应装置如下图所示:
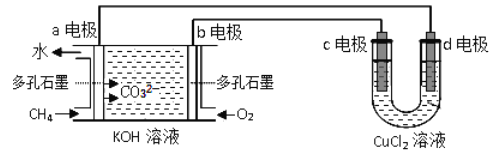
①b电极名称为___________,d电极的电极反应式为_________。
②假设CuCl2溶液足量,当某电极上析出3.2g金属Cu时,理论上燃料电池消耗氧气在标准状况下的体积是______ mL。
(3)在相同条件下,下面各组热化学方程式中,△H1<△H2的是________。(填字母)
A组:2H2(g)+O2(g)=2H2O(g) △H1 2H2(g)+O2(g)═2H2O(l) △H2
B组:S(g)+O2(g)=SO2(g) △H1 S(s)+O2(g)=SO2(g) △H2
C组:C(s)+1/2O2(g)=CO(g) △H1 C(s)+O2(g)=CO2(g) △H2
D组:CO(g)+1/2O2(g)=CO2(g) △H1 2CO(g)+O2(g)=2CO2(g) △H2
(4)25℃,10lkPa条件下,14gN2和3gH2应生成NH3的能量变化如下图所示:
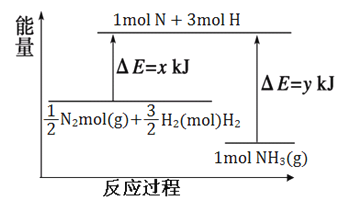
己知:①x=1127;
②25℃101kPa下,N2(g)+3H2(g)![]() 2NH3(g) △H=-92kJ·mol-1。则y=___________。
2NH3(g) △H=-92kJ·mol-1。则y=___________。
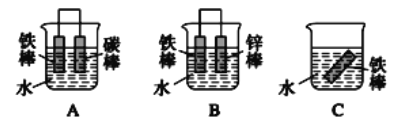
(5)金属材料的腐蚀是人类面临的严重问题,金属的防腐对节约能源、保护环境起着十分重要的作用。下列三个装置中,铁被腐蚀速率由快到慢的顺序为_________(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油分流产品正丁烷可以按以下合成路线进行转化(生成物中的无机物忽略)

提示:
问题:
(1)D中所含官能团的名称:_____________
(2)下列反应中属于取代反应的是:______________
A.① B.② C.④ D.⑤
(3)写出反应⑦的化学方程式:________________
写出反应⑧的化学方程式:___________________
(4)高聚物X的结构简式:_________________
(5)A是直链结构,可以使Br2的CCl4溶液褪色,生成的产物最多有__________种
(6)与G具有相同官能团的同分异构体有___________种
(7)反应③的目的是_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2016海南]下列有关实验操作的叙述错误的是
A.过滤操作中,漏斗的尖端应接触烧杯内壁
B.从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁
C.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
D.向容量瓶转移液体时,导流用玻璃棒可以接触容量瓶内壁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com