
【题目】下列有关实验的叙述完全正确的是

A. AB. BC. CD. D
【答案】C
【解析】
A、次氯酸钠水解生成的次氯酸具有强氧化性,能将有机色质漂白褪色;
B、氯化铜在溶液中水解生成氢氧化铜和氯化氢,加热促进氯化铜水解,生成的氯化氢易挥发使水解趋于完全生成氢氧化铜;
C、离子反应向着离子浓度减小的方向进行;
D、未反应的氯气对取代反应的产物HCl的检验产生干扰。
A项、次氯酸钠水解生成的次氯酸具有强氧化性,能将有机色质漂白褪色,不能用pH试纸测次氯酸钠溶液的pH,不能达到实验目的,故A错误;
B项、氯化铜在溶液中水解生成氢氧化铜和氯化氢,加热促进氯化铜水解,生成的氯化氢易挥发使水解趋于完全生成氢氧化铜,制备无水氯化铜应在HCl气流中蒸发,故B错误;
C项、碘化银和氯化银是同类型的难溶电解质,向浓度相同的银氨溶液中分别加入相同浓度氯化钠和碘化钠溶液,无白色沉淀生成,有黄色沉淀生成,说明碘化银溶度积小于氯化银,故C正确;
D项、氯气溶于水也能与硝酸银反应生成白色的氯化银沉淀,未反应的氯气对取代反应的产物HCl的检验产生干扰,不能达到实验目的,故D错误。
故选C。


科目:高中化学 来源: 题型:
【题目】已知p(A)=-lgc(A)。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
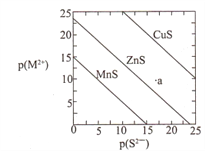
A. a点无ZnS沉淀生成
B. 可用MnS除去MnCl2溶液中混有的少量ZnCl2
C. 向CuS悬浊液中加入少量水,平衡向溶解的方向移动,c(S2-)增大
D. CuS和MnS共存的悬独液中,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化氨基汞[Hg(NH2)Cl]是祛斑霜中常用的添加剂,可由反应:Hg+2NH3+Cl2==Hg(NH2)Cl↓+NH4Cl制备,某学习小组在实验室中利用下列装置制备氯化氨基汞,回答下列问题。
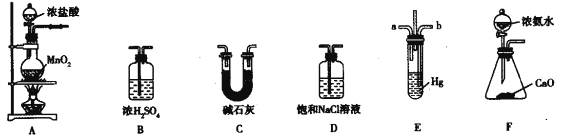
(1)A中发生反应的离子方程式为____________。
(2)F中发生反应的化学方程式为_________。
(3)盛装碱石灰的仪器名称为________,其作用为__________。
(4)整个装置的仪器连接顺序为A→________(装置不能重复使用)。该实验的不足之处是__________。
(5)E中短导管a通入的气体是__________,导管ab采用长短不同的原因是__________。
(6)氯化氨基汞产品中氯化氨基汞的含量测定:称取ag样品,加入水及稀硫酸溶解向溶解后的溶液中加入0.1mol/L KI溶液,立即出现橙红色沉淀,继续滴加KI溶液至沉淀消失,溶液呈无色[已知Hg2++2I—=HgI2↓(橙红色),HgI2+2I—=HgI42—(无色)],共消耗V mL KI溶液。测定产品中氯化氨基汞的质量分数为__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,既属于氧化还原反应又属于置换反应的是( )
A.CuO+H2![]() Cu+H2OB.CO2+Ca(OH)2=CaCO3↓+H2O
Cu+H2OB.CO2+Ca(OH)2=CaCO3↓+H2O
C.Fe2O3+3CO![]() 2Fe+3CO2D.2Na2O2+2H2O=4NaOH+O2↑
2Fe+3CO2D.2Na2O2+2H2O=4NaOH+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。俗名为“臭碱”的硫化钠广泛应用于治金、染料、皮革、电镀等工业。硫化钠的一种制备方法是Na2SO4+2C![]() Na2S+2CO2↑。下列有关说法正确的是
Na2S+2CO2↑。下列有关说法正确的是
A. 1L.0.25mol/L.Na2SO4溶液中含有的氧原子数目为NA
B. 1L.0.1mol/LNa2S溶液中含有的阴离子数目小于0.1NA
C. 生成1mol还原产物时转移电子数为8NA
D. 通常状况下,11.2L.CO2中含有的共价键数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向0.1mol/LNaA溶液中滴滴加盐酸,遇得混合溶液的pH与![]() 的变化关系如下图所示,
的变化关系如下图所示,![]() 下列叙述正确的是
下列叙述正确的是
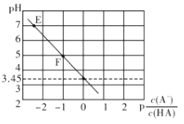
A. E点溶液中c(Na+)=c(A—)
B. Ka(HA)的数量级为10—3
C. 滴加过程中![]() 保持不变
保持不变
D. F点溶液中c(Na+)>c(HA)>c(A—)>c(OH—)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或实验操作正确的是
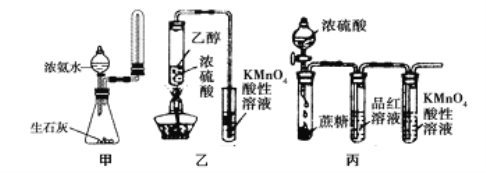
A. 实验室用图甲所示装置制取少量氨气
B. 为使100mL0.5mol/L的NaNO3溶液物质的量浓度变为1mol/L,可将原溶液加热蒸发掉50mL水
C. 利用图乙装置,可制取乙烯并验证其易被酸性KMnO4溶液氧化
D. 利用图丙装置,可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl2是一种常用的还原剂,有关数据如下:
C6H5Cl(氯苯) | C6H4Cl2 | FeCl3 | FeCl2 | |
溶解性 | 不溶于水,易溶于苯 | 不溶于C6H5Cl,C6H4Cl2,苯,易吸水 | ||
熔点/℃ | -45 | 53 | — | — |
沸点/℃ | 132 | 173 | — | — |
实验室可以用多种方法来制备无水FeCl2。回答下列问题:
Ⅰ.按下如图装置用H2还原无水FeCl3制取。
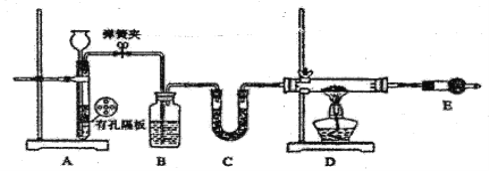
(1)用装置A制取H2,其优点是________________;D中反应的化学方程式为____________________;装置E的作用是____________________________。
(2)通入足量H2,充分反应,如果温度控制不当,产品中会含单质铁,检验产品中是否含铁的方案是____________________________。
Ⅱ.按图装置,在三颈烧瓶中放入162.5g无水氯化铁和225g氯苯,控制反应温度在128℃~139℃加热3h,反应接近100%。反应如下:2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl
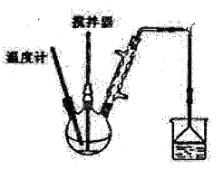
(3)上述反应中,还原剂是____________。
(4)反应温度接近或超过C6H5Cl的沸点,但实验过程中C6H5Cl并不会大量损失,原因是____________________________。
(5)冷却后,将三颈瓶内物质经过过滤,洗涤,干燥后,得到粗产品。
①洗涤所用的试剂可以是____________________________;
②简述回收滤液中C6H5Cl的方案____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列一句话中叙述了两个值,前者记为![]() ,后者记为
,后者记为![]() ,
,![]() 和
和![]() 的关系从A、B、C、D中选择,并填空。
的关系从A、B、C、D中选择,并填空。
A.![]() B.
B.![]() C.
C.![]() D.无法比较
D.无法比较
(1)常温下![]() 的
的![]() 与
与![]()
![]() 等体积混合后溶液中
等体积混合后溶液中![]() 和
和![]() :______;
:______;
(2)同温度下,![]()
![]() 溶液中
溶液中![]() 水解百分率与
水解百分率与![]() 溶液中
溶液中![]() 的水解百分率:______;
的水解百分率:______;
(3)pH值相同的醋酸和盐酸,分别用蒸馏水稀释至原来的![]() 倍和
倍和![]() 倍,稀释后两溶液的
倍,稀释后两溶液的![]() 值仍然相同,则
值仍然相同,则![]() 和
和![]() 的关系是:______;
的关系是:______;
(4)常温下两份等浓度的纯碱溶液,将第二份升高温度,两溶液中![]() :______;
:______;
(5)相同温度下,![]() 值为12的烧碱溶液中水的电离度和
值为12的烧碱溶液中水的电离度和![]() 值为12的
值为12的![]() 溶液中水的电离度:______;
溶液中水的电离度:______;
(6)将![]() 值为2的盐酸和醋酸都稀释相同倍数所得稀溶液的
值为2的盐酸和醋酸都稀释相同倍数所得稀溶液的![]() 值:______;
值:______;
(7)室温下某强酸和某强碱溶液等体积混合后,溶液的![]() 值为7,原酸溶液和原碱溶液的物质的量浓度:______;
值为7,原酸溶液和原碱溶液的物质的量浓度:______;
(8)相同温度下,![]() 的
的![]() 溶液中的
溶液中的![]() 个数和
个数和![]()
![]() 溶液中
溶液中![]() 的个数:______。
的个数:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com