
| ��ɫ | ״̬ | Ӳ�� | �ܶ� | �۵� | ������ | ������ | ��չ�� |
| ����ɫ | ���� | ���� | 2.70g/cm3 | 660.4�� | ���� | ���� | ���� |
| ʵ�鲽�� | ʵ������ | ���� |
| ��һ����ȡһ��Ͻ𣬼��������� |
�úϽ�����M��Fe��Ag��ɣ� | |
| �ڶ�����ȡ����δ��Ӧ��ȫ�Ĺ��壬���������� |
| ʵ�鲽�� | ʵ������ | ���� |
| NaOH | ������ų������岿���ܽ� | �úϽ�����M��Fe��Ag��ɣ� |
| HCl | ������ų������岿���ܽ� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ۢݢޢߢ� |
| B���٢ۢݢߢ� |
| C���٢ۢܢݢ� |
| D��ȫ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��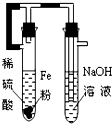 ��ȡFe��OH��2���� |
B�� ���װ�õ������� |
C�� ����HBr |
D�� �����Ԫ�صĴ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | c��һԪ�ᣩ | c��NaOH��/mol/L | �����Һ��pH |
| �� | c��HX��=0.1mol/L | 0.1 | pH=x |
| �� | c��HY��=0.1mol/L | 0.1 | pH=7 |
| �� | c��HZ��=0.1mol/L | 0.1 | pH=9 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| A����20.16 L |
| B������20.16 L |
| C������20.16 L��40.32 L֮�� |
| D������40.32 L |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com