
【题目】下列各个反应,不能用于工业生产的是
A. 二氧化锰和浓盐酸共热制氯气 B. 煅烧黄铁矿(FeS2)制SO2
C. 氯气与石灰乳反应制漂白粉 D. 电解熔融氯化镁制金属镁
 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
【题目】前两年华北地区频繁出现的雾霾天气引起了人们的高度重视,化学反应原理可用于治理环境污染,请回答以下问题。
(1)一定条件下,可用CO处理燃煤烟气生成液态硫,实现硫的回收。
①已知:2CO(g) + O2(g) = 2CO2(g) ΔH = 566 kJ·mol1
S(l) + O2(g) = SO2(g) ΔH = 296 kJ·mol1
则用CO处理燃煤烟气的热化学方程式是________________________。
②在一定温度下,向2 L 密闭容器中充入 2 mol CO、1 mol SO2发生上述反应,达到化学平衡时SO2的转化率为90%,则该温度下该反应的平衡常数K = _________________。
(2)SNCR─SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),其流程如下:

已知该方法中主要反应的热化学方程式:
4NH3(g) + 4NO(g) + O2(g) 4N2(g) + 6H2O(g) ΔH = 1646 kJ·mol1,在一定温度下的密闭恒压的容器中,能表示上述反应达到化学平衡状态的是__________________(填字母)。
a.4υ逆(N2) = υ正(O2)
b.混合气体的密度保持不变
c.c(N2):c(H2O):c(NH3)=4:6:4
d.单位时间内断裂4 mol N─H键的同时断裂4 mol N≡N键
(3)如图所示,反应温度会直接影响SNCR技术的脱硝效率。
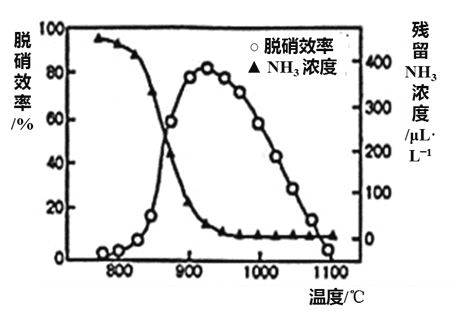
①SNCR技术脱硝的温度选择925 ℃的理由是___________________。
②SNCR与SCR技术相比,SNCR技术的反应温度较高,其原因是____________________________________;但当烟气温度高于1000℃时,SNCR脱硝效率明显降低,其原因可能是_____________________。
(4)一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示:
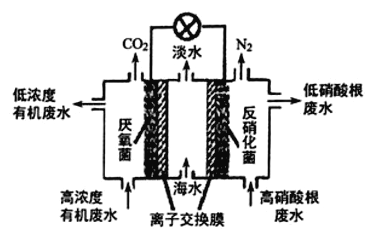
①中间室的Cl 移向_________(填“左室”或“右室”),处理后的含硝酸根废水的pH__________(填“增大”或“减小”)
②若图中有机废水中的有机物用C6H12O6表示,请写出左室发生反应的电极反应式:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有久置的氯水、新制的氯水、氯化钠、氢氧化钠四种溶液,可加入一种试剂就能区别它们,则这种试剂是
A.硝酸银溶液B.酚酞溶液C.紫色石蕊溶液D.饱和食盐水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铈是地壳中含量最高的稀土元素,二氧化铈(CeO2)是其重要的化合物。平板液晶显示屏生产过程中产生大量的废玻璃粉末,其中含CeO2、SiO2、Fe2O3等物质,某实验小组以此粉末为原料回收铈,设计流程如图所示:
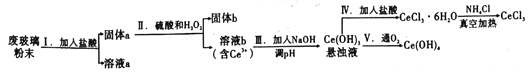
(1)步骤Ⅰ加入过量盐酸后,溶液a中的阳有离子___________________。
(2)步骤Ⅱ中反应的氧化剂和还原剂的物质的量之为___________。
(3)为了使步骤Ⅲ所得悬浊液中的Ce3+浓度为1×10-6mol·L-1,则加入NaOH调节溶液的pH应为____________[已知:Ce(OH)3的Ksp=8.0×10-21,lg2=0.3]。
(4)将NH4Cl固体与CeCl3·6H2O混合真空加热可得无水CeCl3,其中加入NH4Cl的作用是__________。
(5)第Ⅴ步反应的化学方程式是____________________;用反应得到的悬浊液制备纯净的Ce(OH)4需进行的实验操作为______________。
(6)对CeCl3样品纯度进行测定的方法:准确称取样品wg配成100mL溶液,取25.00mL置于锥形瓶中,加入稍过量的过二硫酸铵[(NH4)2S2O8]溶液将Ce3+氧化为Ce4+,然后用萃取剂[用(HT2)表示]萃取Ce4+,再用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点(其离子反应方程式为Ce4++Fe2+=Ce3++Fe3+),重复2~3次,平均消耗VmL标准溶液。
①“萃取”时存在反应:Ce4++n(HT)2![]() Ce(H2n-4)+4H+,若要提高滴定的准确率,应使溶液呈______性(填“酸”“中”或“碱”)。
Ce(H2n-4)+4H+,若要提高滴定的准确率,应使溶液呈______性(填“酸”“中”或“碱”)。
②经计算,CeCl3样品的纯度为________________。 [M(CeCl3)=246.5g·mol-1]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,反应X2(g)+Y2(g)2XY(g);△H<0,达到甲平衡.在仅改变某一条件后,达到乙平衡,图中对此过程的分析正确的是

A. 图I是加入适当催化剂的变化情况
B. 图Ⅱ是扩大容器体积的变化情况
C. 图Ⅲ是增大压强的变化情况
D. 图Ⅲ是升高温度的变化情况
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,都不能与Ag(NH3)2OH溶液发生银镜反应的一组是( )
①福尔马林;②蚁酸;③甲酸乙酯;④乙酸甲酯;⑤甲酸钠;⑥醋酸;⑦葡萄糖;⑧蔗糖;⑨麦芽糖
A.①②③④ B.④⑥⑧ C.⑦⑧⑨ D.⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐(已知:25℃,Ka(CH3COOH)=1.69×10-5)。
(1)醋酸钠溶液呈碱性的原因是_______________(写出有关的离子方程式)
(2)在CH3COONa溶液中离子浓度由大到小的顺序为_____________________(用c(Bn+)表示相应离子浓度);
(3)25℃时,0.10mol/L的醋酸溶液的pH约为___________(已知:lg1.3=0.114);
(4)对于醋酸溶液和醋酸钠溶液的下列说法正确的是____________;
A.稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸钠的水解程度减小.
B.升高温度可以促进醋酸电离,也可以促进醋酸钠水解.
C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离.
D.醋酸和醋酸钠混合液中,醋酸促进醋酸钠的水解、醋酸钠也促进醋酸的电离.
(5)物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合(注:混合前后溶液体积变化忽略不计),混合液中的下列关系式正确的是_______;
A.c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
B.c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.c(CH3COO-)+c(CH3COOH)=0.1mol/L
(6)常温时,有以下3种溶液,其中pH最小的是____________;
A.0.02molL-1CH3COOH与0.02molL-1NaOH溶液等体积混合液
B.0.03molL-1CH3COOH与0.01molL-1NaOH溶液等体积混合液
C.pH=2的CH3COOH与pH=12的NaOH溶液等体积混合液
(7)用pH试纸在常温下分别测定0.10mol/L的醋酸钠溶液和0.10mol/L的碳酸钠溶液,则pH(CH3COONa)_______ pH(Na2CO3).(填:“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴是人体必需的微量元素,含钴化合物作为颜料,具有悠久的历史,在机械制造、磁性材料等领域也具有广泛的应用,请回答下列问题:
(1)Co基态原子的电子排布式为__________________________;
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学中的光敏剂、催化剂等方面得到广泛的应用,其结构如图所示,中心离子为钴离子。
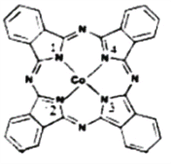
①酞菁钴中三种非金属原子的电负性有大到小的顺序为____________,(用相应的元素符号作答);碳原子的杂化轨道类型为___________________________;
②与钴离子通过配位健结合的氮原子的编号是___________________________;
(3)用KCN处理含Co2+的盐溶液,有红色的Co(CN)2析出,将它溶于过量的KCN溶液后,可生成紫色的[Co(CN)6]4-,该配离子中的配位体为________,配位原子为____________________;
(4)Co的一种氧化物的晶胞如图所示,在该晶体中与一个钴原子等距离且最近的钴原子有_____个;与一个钴原子等距离且次近的氧原子有______个;若该钴的氧化物晶体中钴原子与跟它最近邻的氧原子之间的距离为r,该钴原子与跟它次近邻的氧原子之间的距离为______;已知在该钴的氧化物晶体中钴原子的半径为apm,氧原子的半径为bpm,它们在晶体中是紧密接触的,则在该钴的氧化物晶体中原子的空间利用率为____(用含a、b的式子表示)。
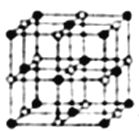
(5)筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如下图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是_______。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com