
【题目】(一)合成氨工艺(流程如图所示)是人工固氮最重要的途径。

2018年是合成氨工业先驱哈伯(PHaber)获得诺贝尔奖100周年。N2和H2生成NH3的反应为:1/2N2(g)+3/2H2(g) ![]() NH3(g) △H(298K)= - 46.2KJmol-1,在Fe催化剂作用下的反应历程为(*表示吸附态)
NH3(g) △H(298K)= - 46.2KJmol-1,在Fe催化剂作用下的反应历程为(*表示吸附态)
化学吸附:N2(g)→2N*;H2(g)→2H*;
表面反应:N*+ H*![]() NH*;NH*+ H*
NH*;NH*+ H*![]() NH2*;NH2* + H*
NH2*;NH2* + H*![]() NH3*
NH3*
脱附:NH3*![]() NH3(g)
NH3(g)
其中, N2的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。 请回答:
(1)利于提高合成氨平衡产率的条件有__________。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)标准平衡常数KΘ=![]() ,其中pΘ为标准压强(1X105Pa),p NH3、 p N2和p H2为各组分的平衡分压,如p NH3=x NH3 p,p为平衡总压,x NH3为平衡系统中NH3的物质的量分数。
,其中pΘ为标准压强(1X105Pa),p NH3、 p N2和p H2为各组分的平衡分压,如p NH3=x NH3 p,p为平衡总压,x NH3为平衡系统中NH3的物质的量分数。
①N2和H2起始物质的量之比为1:3,反应在恒定温度和标准压强下进行,NH3的平衡产率为w,则KΘ=_____________(用含w的最简式表示)
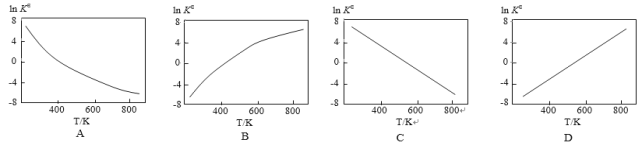
②下图中可以示意标准平衡常数KΘ随温度T变化趋势的是_______。
 (3)实际生产中,常用工艺条件,Fe作催化剂,控制温度773K,压强3.0X105Pa,原料中N2和H2物质的量之比为1:2.8。
(3)实际生产中,常用工艺条件,Fe作催化剂,控制温度773K,压强3.0X105Pa,原料中N2和H2物质的量之比为1:2.8。
①分析说明原料气中N2过量的理由________________________。
②关于合成氨工艺的下列理解,正确的是_______。
A.合成氨反应在不同温度下的△H和△S都小于零
B.控制温度(773K)远高于室温,是为了保证尽可能的平衡转化率和快的反应速率
C.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
D.基于NH3有较强的分子间作用力可将其液化,不断将液氨移去,利于反应正向进行
E.分离空气可得N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂中毒和安全事故发生。
(二)高铁酸钾(K2FeO4)可用作水处理剂。某同学通过“化学-电解法”探究的合成,其原理如图所示。接通电源,调节电压,将一定量Cl2通入KOH溶液,然后滴入含Fe3+的溶液,控制温度,可制得K2FeO4。
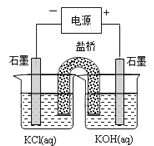
(1)请写出“化学法”得到FeO42-的离子方程式___________________________。
(2)请写出阳极的电极反应式(含FeO42-)___________________________________。
【答案】AD ![]() A 原料气中N2相对易得,适度过量有利于提高H2的转化率;N2在Fe催化剂上的吸附是决速步骤,适度过量有利于提高整体反应速率。 ADE 2Fe3++3C1O-+10OH-=2FeO42-+3Cl-+5H2O或2Fe(OH)3+3C1O-+4OH-=2FeO42-+3Cl-+5H2O Fe3++8OH—3e-=FeO42-+4H2O或Fe(OH)3+5OH--3e-=FeO42-+4H2O
A 原料气中N2相对易得,适度过量有利于提高H2的转化率;N2在Fe催化剂上的吸附是决速步骤,适度过量有利于提高整体反应速率。 ADE 2Fe3++3C1O-+10OH-=2FeO42-+3Cl-+5H2O或2Fe(OH)3+3C1O-+4OH-=2FeO42-+3Cl-+5H2O Fe3++8OH—3e-=FeO42-+4H2O或Fe(OH)3+5OH--3e-=FeO42-+4H2O
【解析】
(一)(1)由勒夏特列原理可知,根据反应![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g)△H(298K)=-46.2kJ/mol,为了提高合成氨平衡产率,即平衡正向移动,低温和高压符合条件,答案选AD;
NH3(g)△H(298K)=-46.2kJ/mol,为了提高合成氨平衡产率,即平衡正向移动,低温和高压符合条件,答案选AD;
(2)① ![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g)
NH3(g)
起始量: 1 3 0
转化量: ![]() 3
3![]() 2
2![]()
平衡量: 1-![]() 3-3
3-3![]() 2
2![]()
x(NH3)%=![]() ;x(N2)%=
;x(N2)%=![]() ;x(H2)%=
;x(H2)%=![]()
 ,化简得
,化简得![]() ;
;
②反应![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g)△H(298K)=-46.2kJ/mol为放热反应,温度T升高,平衡向逆反应方向移动,K0减小,InK0也减小,InK0与温度不成正比,故答案选A;
NH3(g)△H(298K)=-46.2kJ/mol为放热反应,温度T升高,平衡向逆反应方向移动,K0减小,InK0也减小,InK0与温度不成正比,故答案选A;
(3)①由反应![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g)可知,加过量氮气,有利于平衡正向移动,提高H2的转化率以及氨气的产率,同时根据题干“N2的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。”可知,N2在Fe催化剂上的吸附是决速步骤,适度过量有利于提高整体反应速率。②易知A选项正确;控制温度远高于室温是为了保证催化剂的活性,提高反应速率,并非为了保证尽可能高的平衡转化率和快的反应速率,B错误;恒压条件充入少量惰性气体,相当于减压,平衡逆向移动,不利于提高平衡转化率,C错误;不断将氨气液化,生成物浓度降低,有利于平衡正向移动,D正确,当选;通过天然气和水蒸气转化制得的H2,由于含有CH4,CO等易燃易爆气体,容易出现安全隐患,此外CH4,CO可能会与催化剂反应,造成催化剂活性降低,所以必须经过净化处理,E正确。答案选ADE;
NH3(g)可知,加过量氮气,有利于平衡正向移动,提高H2的转化率以及氨气的产率,同时根据题干“N2的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。”可知,N2在Fe催化剂上的吸附是决速步骤,适度过量有利于提高整体反应速率。②易知A选项正确;控制温度远高于室温是为了保证催化剂的活性,提高反应速率,并非为了保证尽可能高的平衡转化率和快的反应速率,B错误;恒压条件充入少量惰性气体,相当于减压,平衡逆向移动,不利于提高平衡转化率,C错误;不断将氨气液化,生成物浓度降低,有利于平衡正向移动,D正确,当选;通过天然气和水蒸气转化制得的H2,由于含有CH4,CO等易燃易爆气体,容易出现安全隐患,此外CH4,CO可能会与催化剂反应,造成催化剂活性降低,所以必须经过净化处理,E正确。答案选ADE;
(二)(1)将一定量C12通入KOH溶液,生成KCl和KClO,KClO具有强氧化性,将Fe3+氧化为FeO42-,然后根据碱性环境,配平即可,得到2Fe3++3C1O-+10OH-=2FeO42-+3Cl-+5H2O或2Fe(OH)3+3C1O-+4OH-=2FeO42-+3Cl-+5H2O;
(2)阳极失电子,反应物为Fe3+产物为FeO42-,然后根据碱性环境及守恒规则,易写出Fe3++8OH- -3e-=FeO42-+4H2O或Fe(OH)3+5OH--3e-=FeO42-+4H2O。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】关于烷烃的叙述不正确的是
A. 分子式符合CnH2n+2的烃一定是烷烃 B. 烷烃均能与氯水发生取代反应
C. 正丁烷的熔、沸点比异丁烷的高 D. 烷烃不能被酸性高锰酸钾溶液等强氧化剂氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X(g)+3Y (g)![]() 2W(g) +M (g) △H=-a kJ·mol-1(a>0)。一定温度下,在体积恒定的密闭容器中,加入1 mol X(g) 与1mol Y (g),下列说法正确的是
2W(g) +M (g) △H=-a kJ·mol-1(a>0)。一定温度下,在体积恒定的密闭容器中,加入1 mol X(g) 与1mol Y (g),下列说法正确的是
A. 充分反应后,放出热量为a kJ
B. 当反应达到平衡状态时,X与W的物质的量浓度之比一定为1:2
C. 当X的物质的量分数不再改变,表明该反应已达平衡
D. 若增大Y的浓度,正反应速率增大,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果不正确的是
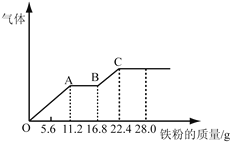
A. 混合酸中HNO3物质的量浓度为2mol/L
B. OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C. 原混合酸中H2SO4物质的量为0.4 mol
D. 第二份溶液中最终溶质为FeSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注,下述为制取Cu2O的两种方法:
方法a:用炭粉在高温条件下还原CuO
方法b:电解法,反应为2Cu+H2O![]() Cu2O+H2↑
Cu2O+H2↑
(1)已知:①2Cu(s)+![]() O2(g)=Cu2O(s)△H1=akJ/mol
O2(g)=Cu2O(s)△H1=akJ/mol
②C(s)+![]() O2(g)=CO(g) △H2=bkJ/mol
O2(g)=CO(g) △H2=bkJ/mol
③Cu(s)+![]() O2(g)=CuO(s)△H3=ckJ/mol
O2(g)=CuO(s)△H3=ckJ/mol
则方法a中反应的热化学方程式是:_________________。
(2)方法b是用肼燃料电池为电源,通过离子交换膜电解法控制电解液中OH-的浓度而制备纳米Cu2O装置如图所示:
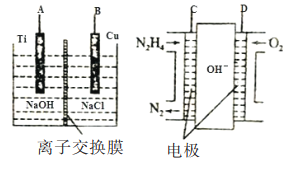
①如图装置中D电极应连______电极。(填“A”或“B”)
②该离子交换膜为______离子交换膜(填“阴”或“阳”),该电解池的B极反应式为:______。
③C极反应式为:__________。
(3)在相同体积的恒容密闭容器中,用以上方法制得的两种Cu2O分别进行催化分解水的实验:
2H2O![]() 2H2(g)+O2(g) △H>0,水蒸气的浓度随时间t变化如表所示:
2H2(g)+O2(g) △H>0,水蒸气的浓度随时间t变化如表所示:
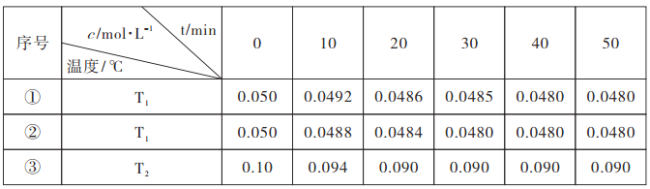
根据上述数据分析:
①催化剂的效率:实验①_______实验②(填“>”或“<”);
②通过实验①、③分析,T1______T2(填“>”或“<”);
③实验①、②、③的化学平衡常数K1、K2、K3的大小关系为:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用镀锌铁皮按下列流程制备七水合硫酸锌(ZnSO4·7H2O)
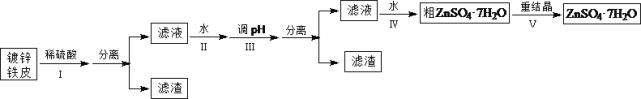
相关信息如下:①金属离子形成氢氧化物沉淀的相关pH范围。
金属离子 | pH | |
开始沉淀 | 完全沉淀 | |
Fe3+ | 1.5 | 2.8 |
Fe2+ | 5.5 | 8.3 |
Zn2+ | 5.4 | 8.2 |
②ZnSO4的溶解度(物质在100g水中溶解的质量)随温度变化曲线。
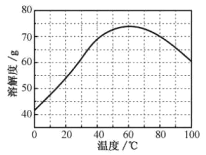
请回答:
(1)①镀锌铁皮上的油污可用Na2CO3溶液去除,理由是_______________________________。②步骤Ⅰ,可用于判断镀锌层完全反应的实验现象是_______________________________。
(2)步骤Ⅱ,需加入过量H2O2,理由是_______________________________。
(3)步骤Ⅲ,合适的pH范围是_______________________________。
(4)步骤Ⅳ,需要用到下列所有操作:a.蒸发至溶液出现晶膜;b.在60℃蒸发溶剂;c.冷却至室温;d.在100℃蒸发溶剂;e.过滤。请给出上述操作的正确顺序___________________(操作可重复使用)。
(5)步骤Ⅴ,某同学采用不同降温方式进行冷却结晶,测得ZnSO4·7H2O晶体颗粒大小分布如图1所示。根据该实验结果,为了得到颗粒大小相对均一的较大晶粒,宜选择_________方式进行冷却结晶。
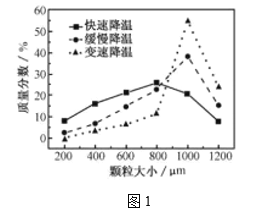
A.快速降温 B. 缓慢降温 C.变速降温
(6)ZnSO4·7H2O产品的纯度可用配位滴定法测定。
① 下列关于滴定分析,正确的是________________。
A.图2中,应将凡士林涂在旋塞的a端和旋塞套内的c端

B.滴定前,锥形瓶和滴定管均须用标准溶液润洗
C.将标准溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移
D.滴定时,通常用左手控制旋塞滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转
E.滴定前滴定管尖嘴内无气泡,滴定后尖嘴内有气泡,则测得的体积比实际消耗的小
②图3中显示滴定终点时的度数是_____________mL。
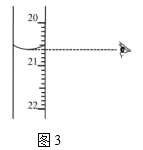
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B3C+4D中,表示该反应速率最快的是( )
A. υ(A)=0.5molL1S1 B. υ(B)=0.3 molL1S1
C. υ(C)=1.2molL1min1 D. υ(D)=0.6 molL1min1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫铁矿(主要成分为![]() )为原料制备氯化铁晶体(
)为原料制备氯化铁晶体(![]() )的工艺流程如下所示:
)的工艺流程如下所示:

下列说法不正确的是
A. “酸溶”过程中使用的酸也可以是硝酸
B. 为防止污染,“焙烧”过程中产生的![]() 应回收利用
应回收利用
C. 通入氯气的目的是氧化![]()
D. 用![]() 制取无水
制取无水![]() 时,需要在氯化氢气流中加热
时,需要在氯化氢气流中加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.用化学用语回答下列问题:
(1)写出二氧化碳分子的电子式:_______;
(2)写出氮气分子的结构式______。
Ⅱ.下列物质:①N2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩C2H6,含有极性键和非极性键的是_____;(填序号)
Ⅲ.下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④硫酸溶于水;⑤蔗糖溶于水;⑥HI分解;⑦ 碘升华;⑧溴蒸气被木炭吸附。
(1)未破坏化学键的是____;(填序号)
(2)仅离子键被破坏的是___。(填序号)
Ⅳ.下列物质:①1H、2H、3H;②H2O、D2O、T2O;③O2、O3;④14N、14C
(1)互为同位素的是:_____;(填序号)
(2)互为同素异形体的是:____;(填序号)
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有_____种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com