
【题目】每天早上5:30起床学习化学会使人变得更加可爱聪明美丽帅气,而丑陋的人则会被尿憋醒,尿的主要成分是尿素,化学式为CO(NH2)2,结构可表示为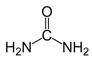 下列有关说法正确的是
下列有关说法正确的是
A.1mol CO(NH2)2分子中含有3mol δ键
B. CO(NH2)2分子中C原子、N原子的轨道杂化类型是均为sp3
C.组成尿素的四种元素第一电离能由大到小的顺序是O、N、C、H
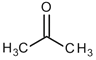
D.根据结构推测,尿素可能易溶于水,熔沸点高于丙酮![]()
![]()
科目:高中化学 来源: 题型:
【题目】类比pH的定义,对于稀溶液可以定义pC=-lgC,pKa=-lgKa,常温下,某浓度H2A溶液在不同pH值下,测得pC(H2A)、pC(HA﹣)、pC(A2﹣)变化如图所示,下列说法正确的是

A.随着pH的增大,pC增大的曲线是A2﹣的物质的量浓度的负对数
B.pH=3.50时,c(HA﹣)> c(H2A) > c(A2﹣)
C.b点时c(H2A)·c(A2﹣)/c2(HA﹣)=10﹣4.5
D.pH=3.00~5.30时,c(H2A)+c(HA﹣)+c(A2﹣)先减小后增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,相同pH的两种一元弱酸HA与HB溶液分别加水稀释,溶液pH随加水体积变化的曲线如图所示。下列说法正确的是

A. HB的酸性强于HA
B. a点溶液的导电性大于b点溶液
C. 同浓度的NaA与NaB溶液中,c(A-)=c(B-)
D. 加水稀释到pH相同时,酸HA、HB用到的水V(A)小于V(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.某价电子排布为3d14s2 的 基态原子,该元素位于周期表中第四周期第ⅢB族
B.在元素周期表中,s区,d区和ds区的元素都是金属(氢元素除外)
C.某基态原子的核外电子排布图为![]() , 它违背了泡利原理
, 它违背了泡利原理
D.Xe元素的所在族的原子的价电子排布式均为ns2np6,属于非金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)六种元素中第一电离能最小的是_________(填元素符号,下同)。
(2)黄血盐是由A、B、C、D四种元素形成的配合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式_________,黄血盐晶体中各种微粒间的作用力不涉及______________(填序号)。
a.金属键 b.共价键 c.配位键
d.离子键 e.氢键 f.分子间的作用力
(3)E2+的价层电子排布图为___________________,很多不饱和有机物在E催化下可与H2发生加成:如①CH2=CH2 ②HC≡CH ③![]() ④HCHO。其中碳原子采取sp2杂化的分子有____________(填物质序号),HCHO分子的立体结构为______________,它加成后产物甲醇的熔、沸点比CH4的熔、沸点高,其主要原因是____________。
④HCHO。其中碳原子采取sp2杂化的分子有____________(填物质序号),HCHO分子的立体结构为______________,它加成后产物甲醇的熔、沸点比CH4的熔、沸点高,其主要原因是____________。
(4)金属C、F晶体的晶胞如下图(请先判断对应的图),C、F两种晶体晶胞中金属原子的配位数之比为_________。金属F的晶胞中,若设其原子半径为r,晶胞的边长为a,根据硬球接触模型,则r = _______a,列式表示F原子在晶胞中的空间占有率______________(不要求计算结果)。
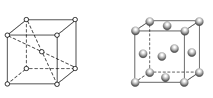
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂—铜空气燃料电池是低成本高效电池。该电池通过一种复杂的铜“腐蚀”现象产生电能,其中放电过程为2Li+Cu2O+H2O===2Cu+2Li++2OH-。下列说法不正确的是
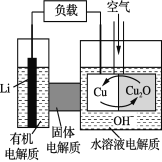
A. 放电时,Li+透过固体电解质向Cu极移动
B. 通空气时,铜被腐蚀,产生Cu2O
C. 放电时,正极的电极反应式为:Cu2O+2H+ +2 e- ===2Cu+H2O
D. 整个反应过程中,氧化剂为O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产。下列说法中正确的是
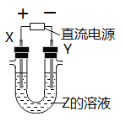
A.氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠
B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4
C.海水提镁中,X、Y均为石墨,Z为MgCl2溶液
D.电镀工业中,X是镀层金属,Y是待镀金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容密闭容器中发生反应:2SO2(g)+O2(g)![]() 2SO3(g),下列证据能说明反应一定达到化学平衡状态的是
2SO3(g),下列证据能说明反应一定达到化学平衡状态的是
A.容器内的压强不再改变B.c(SO2):c(O2):c(SO3)=2:1:2
C.混合气体的密度不再改变D.SO2的生成速率与SO3的消耗速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
A.麦芽糖与蔗糖的水解产物均含葡萄糖,故二者均为还原型二糖
B.室温下,将![]() HA溶液和
HA溶液和![]() 溶液等体积混合
溶液等体积混合![]() 忽略体积的变化
忽略体积的变化![]() 测得混合溶液的
测得混合溶液的![]() ,则混合溶液中由水电离出的
,则混合溶液中由水电离出的![]()
C.纯碳新材料“碳纳米泡沫”,每个泡沫含有约4000个碳原子,直径约6到9nm,在低于![]() 时,泡沫具有永久磁性,“碳纳米泡沫”与石墨互为同素异形体
时,泡沫具有永久磁性,“碳纳米泡沫”与石墨互为同素异形体
D.已知![]() 的
的![]() 为
为![]() ,则将等体积的
,则将等体积的![]()
![]() 的
的![]() 溶液和
溶液和![]()
![]()
![]() 溶液混合后会有
溶液混合后会有![]() 沉淀产生
沉淀产生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com